
- •Правила роботи в лабораторії хімії
- •Теоретичні питання:
- •Завдання для самопідготовки:
- •Скласти електронну та графічну конфігурацію:
- •Що спільного у будові даних атомів?___________________________________________________________
- •Як змінюються окисні властивості серед простих речовин галогенів?
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторне заняття № 2 Тема: Виявлення хлорид-йону в розчині.
- •1. Способи добування хлору.
- •Теоретичні питання :
- •Завдання для самопідготовки :
- •2.До розчину, що містить 0,585г натрій хлориду, додали розчин, що містить 3,58г арґентум нітрату, і осад відфільтрували. Що міститься у фільтраті? Яка його маса?
- •3.Як змінюється сила кислот: hf- hCl- hBr- hi? Від чого це залежить?
- •4.Яким найпростішим способом можна очистити йод від натрієвих солей галогеноводневих кислот?
- •5. Скласти рівняння реакцій та виразити їх у йонній формі (повній та скороченій) між:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Скласти рівняння реакції, за допомогою яких можна здійснити перетворення:
- •2. За допомогою рівнянь реакцій доведіть окисно-відновну подвійність sº.
- •Яка маса плюмбум(II) сульфіду утвориться при дії надлишку сірководню на плюмбум(II) нітрат масою 60г з масовою часткою солі 10%?(4,33г)
- •3.Який об’єм сірчистого газу було окиснено хлорною водою, якщо після доливання до одержаного розчину надлишку барій хлориду випало 2,33г осаду?(224мл)
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Теоретичні питання:
- •Завдання для самопідготовки:
- •Здійснити хімічне перетворення:
- •При дії розчину сульфатної кислоти на 1 кг технічного магній карбонату виділилось 224 л вуглекислого газу. Визначити масову частку домішок у зразку магній карбонату.
- •Відповідь:
- •З якими із поданих речовин взаємодіятиме розведена сульфатна кислота:
- •До яких негативних змін у природі призводять викиди в атмосферу сульфур(IV) оксиду? Відповідь проілюструвати рівняннями реакцій.
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторне заняття № 6
- •Теоретичні питання:
- •Завдання для самопідготовки:
- •1. Здійснити хімічні перетворення:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Добудьте цинк сульфат двома способами:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Скласти електронні формули атомів Нітрогену і Оксигену. Що спільного і що відмінного у їх будові?
- •2. Назвати сполуки:
- •3. Здійснити хімічні перетворення :
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Скласти рівняння реакцій та виразити їх у йонній формі (повній та скороченій) між:
- •Яку масу кальцій гідроксиду можна нейтралізувати розчином нітратної кислоти масою 50 г , у якому масова частка розчиненої речовини 12,6%?
- •Скласти окисно-відновні рівняння ( методом електронного балансу ):
- •Напишіть рівняння реакцій таких перетворень:
- •Що таке “Царська вода” ? Як діє “Царська вода” на благородні метали ? Скласти рівняння хімічної реакції.
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Завдання для самопідготовки:
- •6. Написати рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
- •7. У результаті дії на кальцій фосфід утворюється летка сполука фосфору. Напишіть рівняння реакції:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Під час нагрівання цинк оксиду з вугіллям утворюється газ, що займається на повітрі, якщо його підпалити. Напишіть відповідні рівняння.
- •Де знаходиться у природі і у яких галузях використовується вуглекислий газ?
- •При доокисненні карбон (іі) оксиду киснем одержали 6,72 л вуглекислого газу. Визначити об’єм кисню, який витратився на цей процес, якщо вихід продукту становив 85% від теоретично можливого.
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Якщо вуглекислий газ пропустити крізь воду, забарвлену лакмусом у фіолетовий колір, то забарвлення стає червоним, а під час нагрівання знову змінюється на фіолетове. Поясніть ці явища.
- •Здійснити перетворення:
- •3. Скласти рівняння реакцій та виразити їх у йонній формі (повній та скороченій) між:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Здійснити перетворення:
- •Закінчити можливі реакції:
- •4. Чи можна зберігати розчин мідного купоросу у відрах: а) оцинкованих;
- •Визначте масу калію, яку необхідно використати для приготування 200 г розчину калій гідроксиду з масовою часткою лугу 10%.
- •Лабораторна робота
- •Звіт про лабораторну роботу
- •Контрольні завдання:
- •Ряд електронегативності елементів:
- •Ряд активності металів:
Контрольні завдання:
Здійснити перетворення:
а) ZnS → H2S → SO2 → FeS2 → H2SO4;
б) S → SO2 → SO3 → H2SO4 → S
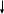
 Na2S
K2SO3
K2SO4
Na2S
K2SO3
K2SO4
При випалюванні залізного колчедану масою 96 г одержали ферум (ІІІ) оксид масою 60 г. Обчислити вихід продукту реакції за відношенням до теоретичного.
Окиснили сульфід цинку масою 19,4 г. Одержали сульфур (ІV) оксид об’ємом 3,36 л. Визначити вихід сульфур (ІV) оксиду.
Порівняти оксиди сульфуру (IV) та (VI) за складом, типом хімічного зв’язку та фізичними властивостями.
ЛАБОРАТОРНЕ ЗАНЯТТЯ № 5
Тема: Хімічні властивості розведеної сульфатної кислоти.
Література:
Ярошенко О. Г. Хімія : Підручн. для 10 кл. загальноосвіт. навч. закл. (рівень стандарту,академічнийрівень). — К. : Грамота, 2010, с. 70-72 .
Буринська К.М., Величко Л.П.”Хімія”,10клас, Київ, Ірпінь, “Перун” ,1999р. с. 30-32.
План:
1. Вивчення хімічних властивостей розведеної сульфатної кислоти:
а) взаємодія з металами;
б) оксидами металів;
в) гідроксидами;
г) солями;
д) дія сульфатної кислоти на індикатори.
2. Розв’язання задач на вихід продукту.
Знати:
1. Техніку безпеки при роботі з кислотами.
2. Властивості розведеної сульфатної кислоти.
Уміти:
1. Дотримуватись правил з техніки безпеки.
2. Економно витрачати реактиви.
3. Складати рівняння хімічних реакцій, розв’язування задач на вихід продукту.
Теоретичні питання:
Техніка безпеки при роботі з кислотами.
Виробництво сульфатної кислоти.
Фізичні властивості розведеної сульфатної кислоти.
Хімічні властивості розведеної сульфатної кислоти.
Використання сульфатної кислоти та її солей.
Завдання для самопідготовки:
Здійснити хімічне перетворення:
S → SO2 → SO3 → H2SO4 → Fe2(SO4)3

PbS → Na2SO4 → NaHSO4
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
При дії розчину сульфатної кислоти на 1 кг технічного магній карбонату виділилось 224 л вуглекислого газу. Визначити масову частку домішок у зразку магній карбонату.
Відповідь:
З якими із поданих речовин взаємодіятиме розведена сульфатна кислота:
Zn, SO2, Hg, CaCO3, NaOH, Fe(OH)3? Скласти рівняння відповідних реакцій.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
