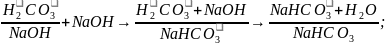- •Понятие об обмене веществ и энергии в организме. Ассимиляция и диссимиляция, их взаимосвязь и соотношение в зависимости от функционального состояния организма и его возраста.
- •Понятие об активной реакции среды, водородном показателе и его значениях в биологических жидкостях (крови, моче, слюне, желудочном и кишечном соках).
- •Понятие о буферных системах крови, их состав, названия и механизм действия.
- •Ферменты, их строение и биологическая pоль. Специфичность действия ферментов.
- •Классификация и механизм действия ферментов.
- •Влияние температуры, рН среды, активаторов и ингибиторов на активность ферментов.
- •Понятие о витаминах и их биологической роли. Классификация витаминов и механизм их действия.
- •9.Понятие о гиповитаминозе, гипервитаминозе и авитаминозе. Признаки и причины развития этих состояний организма.
- •Биологическая роль и пищевые источники водорастворимых витаминов (с, в1, в2, в6, рр).
- •Биологическая роль и пищевые источники жирорастворимых витаминов.
- •Понятие о гормонах и эндокринной системе организма. Классификация гормонов.
- •13.Биологическая роль гормонов гипофиза.
- •18..Понятие о биологическом окислении. Состав, названия и роль ферментов биологического окисления.
- •19.Понятие о макроэргических веществах и их роли в организме. Схема строения атф и ее роль в энергетическом обмене.
- •21.Понятие об углеводах, их биологическая роль и классификация.
- •22.Переваривание углеводов в пищеварительном тракте.
- •23.Понятие о состоянии гипогликемии, гипергликемии и глюкозоурии. Регуляция уровня глюкозы в крови.
- •24. Понятие о гликолизе. Образование и устранение избытка молочной кислоты (лактата). Энергетический эффект гликолиза.
- •25. Понятие об аэробном окислении углеводов. Образование ацетил-КоА из пвк.
- •26. Цикла Кребса его роль в окислении веществ. Энергетический эффект аэробного окисления углеводов.
- •27. Регуляция обмена углеводов в организме человека.
- •28. Понятие о липидах, их биологическая роль и классификация.
- •29. Переваривание и всасывание липидов в пищеварительном тракте. Роль желчных кислот в этом процессе.
- •30. Понятие о депонировании и мобилизации липидов. Транспорт липидов в организме.
- •31. Окисление глицерина. Энергетический эффект этого процесса и связь его с окислением углеводов.
- •32. Окисление жирных кислот. Энергетический эффект этого процесса
- •33. Понятие о кетоновых телах и их биологическая роль.
- •34. Регуляция обмена липидов в организме человека.
- •35. Понятие о белках, их биологическая роль и классификация.
- •36. Понятие о структуре белков и видах химической связи в молекулах белков.
- •37. Переваривание белков в пищеварительном тракте.
- •38. Понятие о катаболизме белков в клетках тканей организма. Образование и устранение аммиака. Синтез мочевины в печени.
- •39. Понятие о синтезе белков в организме. Роль днк и рнк в этом процессе.
- •40. Регуляция обмена белков.
- •1.Содержание воды, белков, углеводов, липидов и минеральных веществ в скелетных мышцах. Роль этих веществ при мышечной деятельности.
- •2. Макроэргические соединения мышц, концентрация и локализация их в мышечном волокне. Роль этих соединений в процессе сокращения мышц.
- •3. Важнейшие белки мышц: сократительные, саркоплазматические, миострамины. Биологическая роль этих белков.
- •8. Ресинтез атф в процессе гликолиза. Кинетические особенности процесса и его роль при мышечной деятельности.
- •9. Миокиназная реакция и её роль в поддержании постоянства концентрации атф в работающих мышцах.
- •10. Ресинтез атф в процессе окислительного фосфорилирования. Кинетические особенности и роль аэробного ресинтеза атф при мышечной деятельности.
- •11. Основные показатели кислородного обеспечения организма: о2-запрос, о2 –потребление, о2-дефицит, о2-долг и пмк. Величины этих показателей в состоянии покоя и при мышечной деятельности.
- •12. Последовательность развития процессов ресинтеза атф в организме при переходе от состояния покоя к мышечной деятельности.
- •18. Особенности протекания биохимических процессов в периоде отдыха после мышечной деятельности.
- •19. Явление суперкомпенсации веществ и его роль в процессе тренировки.
- •20. Гетерохронность процессов восстановления в организме после мышечной деятельности.
- •21. Специфичность биохимической адаптации организма в процессе тренировки. Биохимическое обоснование основных принципов спортивной тренировки.
- •22. Биохимические основы качества силы мышц. Биохимическое обоснование основных принципов тренировки, направленных на развитие силы.
- •23.Биохимические основы качества быстроты мышц. Биохимическое обоснование методов тренировки для развития скоростных качеств спортсмена.
- •25. Биохимическая характеристика состояния тренированности организма.
- •26. Цель, задачи и организация биохимического контроля в спорте.
- •27. Биохимическая характеристика срочного, отставленного и кумулятивного эффектов тренировки. Их роль в формировании тренированности организма.
- •28. Основные требования к методам биохимических исследований при поведении биохимического контроля в спорте.
- •29. Понятие об антидопинговом контроле в спорте.
- •30. Основные показатели крови, изучаемые при биохимическом контроле в спорте. Диагностика функционального состояния организма и его работоспособности по результатам биохимических анализов крови.
- •31. Особенности биохимической адаптации организма при выполнении физических упражнений в беге на короткие дистанции.
- •32. Особенности биохимической адаптации организма при выполнении физических упражнений в беге на средние дистанции.
- •33. Особенности биохимической адаптации организма при выполнении физических упражнений в беге на длинные дистанции.
- •34. Особенности биохимической адаптации организма при выполнении физических упражнений в плавании
- •35. Особенности биохимической адаптации организма при выполнении физических упражнений в борьбе
- •36. Особенности биохимической адаптации организма при выполнении физических упражнений в лыжных гонках.
- •37. Особенности биохимической адаптации организма при выполнении физических упражнений в спортивной ходьбе.
- •38. Особенности биохимической адаптации организма при выполнении физических упражнений в тяжёлой атлетике
- •39. Особенности биохимической адаптации организма при выполнении физических упражнений в спортивных играх.
- •40. Особенности биохимической адаптации организма при выполнении физических упражнений в гимнастике.
Химический состав организма человека и его возрастные особенности. Содержание воды, углеводов, липидов, белков и минеральных веществ в организме. Влияние физической тренировки на химический состав органов и тканей.
В организме человека обнаруживают не менее 60 химических элементов. Все элементы в зависимости подразделяют на три группы: 1. Основные: C, O, H, N – до 98%; 2. Макроэлементы: содержится в количествах >0,001% P, S, Ca, Na, K, Cl.;3. Микроэлементы: <0,001%: Cu, Fe, Co, B, Zn, Si, Mo. Организм: 1. H2O (60-65%), 2. Сухой остаток: органические (углеводы 1,5-2% , липиды 12-15%, белки 18-20%); минеральные 3-5% (соли: карбонаты, фосфаты, хлориды, сульфаты и др.; кислоты: HCl; ионы: K+, Na+, Ca++, HCO3,). Химический состав организма изменяется в зависимости от возраста и занятие спорта. В растущем организме больше воды и меньше УБЖ минеральных веществ. В пожилом возрасте содержание воды уменьшается, снижается содержание белков, может увеличивается содержание жиров. При скоростно-силовых нагрузках в организме более значительно увеличивается содержание белков, креатин фосфата, ферментов анаэробного энергообеспечения, меньше накапливаются углеводы в мышцах и печени. При нагрузках на выносливость, более значительно увеличивается содержание углеводов в мышцах и печени. В меньшей степени увеличивается содержание белков. Лучше развиты системы ферментов аэробного обеспечения.
Понятие об обмене веществ и энергии в организме. Ассимиляция и диссимиляция, их взаимосвязь и соотношение в зависимости от функционального состояния организма и его возраста.
Обмен веществ – это строго упорядоченная система биохимических процессов ассимиляции и диссимиляции, необходимых для нормальной жизнедеятельности организма. Ассимиляция – это совокупность биохимических процессов синтеза веществ и накопление энергии в клетках. Диссимиляция – это совокупность биохимических процессов распада веществ и освобождение энергии в клетках. Интенсивность обмена веществ наиболее высокая на ранних этапах развития в растущем организме. С возрастом постепенно снижается. Значительно понижается у людей престарелого возраста. В растущем организме преобладают ассимиляции необходимые для нормального роста и развития организма. У взрослого человека в возрасте 20-30 лет ассимиляция и диссимиляция уравновешены. В пожилом организме начинают проявляться процессы преобладания диссимиляции (особенно по белкам и азот содержащим вещества). У спортсменов в покое ассимиляция и диссимиляция уравновешены. При физических нагрузках преобладают процессы диссимиляции. В периоде отдыха преобладают процессы ассимиляции с постепенным выравниваем к состоянию равновесия.
Понятие об активной реакции среды, водородном показателе и его значениях в биологических жидкостях (крови, моче, слюне, желудочном и кишечном соках).
Под активной реакции среды понимают способность водных растворах влиять на химические и биологические свойства веществ в зависимости от концентрации ионов [H+], [OH-]. Другие ионы на активную реакцию среды не влияют. Различают три вида реакции среды: 1. Нейтральная [H+]=[OH-], pH=7,0; 2. Кислая среда [H+]>[OH-], pH<7,0; 3. Щелочная среда [H+]<[OH-], pH>7,0.
Активная реакция среды отражается в значениях водородного показателя pH=-lg[H+].
pHводы=-lg[10-7]=7,0
Величины pH в биологических жидкостях: слюна – рН=6,8 (близкая к нейтральной).; желудочный сок – pH=1,5-2 (кислая).; кишечный сок – pH=7,9-9 (щелочная).; кровь – pH=7,4 (слабо щелочная).; моча – pH=5,5.
Понятие о буферных системах крови, их состав, названия и механизм действия.
Буферные системы – это двухкомпонентные химические системы обеспечивающие постоянство pH и активной реакции среды. При добавлении к буферному раствору сильной кислоты или щёлочи, один компонент нейтрализует избыток ионов H+, другой компонент – избыток ионов OH. Сохранение стабильности pH обеспечивает стабильность биохимических процессов в клетках. Мы более чувствительны к изменению pH среды – ферменты, которые являются катализаторами химических процессов. Буферные системы препятствуют снижению рН.
Основными буферными системами в организме являются: бикарбонатная – H2CO3+NaHCO3; фосфатная – NaH2PO4+Na2HPO4; ацетатная – CH3COOH+CH3COONA; аммонийная – NH4Cl+NH4OH; белковая – белок-кислота+белок-соль. Молекулы белков содержат аминокислоты, в составе которых имеются свободные амина группы и карбоксильные группы.
Пример буферного действия: