
- •Термодинамико-топологический анализ фазовых диаграмм как основа синтеза схем разделения Учебное пособие для самостоятельной работы студентов
- •8. Выявление условий работоспособности простейшего комплекса 77
- •1. Подсистемы химико-технологической системы. Классификация свойств. Диаграммы состав - свойство
- •2. Термодинамические закономерности и моделирование фазовых равновесий
- •2.1. Термодинамические основы фазовых равновесий в многокомпонентных неидеальных системах
- •2.2. Математическое моделирование фазовых равновесий
- •3. Локальные закономерности структур фазовых диаграмм
- •3.1. Процессы, протекающие в поле градиента скалярного свойства
- •3.2. Процесс равновесного открытого испарения
- •4. Нелокальные закономерности диаграмм фазового равновесия (на примере систем "жидкость-пар")
- •5. Классификация диаграмм и их преобразования при варьировании давления (температуры)
- •5.1. Классификация диаграмм трех- и четырехкомпонентных систем
- •5.2. Тангенциальная азеотропия и биазеотропия
- •6. Уравнение процесса ректификации, его анализ. Синтез принципиальных схем ректификации
- •6.1. Уравнение ректификации. Векторные поля рабочих нод и движущей силы процесса
- •6.2. Общие подходы к синтезу технологических схем разделения.
- •6.3. Методы разделения и принципы их выбора
- •7. Принцип перераспределения полей концентраций между областями разделения и приемы его реализации
- •7.1. Реализация принципа перераспределения полей концентраций в процессах ректификационного разделения жидких смесей за счет варьирования внешних параметров
- •7.2. Реализация принципа перераспределения полей концентраций при разделении смесей с различными особенностями фазового поведения
- •7.3. Реализация принципа перераспределения полей концентраций при сочетании различных процессов
- •7.4. Реализация принципа перераспределения полей концентраций в процессах с разделяющими агентами
- •8. Выявление условий работоспособности простейшего комплекса
- •8.1. Тройные системы
- •8.2. Влияние состава исходной смеси на работоспособность комплексов
- •8.3. Четырехкомпонентные смеси
- •Алгоритм анализа балансовых соотношений в четырехкомпонентной системе:
- •Литература
7. Принцип перераспределения полей концентраций между областями разделения и приемы его реализации
Во всех фазовых диаграммах за исключением одной, отвечающей зеотропным смесям, концентрационный симплекс системы или его составляющие распадаются на замкнутые концентрационные ячейки развития процесса ректификации. Границами между отдельными ячейками выступают сепаратрисы седел, а в частном случае бинарных смесей - азеотропные точки. Для тройных систем границей является линия (сепаратриса), для четырехкомпонентных смесей - сепаратрические поверхности, а для симплексов большей размерности, равной n-1 (где n - число компонентов), - сепаратрические гиперповерхности размерности n-2 (сепаратрические многообразия). Таким образом, развитие процесса ректификации в любой двухсекционной колонне ограничено, т.е. не все составы достижимы. Ограничения такого рода имеют термодинамический характер и подобны ограничениям при проведении химических реакций. Аналогичная картина наблюдается для фазовых диаграмм "жидкость-твердое тело", т.е. для процессов кристаллизации.
Разнообразие структур фазовых диаграмм "жидкость-пар" обусловлено наличием азеотропов с максимумом и минимумом температур кипения и седловидных азеотропов разного порядка, что приводит, как уже отмечалось, к разбиению концентрационного симплекса на ряд областей развития процесса. Разделение таких смесей на чистые компоненты или фракции заданного состава возможно при использовании принципа перераспределения полей концентраций (ПППК) между областями разделения.
Различные приемы реализации принципа перераспределения полей концентраций описывались в специальной литературе в виде конкретных методов разделения бинарных и многокомпонентных смесей, начиная с сороковых годов 20 века. Их арсенал непрерывно пополняется в связи с развитием физико-химических основ процессов разделения. В применении к процессам разделения сущность принципа перераспределения заключается в следующем. Так как фазовые диаграммы в общем случае распадаются на ряд областей протекания процессов разделения, то один и тот же состав или совокупность составов, представляемых некоторым полем концентраций, принадлежат попеременно разным областям разделения в зависимости либо от особенностей проведения процесса, либо от особенностей фазового поведения смесей при разных внешних параметрах. Таким образом, тип фазовой диаграммы и свойства динамической системы разделения - это две неотъемлемые характеристики каждого из используемых приемов. В настоящее время наибольшее распространение получили четыре группы методов разделения, ориентированных на указанный принцип.
7.1. Реализация принципа перераспределения полей концентраций в процессах ректификационного разделения жидких смесей за счет варьирования внешних параметров
Первая группа приемов предусматривает использование ректификационного метода разделения с набором двухсекционных колонн и преобразованной диаграммы фазового равновесия. Преобразование структуры фазовой диаграммы можно осуществить двояко. Одно из них заключается в том, чтобы область разделения, в которой находится состав исходной смеси, распространилась бы на все концентрационное пространство. Этого можно достичь за счет изменения внешних параметров фазового равновесия, например, давления, сделав азеотропную систему зеотропной, которой свойственна единственная область ректификации. Теоретической базой таких преобразований является теория тангенциальной азеотропии (см. подраздел 5.2).
Данный
прием является предельным. Его реализация
во многих случаях наталкивается на
принципиальные затруднения. Это связано
с тем, что теория тангенциальной
азеотропии описывает переход от одной
грубой структуры к другой через тонкие
структуры, а правила сопряжения особых
точек связаны с необходимыми, но не
достаточными условиями такого перехода.
Сама эволюция азеотропных точек при
изменении внешних параметров, т.е.
изменение состава азеотропа при
варьировании давления (температуры),
подчиняется определенным законам. Так,
при допущении идеального поведения
паровой фазы в условиях, далеких от
критических, изменение состава азеотропа
с температурой (давлением) описывается
уравнением Сторонкина-Морачевского,
которое является математической записью
известного закона Вревского. Направление
движения бинарного азеотропа в этих
условиях определяется разностью
парциальных молярных теплот испарения
![]() .
.
Поскольку
![]() и
и
![]() являются нелинейными функциями
температуры и состава, то могут
реализоваться случаи, когда
являются нелинейными функциями
температуры и состава, то могут
реализоваться случаи, когда
![]() .
Им соответствуют точки возврата
азеотропа, или поворотные точки. Эти
точки являются точками экстремума
зависимости хаз(Т).
Все возможные виды зависимостей состава
азеотропа от температуры, в том числе
экстремальных, представлены на рис.
7.1-7.2.
.
Им соответствуют точки возврата
азеотропа, или поворотные точки. Эти
точки являются точками экстремума
зависимости хаз(Т).
Все возможные виды зависимостей состава
азеотропа от температуры, в том числе
экстремальных, представлены на рис.
7.1-7.2.
Если состав бинарного азеотропа характеризуется максимумом концентрации компонента 1, то тангенциальный азеотроп в этом случае не наблюдают и, следовательно, диаграмма сохраняет свою топологическую структуру. Здесь переход к другой грубой структуре в технологически приемлемом диапазоне давлений исключен.
С другой стороны, если концентрация первого компонента уменьшается, для азеотропа, например, с минимумом температуры кипения имеется второе ограничение, несовместимое с азеотропией и связанноес наличием псевдоидеальной точки х*, для которой ln(1/2)=0. Это ограничение снимается только в случае наличия точки Банкрофта, для которой справедливо ln (P01/P02) = 0. Аналогичные закономерности наблюдаются для азеотропа с максимумом температуры кипения. Нельзя не отметить еще один случай, когда азеотроп при изменении температуры (давления) достигает тангенциальности (х1=1, х2=0), исчезает, а потом вновь появляется, но движется в обратную сторону (рис. 7.1 д, е и рис.7.2 л,м).
Таким образом, наличие экстремальных точек на зависимости хаз(Т) существенно сокращает диапазон изменения состава азеотропа и ограничивает возможности реализации описанного выше предельного приема реализации ПППК. Прием также не применим, когда разность парциальных молярных теплот испарения очень мала. В этом случае азеотроп почти неподвижен.
Если азеотроп изменяет свой состав при варьировании внешних условий, но по каким-то причинам (наличие поворотных точек, достижение критической точки или выпадение твердой фазы) тангенциальный азеотроп недостижим, может быть реализован другой прием, который также базируется на принципе перераспределения полей концентраций между областями ректификации. Этот прием был предложен для разделения бинарных азеотропных смесей с минимумом температуры кипения С.В. Львовым, а для азеотропных смесей с максимумом температуры кипения - Н.И. Гельпериным (рис. 7.3).
В данном случае используются геометрические особенности фазовых диаграмм, при разных условиях принадлежащих одному и тому же топологическому типу. Суть приема заключается в том, что один и тот же состав за счет передвижения границы между областями ректификации при изменении внешних параметров принадлежит то одной области, то другой.

Рис. 7.1. Возможные виды зависимостей состава азеотропа от температуры
в системах без точек Банкрофта
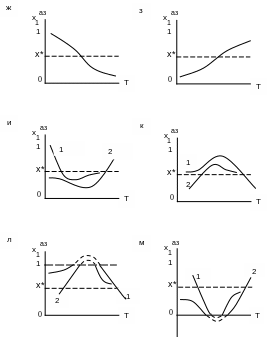
Рис. 7.2. Возможные виды зависимостей состава азеотропа от температуры
в системах с точками Банкрофта
Здесь необходимым условием является пересечение областей ректификации, соответствующих разным внешним параметрам, например, разным давлениям. На рис. 7.3 представлены фазовые диаграммы и структуры разделительных комплексов бинарных азеотропных смесей.
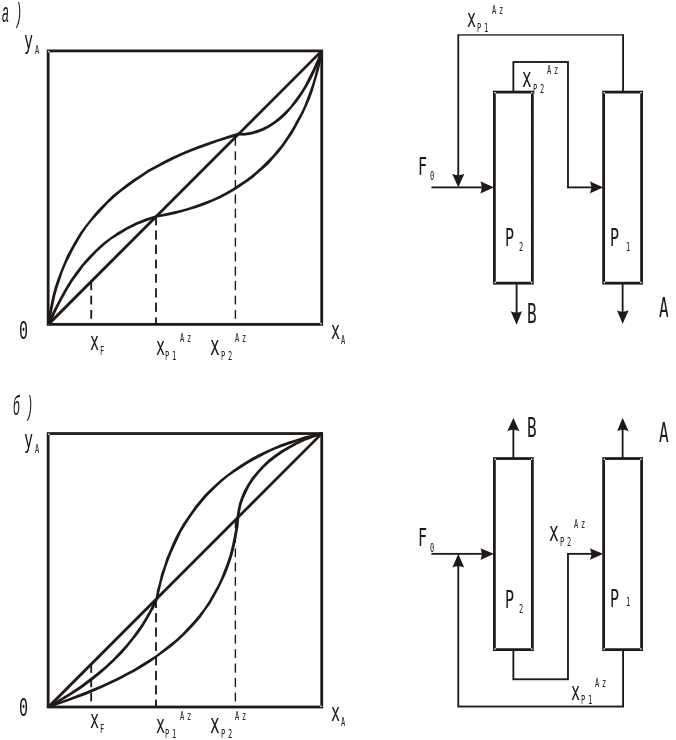
Рис. 7.3. Разделение бинарных азеотропных смесей в комплексах колонн, работающих под разным давлением а) положительный азеотроп; б) отрицательный азеотроп
Очевидно,
что условием их использования при
разделении многокомпонентных смесей
является размещение таких комплексов
на концах технологической цепочки.
Исследование особенностей функционирования
двухколонных ректификационных комплексов
показало, что их применение целесообразно
только при наличии заметного азеотропного
сдвига
![]() ,
который связан с величиной кратности
рецикла
соотношением:
,
который связан с величиной кратности
рецикла
соотношением:
![]() (7.1)
(7.1)
На практике разделение под разными давлениями бинарных азеотропных смесей реализовано, в частности, в производстве этилцеллозольва: при разделении карбинольной фракции используется подвижность азеотропа этиленгликоль - этилкарбинол, состав которого меняется на 0.17 м.д. при варьировании давления от 10 до 760 мм рт. ст.
Описанный прием применим и для разделения многокомпонентных смесей, что иллюстрируют примеры разделения трехкомпонентных смесей. Для модельной системы класса (3.2.1- 2b) на рис. 7.4 показано перераспределение областей составов при изменении давления в ректификационных колоннах. Изменение составов бинарных азеотропов приводит к перемещению границ областей ректификации, при этом появляется область составов, одновременно принадлежащая различным областям протекания разделительного процесса.
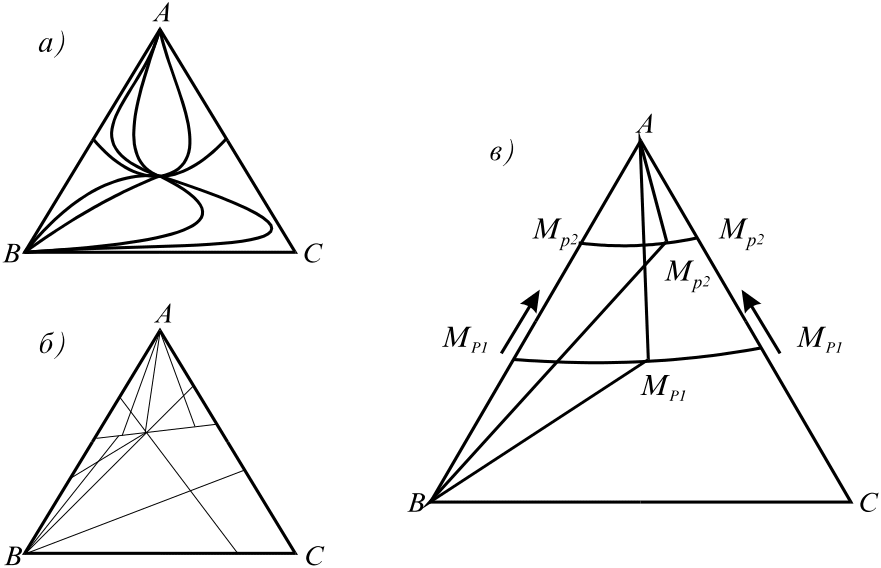
Рис. 7.4. Фазовая диаграмма (а), области составов конечных продуктов при непрерывной ректификации (б) и перераспределение составов между областями разделения при изменении давления (в)
М и М - бинарные азеотропы; М - тройной азеотроп
Рассмотрим
трехколонный комплекс разделения смеси
муравьиная кислота - уксусная кислота
– вода, являющейся фракцией оксидата
прямогонного бензина, на практически
чистые компоненты. Структура фазовой
диаграммы этой системы класса (3.1.1 -1)
характеризуется наличием трехкомпонентного
седловинного азеотропа и бинарного
азеотропа с максимумом температуры
кипения. При изменении давления
топологическая структура фазового
портрета остается неизменной, смещаются
только границы между областями
ректификации. Динамическая система
ректификации в каждой из колонн схемы
остается качественно неизменной при
преобразованиях фазовой диаграммы. На
рис. 7.5 представлена одна из возможных
структур комплекса разделения смеси
(вода - муравьиная кислота - уксусная
к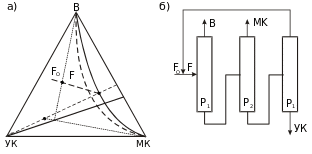 ислота)
конкретного состава и линии материального
баланса на диаграмме фазового равновесия.
ислота)
конкретного состава и линии материального
баланса на диаграмме фазового равновесия.
Рис. 7.5. Линии материального баланса (а) и схема разделения смеси вода (В) - муравьиная кислота (МК) - уксусная кислота (УК) при варьировании давления: ______ давление Р1 _ _ _ _ _ _ давление Р2
Рассмотренный технологический прием порождает рецикловый поток, обусловленный термодинамическими ограничениями фазового равновесия. Наличие рецикловых потоков является обязательным элементом схем разделения, ориентированных на принцип перераспределения полей концентраций, и, таким образом, каждому приему реализации данного принципа можно поставить в соответствие разделительный комплекс как совокупность аппаратов, охваченных обратными связями. Такие комплексы могут выступать основной структурной единицей синтеза схем разделения сложных смесей.
