Ответы на вопросы к Колловиуму № 1
.doc
|
№ 30 Медиаторы воспаления: виды, происхождение и значение в развитии воспалительного процесса.
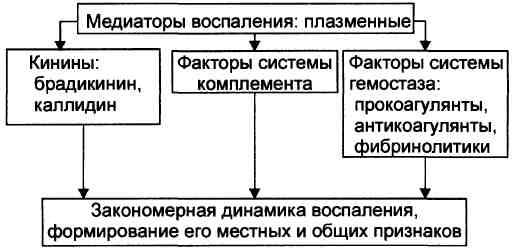
МЕДИАТОРЫ ВОСПАЛЕНИЯ - БАВ, • образующиеся при воспалении, • обеспечивающие закономерный характер его развития и исходов, • формирование его местных и общих признаков Все медиаторы воспаления или их неактивные предшественники образуются в различных клетках организма. Тем не менее их подразделяют на клеточные и плазменные (рис.).
Клеточные медиаторы высвобождаются в очаге воспаления уже в активированном состоянии непосредственно из клеток, в которых они синтезировались и накопились. Плазменные медиаторы образуются в клетках и выделяются в межклеточную жидкость, лимфу и кровь, но не в активном состоянии, а в виде предшественников. Эти вещества активируются под действием различных промоторов преимущественно в плазме крови. Они становятся физиологически дееспособными и поступают в ткани. Чёткую границу между клеточными и плазменными медиаторами воспаления удаётся провести далеко не всегда. Предложено множество классификаций медиаторов воспаления. Все они содержат в качестве классифицирующих несколько критериев. Поэтому рассматриваемые медиаторы воспаления подразделены на группы и подгруппы в соответствии со сложившимися представлениями.
|
№ 31 Сосудистые реакции и изменения крово- и лифообразования в очаге воспаления: стадии, механизмы, проявления и значение.
Компонент воспаления «сосудистые реакции и изменения крово- и лимфообращения» является результатом альтерации ткани. Понятие «сосудистые реакции» подразумевает изменения тонуса стенок сосудов, их просвета, крово- и лимфообращения в них, проницаемости сосудистых стенок для клеток и жидкой части крови.
При воспалении на разных стадиях сосудистых реакций происходят следующие важные и последовательные процессы. • Повышение тонуса стенок артериол и прекапилляров, сопровождающееся уменьшением их просвета и развитием ишемии. • Снижение тонуса стенок артериол, сочетающееся с увеличением их просвета, развитием артериальной гиперемии, усилением лимфообразования и лимфооттока. • Уменьшение просвета венул и лимфатических сосудов, нарушение оттока крови и лимфы по ним с развитием венозной гиперемии и застоя лимфы. • Дискоординированное изменение тонуса стенок артериол, венул, пре- и посткапилляров, лимфатических сосудов, сочетающееся с увеличением адгезии, агрегации и агглютинации форменных элементов крови, её сгущением и развитием стаза. ИШЕМИЯ При воздействии на ткань флогогенного агента, как правило, развивается кратковременное (на несколько секунд) повышение тонуса ГМК стенок артериол и прекапилляров, т.е. локальная вазоконстрикция. Эта первая стадия сосудистых реакций в виде местной вазоконстрикции приводит к нарушению кровотока — ишемии. Причины. Причина вазоконстрикции — высвобождение под влиянием альтерирующего фактора БАВ с сосудосуживающим эффектом: катехоламинов, тромбоксана А2, Пг, лейкотриенов. Преходящий характер вазоконстрикции и ишемии объясняется быстрой инактивацией катехоламинов ферментами (главным образом мо-ноаминоксидазой), разрушением Пг и лейкотриенов в реакциях окисления. Значение. Значение ишемии состоит в локализации повреждающего влияния флогогенного агента и в препятствии его распространению за пределы очага непосредственного контакта с тканью. Проницаемость стенок микрососудов на этом этапе сосудистых реакций ещё не увеличена. АРТЕРИАЛЬНАЯ ГИПЕРЕМИЯ Вторая стадия сосудистых реакций в виде расширения просвета артериол и прекапилляров приводит к артериальной гиперемии — увеличению притока артериальной крови и кровенаполнения ткани. Механизмы Из механизмов, приводящих к развитию артериальной гиперемии, важное значение имеют нейрогенный, гуморальный и миопаралитический. Нейрогенный механизм (холинергический по своему существу) развития артериальной гиперемии характеризуется: • увеличением высвобождения парасимпатическими нервными окончаниями ацетилхолина; • повышением чувствительности холинорецепторов к ацетилхолину, что, как правило, наблюдается в условиях избытка внеклеточного содержания К+ и Н+ (характерно для очага воспаления). Гуморальный механизм. Гуморальный компонент механизма развития артериальной гиперемии заключается в местном увеличении образования медиаторов с сосудорасширяющим действием: кининов, ПгЕ, Пг1, аденозина, оксида азота, гистамина. Миопаралитический механизм заключается в уменьшении базального тонуса артериол. Значение и последствия. При артериальной гиперемии к тканям увеличивается приток кислорода, субстратов метаболизма и в связи с этим возрастает фильтрационное давление. Последнее в регионе артериальной гиперемии ведёт к некоторому повышению объёма межклеточной жидкости с низким содержанием белка (транссудата). Одновременно происходят активация обмена веществ и синтеза новых клеточных и неклеточных структур взамен повреждённых или погибших. ВЕНОЗНАЯ ГИПЕРЕМИЯ Параллельно с вышеуказанными изменениями, как правило, появляются признаки венозной гиперемии в виде увеличения просвета посткапилляров и ве-нул и замедления в них тока крови. Предстаз Через некоторое время появляются периодические маятникообразные движения крови «вперёд - назад». Это является признаком перехода венозной гиперемии в состояние, предшествующее стазу (предстаз). Причины венозной гиперемии и предстаза Известны следующие основные причины венозной гиперемии и предстаза. • Сдавление венул экссудатом. • Сужение просвета венул микротромбами, агрегатами форменных элементов крови, набухшими клетками эндотелия. • Снижение тонуса стенок венул в результате уменьшения возбудимости их нервно-мышечных элементов, а также повреждения их волокнистых структур и межклеточного вещества под действием флогогенного фактора, избытка медиаторов воспаления, в том числе ферментов (эластаз, коллаге-наз, других гидролаз). • Сгущение крови, повышение её вязкости и понижение в связи с этим текучести, что определяется повышенным выходом плазмы крови в ткань при экссудации. • Скопление большого количества лейкоцитов у стенок посткапилляров и венул (феномен краевого стояния лейкоцитов). СТАЗ Четвёртая стадия сосудистых реакций — стаз — характеризуется дискоордини-рованным изменением тонуса стенок микрососудов и как следствие — прекращением тока крови и лимфы в очаге воспаления. Длительный стаз ведёт к развитию дистрофических изменений в ткани и гибели отдельных её участков. ЗНАЧЕНИЕ И ПОСЛЕДСТВИЯ ВЕНОЗНОЙ ГИПЕРЕМИИ И СТАЗА Значение венозной гиперемии и стаза в очаге воспаления состоит в изоляции очага повреждения (благодаря препятствию оттоку крови и лимфы из него и тем самым содержащихся в них микробов, токсинов, продуктов метаболизма, ионов, БАВ и других агентов, способных повредить другие ткани и органы организма). При венозной гиперемии и стазе происходят дальнейшие расстройства специфической и неспецифической функций тканей, дистрофические и структурные изменения в них вплоть до некроза. Повышение проницаемости стенок микрососудов способствует образованию экссудата. |
№ 32 Экссудация и выход форменных элементов крови в ткань при воспалении: причины, механизмы развития, проявления и значение.
Артериальная и венозная гиперемия, стаз и повышение проницаемости стенок микрососудов в очаге воспаления сопровождаются выходом плазмы, а также форменных элементов крови из микрососудов в ткани и/или полости тела с образованием экссудата (рис.).
Процесс экссудации начинается вскоре после действия повреждающего фактора на ткань и продолжается до начала репаративных реакций в очаге воспаления. экссудат - жидкость, выходящая из микрососудов, содержащая большое количество белка и, как правило, форменные элементы крови. Накапливается в тканях и/или полостях тела при воспалении. Причины экссудации Основная причина экссудации — увеличение проницаемости стенок микрососудов вследствие множества процессов, повреждающих их стенку и перечисленных на рис.
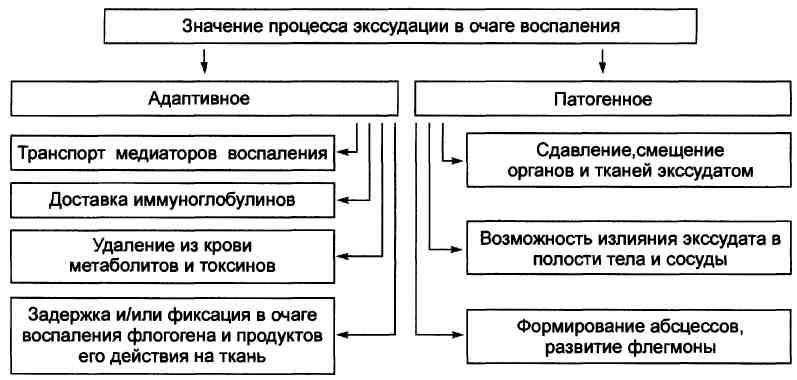
Значение экссудации В очаге воспаления процесс экссудации имеет двоякое биологическое значение: адаптивное и патогенное (рис.).
Факторы потенциации Существует группа факторов, потенцирующих образование экссудата. • Увеличение перфузионного давления (усиливает фильтрацию жидкости через сосудистую стенку). • Возрастание площади экссудации (в результате растяжения стенок микрососудов). • Повышение проницаемости базальной мембраны сосудов (под влиянием медиаторов воспаления). • Увеличение осмотического и онкотического давления в очаге воспаления. • Усиление трансцитоза. • Снижение эффективности резорбции жидкости в посткапиллярном отделе сосудов микроциркуляторного русла. |
|
|
||
|
|
|
№ 33 Фагоцитоз: его значение в развитии воспалительного процесса. Незавершённый фагоцитоз: причины и последствия.
ФАГОЦИТОЗ - активный биологический процесс, заключающийся в поглощении чужеродного материала и его внутриклеточной деструкции специализированными клетками организма — фагоцитами. Фагоцитоз осуществляют специальные клетки — фагоциты (преимущественно макрофаги и нейтрофилы). В ходе фагоцитоза образуются большие эндоцитоз-ные пузырьки — фагосомы. Фагосомы сливаются с лизосомами и формируют фаголизосомы. Фагоцитоз индуцируют сигналы, воздействующие на рецепторы в плазмолемме фагоцитов (например, AT, опсонизирующие фагоцитируемую частицу). Терминология Применительно к процессу фагоцитоза применяют следующие уточняющие определения: • Собственно фагоцитоз: поглощение клеток, их фрагментов и их внутриклеточное переваривание. • Незавершённый фагоцитоз (см. ниже). • Иммунный (специфический) фагоцитоз и опсонизация (см. ниже). • Неспецифический фагоцитоз характерен, например, для альвеолярных макрофагов, захватывающих пылевые частицы различной природы, сажу и т.п. • Ультрафагоцитоз — захватывание фагоцитом мелких корпускулярных частиц (пыли, попадающей с воздухом в лёгкие, или инородных частиц в тканях). СТАДИИ ФАГОЦИТОЗА В процессе фагоцитоза условно выделяют несколько основных стадий: • Сближение фагоцита с объектом фагоцитоза. • Распознавание фагоцитом объекта поглощения и адгезия к нему. • Поглощение объекта фагоцитом с образованием фаголизосомы. • Разрушение объекта фагоцитоза. НЕЗАВЕРШЁННЫЙ ФАГОЦИТОЗ Поглощённые фагоцитами бактерии обычно погибают и разрушаются, но некоторые микроорганизмы, снабжённые капсулами или плотными гидрофобными клеточными стенками, захваченные фагоцитом, могут быть устойчивы к действию лизосомальных ферментов или способны блокировать слияние фаго-сом и лизосом. В силу этого обстоятельства они на длительное время остаются в фагоцитах в жизнеспособном состоянии. Такая разновидность фагоцитоза получила название незавершённого. Существует множество причин незавершённого фагоцитоза, основные из них перечислены на рис.
Многие факультативные и облигатные внутриклеточные паразиты не только сохраняют жизнеспособность внутри клеток, но и способны размножаться. Персистирование патогенов опосредуют три основных механизма. • Блокада фагосомо-лизосомального слияния. Этот феномен обнаружен у вирусов (например, у вируса гриппа), бактерий (например, у микобакте-рий) и простейших (например, у токсоплазм). • Резистентность к лизосомальным ферментам (например, гонококки и стафилококки). • Способность патогенных микроорганизмов быстро покидать фагосомы после поглощения и длительно пребывать в цитоплазме (например, риккетсии). |
№ 34 Острое и хроническое воспаление: их взаимосвязь. Причины, условия возникновения, проявления и последствия. Связь воспаления, иммунитета и аллергии.
ОСТРОЕ ВОСПАЛЕНИЕ Острое воспаление характеризуется: • интенсивным течением и завершением воспаления обычно в течение 1—2 недель (в зависимости от повреждённого органа или ткани, степени и масштаба их альтерации, реактивности организма и др.); • умеренно выраженной альтерацией и деструкцией тканей, экссудативных и пролиферативных изменений в очаге повреждения при нормергическом характере воспаления. При гиперергическом его течении в очаге воспаления доминируют альтерация и разрушение тканей. Хроническое воспаление Хроническое воспаление может быть первичным и вторичным. • Если течение воспаления после острого периода приобретает затяжной характер, то оно обозначается как «вторично-хроническое». • Если воспаление изначально имеет персистирующее — вялое и длительное — течение, его называют «первично-хроническим». Учитывая, что в очаге хронического воспаления находят большое количество мононуклеарных фагоцитов и лимфоцитов, хроническое воспаление (в том числе специфические его формы при ряде инфБ) обозначают как мононуклеарно--инфильтративное. Проявления хронического воспаления Для хронического воспаления характерен ряд признаков: гранулёмы, капсула, некроз, преобладание моноцитарного и лимфоцитарного инфильтрата. • Формирование гранулём (например, при туберкулёзном, бруцеллёзном или сифилитическом воспалении). • Значительная инфильтрация очага воспаления различными видами лейкоцитов, но преимущественно моноцитами и лимфоцитами. • Образование фиброзной капсулы (например, при наличии в ткани инородного тела или отложении солей кальция). • Частое развитие некроза в центре очага хронического воспаления. Протекает такое воспаление в течение многих лет и даже всей жизни пациента (например, у больных проказой, туберкулёзом, токсоплазмозом, хроническими формами пневмонии, гломерулонефрита, гепатита, ревматоидного артрита и др.). Причины хронического воспаления Причины хронического воспаления многообразны.
Условия, способствующие хроническому течению воспаления К условиям, способствующим хроническому, персистирующему течению воспаления, относят многочисленные патогенетические моменты. • Значительное накопление в очаге воспаления активированных макрофагов. •Длительная стимуляция макрофагов различными цитокинами, иммунными комплексами, продуктами распада микробов или клеток организма. • Миграция в очаг воспаления избыточного количества полиморфно-ядерных лейкоцитов. • Активация ангиогенеза в очаге хронического воспаления. • Названные выше и другие факторы приводят к накоплению в очаге воспаления большого числа активированных макрофагов.
|
№ 35 Местные и общие проявления воспаления: причины, механизмы развития и взаимосвязь. Принципы терапии воспаления.
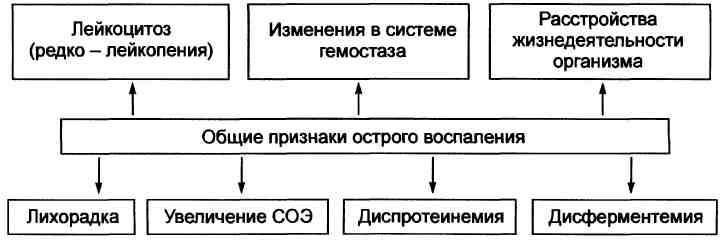
Признаки острого воспаления Признаки острого воспаления и их основные причины подразделяют на местные и общие (системные). МЕСТНЫЕ ПРИЗНАКИ ОСТРОГО ВОСПАЛЕНИЯ Местные признаки острого воспаления сформулированы ещё в античности. К ним отнесены rubor, tumor, dolor, calor, functio laesa. Rubor Причины покраснения (лат. rubor): артериальная гиперемия; увеличение числа, а также расширение артериол и прекапилляров; возрастание количества функционирующих капилляров, заполненных артериальной кровью; «артериализация» венозной крови, обусловленная повышением содержания НЬ02 в венозной крови. Tumor Причины припухлости (лат. tumor): увеличение кровенаполнения ткани в результате развития артериальной и венозной гиперемии; увеличение лимфообразования (в связи с артериальной гиперемией); развитие отёка ткани; пролиферация в очаге воспаления. Dolor Причины боли (лат. dolor): воздействие на рецепторы медиаторов воспаления (гистамина, серотонина, кининов, некоторых Пг); высокая концентрация Н+, метаболитов (лактата, пирувата и др.); деформация ткани при скоплении в ней воспалительного экссудата. Calor Причины повышения температуры (лат. calor) в зоне воспаления: развитие артериальной гиперемии, сопровождающейся увеличением притока более тёплой крови; повышение интенсивности обмена веществ, что сочетается с увеличением высвобождения тепловой энергии; разобщение процессов окисления и фосфорилирования, обусловленное накоплением в очаге воспаления избытка ВЖК, Са2+ и других агентов. Functio laesa Причины нарушения функции (лат. functio laesa) органа или ткани: повреждающее действие флогогенного фактора; развитие в ответ на это альтеративных процессов, сосудистых реакций и экссудации; СИСТЕМНЫЕ ИЗМЕНЕНИЯ ПРИ ОСТРОМ ВОСПАЛЕНИИ Системные, общие изменения в организме представлены на рис.
Принципы терапии воспаления При разработке схемы лечения воспаления базируются на этиотропном, патогенетическом, саногенетическом и симптоматическом принципах. ЭТИОТРОПНАЯ ТЕРАПИЯ Этиотропный принцип лечения подразумевает устранение, прекращение, уменьшение силы и/или длительности действия на ткани и органы флогогенных факторов. ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ Патогенетический принцип лечения имеет целью блокирование механизма развития воспаления. При этом воздействия направлены на разрыв звеньев патогенеза воспаления, лежащих в основе главным образом процессов альтерации и экссудации. САНОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ Саногенетический принцип терапии направлен на активацию общих и местных механизмов компенсации, регенерации, защиты, восстановления и устранения повреждений и изменений в тканях и клетках, вызванных флогогенным агентом, а также последствий его влияния. Например, стимуляция иммунных и пролиферативных реакций, развитие артериальной гиперемии, фагоцитоза и др. СИМПТОМАТИЧЕСКАЯ ТЕРАПИЯ Воспаление характеризуется более или менее выраженными изменениями в различных тканях, органах и их физиологических системах. Оно, как правило, сопровождается неприятными и тягостными ощущениями, включая болевые, а также расстройствами жизнедеятельности организма в целом. В связи с этим проводится специальное лечение, направленное на предупреждение или устранение указанных симптомов (с этой целью применяют, например, болеутоляющие, анестезирующие ЛС, транквилизаторы, антистрессорные ЛС, вещества, способствующие нормализации функций органов и физиологических систем). |
|
|
|
№ 36 Представление о системе иммунобиологического надзора, её структуре, функции, роли в организме.
Биологическое значение системы иммунобиологического надзора ИБН заключается в контроле (надзоре) за индивидуальным и однородным клеточно-молекулярным составом организма. Обнаружение носителя чужеродной генетической или антигенной информации (молекулы, вирусы, клетки или их фрагменты) сопровождается его инактивацией, деструкцией и, как правило, элиминацией. При этом клетки иммунной системы способны сохранять «память» о данном агенте. Повторный контакт такого агента с клетками системы ИБН сопровождается развитием эффективного ответа, который формируется при участии как специфических — иммунных механизмов защиты, так и неспецифических факторов резистентности организма (рис.).
К числу основных в системе представлений о механизмах надзора за индивидуальным и однородным антигенном составе организма относят понятия об Аг, иммунитете, иммунной системе и системе факторов неспецифической защиты организма. Антиген — вещество экзо- или эндогенного происхождения, вызывающее развитие иммунных реакций. Виды антигенов В соответствии со структурой и происхождением Аг подразделяют на несколько видов. • В зависимости от структуры различают белковые и небелковые Аг. • В зависимости от происхождения различают экзогенные и эндогенные Аг. ИММУНИТЕТ В иммунологии термин «иммунитет» применяют в трёх значениях. • Для обозначения состояния невосприимчивости организма к воздействию носителя чужеродной генетической или антигенной информации (бактерии, вирусы, риккетсии, паразиты, грибы, клетки чужеродного трансплантата, опухолей и др.). • Для обозначения реакций системы ИБН против Аг. • Для обозначения физиологической формы иммуногенной реактивности организма, наблюдающейся при контакте клеток иммунной системы с генетически или антигенно чужеродной структурой. В результате эта структура подвергается деструкции и, как правило, элиминируется из организма. ИММУННАЯ СИСТЕМА Субстратом развития иммунного ответа являются органы, ткани и клетки, функционально объединённые в иммунную систему. Иммунная система — комплекс органов и тканей, содержащих иммунокомпетентные клетки и обеспечивающая антигенную индивидуальность и однородность организма путём обнаружения и, как правило, деструкции и элиминации из него чужеродного Аг. Иммунная система состоит из центральных и периферических органов. |
№ 37 Типовые формы нарушения иммуногенной рактивности организма: виды, общая характеристика
Расстройства механизмов ИБН за индивидуальным и однородным составом организма проявляются разнообразными иммунопатологическими состояниями и реакциями (рис.).
Иммунодефицитные состояния, патологическая толерантность, реакции «трансплантат против хозяина» являются следствием дефекта или нарушения деятельности одного или нескольких звеньев системы ИБН, обеспечивающих в норме эффективный иммунный ответ. Этиология Иммунопатологические состояния могут быть первичными или вторичными. • Причиной первичных нарушений является наследуемый или врождённый дефект генетической программы иммунокомпетентных клеток, а также клеток, обеспечивающих неспецифическую защиту организма. • Причиной вторичных нарушений являются расстройства, возникающие после рождения на разных этапах онтогенеза индивида. Они развиваются в результате повреждения клеток системы ИБН, имевших нормальную генетическую программу, под влиянием факторов различной природы: А) Физической (например, высокой дозы рентгеновского излучения или свободных радикалов). Б) Химической (в частности, цитостатических агентов или перекисных соединений). В) Биологической (например, значительного повышения уровня в крови глюкокортикоидов, повреждения клеток иммунной системы вирусами, бактериями, чужеродными клетками и AT). Патогенез Патогенез иммунопатологических состояний сложен и имеет несколько вариантов развития. Гипорегенераторный. Этот вариант патогенеза (например, иммунодефицита и патологической толерантности) заключается в торможении пролиферации стволовых гемопоэтических и/или полипотентных, а также других пролиферирующих предшественников клеток иммунной системы. В результате в организме наблюдается делеция (удаление) какого-либо клона клеток системы ИБН, а также выраженное в большей или меньшей мере уменьшение общего числа иммуноцитов и других факторов системы ИБН. Дисрегуляторный. Данный механизм нарушений иммунитета обусловлен расстройствами дифференцировки антигенпредставляющих клеток и/или Т- и/или В-лимфоцитов, а также кооперации этих клеток. Деструктивный (цитолитический). Этот вариант патогенеза состоит в массированном разрушении иммуноцитов. |
№ 38 Иммунодефицитные состояния (ИДС), связанные с нарушениями в А-субсистеме иммунитета (А-завимимые «фагоцитарные», «мононуклеарные» ИДС): причины, механизмы развития, проявления.
Иммунодефицитные состояния и иммунодефициты — типовые формы патологии системы ИБН, характеризующиеся снижением эффективности или неспособностью иммунной системы организма к осуществлению реакций деструкции и элиминации чужеродного Аг. Иммунодефициты — самостоятельные заболевания (нозологические формы) и сопутствующие синдромы, характеризующиеся недостаточностью иммунной системы.
Этиология Первичные иммунодефициты проявляются развитием инфекционных поражений организма вскоре после рождения, но могут не иметь клинических проявлений и до более позднего возраста. Причина Генные и хромосомные дефекты (многочисленные иммунодефициты разных классов). Иммунодефицитные сосотояния, связанные с нарушениями в А подсистеме: |
|
|
||
|
|
||
|
№ 39 Иммунодефицитные состояния, связанные с нарушением в системе B-лимфоцитов («B-зависимые», гуморальные ИДС): причины, механизмы развития, проявления.
Иммунодефицитные состояния и иммунодефициты — типовые формы патологии системы ИБН, характеризующиеся снижением эффективности или неспособностью иммунной системы организма к осуществлению реакций деструкции и элиминации чужеродного Аг. Иммунодефициты — самостоятельные заболевания (нозологические формы) и сопутствующие синдромы, характеризующиеся недостаточностью иммунной системы. Этиология возникновения первичных иммунодефицитов Первичные иммунодефициты проявляются развитием инфекционных поражений организма вскоре после рождения, но могут не иметь клинических проявлений и до более позднего возраста. Причина Генные и хромосомные дефекты (многочисленные иммунодефициты разных классов). Примером иммунодефицитного состояния, связанного с В-клетками является Агаммаглобулинемия (синдром Брутона)
Другим заболеванием, связанным с гуморальным иммунитетом является вариабельный общий иммунодефицит. Для него свойственны:
Так же могут возникать заболевания, связанные с избирательным дефицитом конкретного вида Ig(селективный дефицит Ig G, A, M , E, D) |
№ 40 Иммунодефицитные состояния, связанные с нарушением в системе T-лимфоцитов (T-зависимые, клеточные ИДС): причины, механизмы развития, проявления. Комбинированные ИДС.
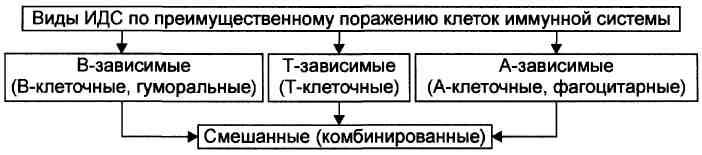
Иммунодефицитные состояния и иммунодефициты — типовые формы патологии системы ИБН, характеризующиеся снижением эффективности или неспособностью иммунной системы организма к осуществлению реакций деструкции и элиминации чужеродного Аг. Иммунодефициты — самостоятельные заболевания (нозологические формы) и сопутствующие синдромы, характеризующиеся недостаточностью иммунной системы. В зависимости от преобладания дефекта иммуноцитов того или иного класса, иммунодефициты и иммунодефицитные состояния подразделяют на В-, Т-, А-зависимые (относящиеся к антигенпредставляющим клеткам) и смешанные (рис.).
Этиология Первичные иммунодефициты проявляются развитием инфекционных поражений организма вскоре после рождения, но могут не иметь клинических проявлений и до более позднего возраста. Причина Генные и хромосомные дефекты (многочисленные иммунодефициты разных классов). Синдром ДиДжорджи – гипоплазия тимуса, сопровождается дефектом выходных отверстий сердца и гипокальциемией. Возникновение обусловлено генетическим дефектом, чаще врожденном, реже – вызванном употреблением алкоголя. Проявления:
|
№ 41 Иммунодефицитные состояния (ИДС), связанные с нарушениями в системе комплимента: причины, механизмы развития, проявления.
Иммунодефицитные состояния и иммунодефициты — типовые формы патологии системы ИБН, характеризующиеся снижением эффективности или неспособностью иммунной системы организма к осуществлению реакций деструкции и элиминации чужеродного Аг. Иммунодефициты — самостоятельные заболевания (нозологические формы) и сопутствующие синдромы, характеризующиеся недостаточностью иммунной системы. Виды. Первичные — наследуемые и врождённые (генетические) дефекты иммунной системы. Вторичные — иммунная недостаточность развивается вследствие эндо- и экзогенных воздействий на нормальную иммунную систему (например, около 90% всех вирусных инфекций сопровождается транзиторной иммунодепрес-сией). Избирательные — вызваны селективным поражением различных популяций иммунокомпетентных клеток. Неспецифические — дефект(ы) механизмов неспецифической резистентности организма (неспецифического иммунитета), фагоцитов и комплемента. Комбинированные — сочетанное поражение клеточных и гуморальных механизмов иммунитета (например, В- и Т-лимфоцитов). В зависимости от преобладания дефекта иммуноцитов того или иного класса, иммунодефициты и иммунодефицитные состояния подразделяют на В-, Т-, А-зависимые (относящиеся к антигенпредставляющим клеткам) и смешанные (рис.).
Этиология Первичные иммунодефициты проявляются развитием инфекционных поражений организма вскоре после рождения, но могут не иметь клинических проявлений и до более позднего возраста. Причина Генные и хромосомные дефекты (многочисленные иммунодефициты разных классов). Вторичные иммунодефициты, или иммунодефицитные состояния Причины иммунодефицитных состояний многообразны, к ним отнесены: 1. Иммуносупрессивные препараты (включая фенитоин [дифенин], пени-цилламин, глюкокортикоиды). 2. Недостаточность питания, полостного и мембранного пищеварения, а также кишечного всасывания. 3. Наркотики и токсические вещества. 4. Лучевые воздействия, химиопрепараты. 5. Рост злокачественных опухолей. 6. Вирусы (например, ВИЧ). 7. Состояния, приводящие к потере белка (например, нефротический синдром). 8. Гипоксия. 9. Гипотиреоз. 10. Уремия. 11. Аспления. |
|
|