
- •Лабораторная работа №1 Тема: алкилирование бензола этиленом (пропиленом) Теоретические основы алкилирования
- •Цель работы
- •Методика выполнения работы
- •Анализ продуктов реакции
- •Приготовление катализаторного комплекса
- •Методика проведения эксперимента
- •Приготовление алюмохромового оксидного катализатора
- •Методика проведения эксперимента
- •Получение хлорида водорода
- •Анализ продуктов изомеризации
- •Методика проведения опыта
- •Анализ газов пиролиза
- •Анализ жидких продуктов пиролиза
- •Методика проведение опыта
- •Цель работы
- •Методика выполнения работы Реактивы
- •Контрольные вопросы
- •Литература
- •Описание лабораторной установки
- •Методика проведения лабораторной работы
- •Методика проведения анализов процесса
- •Литература
- •Лабораторная работа №8
- •Теоретическая часть
- •Методика проведения
- •Обработка результатов
- •Порядок выполнения работы
- •Определение потенциала ионизации растворителя деасфальтизации по растворимости гудрона в нём
- •Порядок выполнения работы
- •Контрольные вопросы
- •Техника безопасности в процессе гидратации ацетилена
- •Получение, очистка и анализ ацетилена
- •Аппаратура и методика проведения опыта
- •Методика выполнения работы
- •Тема: получение фенола и ацетона из изопропилбензола
- •Окисление изопропилбензола в гидропероксид
- •Методика выполнения работы
- •Методика выполнения работы
- •Приготовление катализаторного раствора
- •Выделение палладия из отработанного катализаторного раствора
- •Порядок выполнения работы
- •Контрольные вопросы
- •Литература
Получение хлорида водорода
Хлорид водорода получают в приборе, изображенном на рисунке 3.2, который стоит из капельной воронки 2 емкостью 150 мл, колбы с боковым отводом 1 ёмкостью 700 мл, уравнительной линии 3, тройника 4, трубки с безводным хлоридом кальция 5, склянки Тищенко 6 и барботера 7.
Внимание! Обязательно надеть резиновые перчатки и защитные очки!
Для
получения хлорида водорода в колбу 1
наливают
200 мл концентрированной соляной
кислоты (d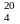 =1,198),
устанавливают на колбе воронку 2,
закрывают
кран и наливают в воронку 100 мл
концентрированной серной кислоты
(d
=1,836).
Присоединяют к воронке уравнительную
линию 3,
а
барботер 7 к
реактору
изомеризации таким образом, чтобы конец
барботера доходил до дна реактора. В
склянку Тищенко наливают концентрированную
серную кислоту до уровня на 2—3 мм выше
верхнего среза отверстия в перегородке
и только после этого осторожно приливают
серную кислоту к соляной кислоте с такой
скоростью, чтобы можно было считать
пузырьки газа, проходящие через склянку
Тищенко.
=1,198),
устанавливают на колбе воронку 2,
закрывают
кран и наливают в воронку 100 мл
концентрированной серной кислоты
(d
=1,836).
Присоединяют к воронке уравнительную
линию 3,
а
барботер 7 к
реактору
изомеризации таким образом, чтобы конец
барботера доходил до дна реактора. В
склянку Тищенко наливают концентрированную
серную кислоту до уровня на 2—3 мм выше
верхнего среза отверстия в перегородке
и только после этого осторожно приливают
серную кислоту к соляной кислоте с такой
скоростью, чтобы можно было считать
пузырьки газа, проходящие через склянку
Тищенко.
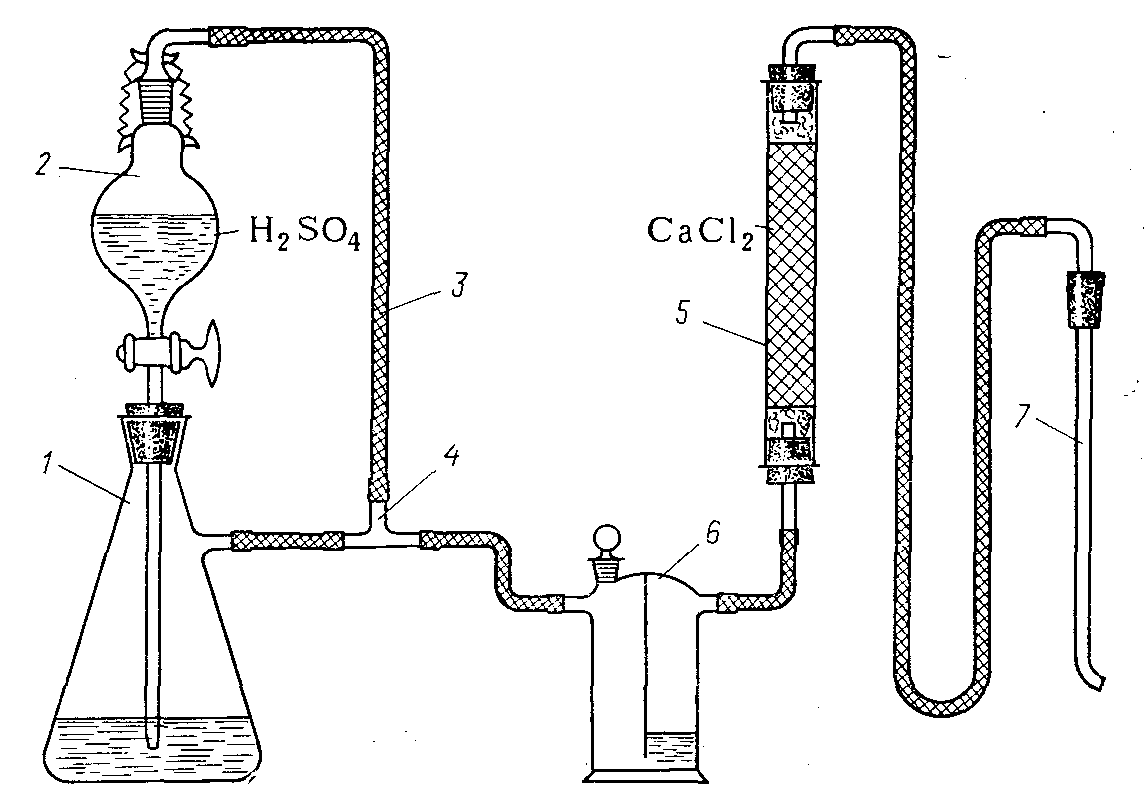
Рисунок 3.2 – Прибор для получения хлорида водорода:
1 — колба; 2 — капельная воронка; 3 — уравнительная линия; 4 — тройник; 5 — трубка с хлоридом кальция безводным; 6 — склянка Тищенко;
7 — барботер.
Анализ продуктов изомеризации
Анализ продуктов изомеризации циклогексана (метилциклопентана) проводят на хроматографе с детектором по теплопроводности.
Для количественного расчета полученных хроматограмм предварительно проводят калибровку хроматографа и строят калибровочные графики. Готовят четыре искусственные смеси метилциклопентана с циклогексаном с концентрацией метилциклопентана 5, 10, 15 и 20% (масс.). Каждую смесь роматографии-руют не менее двух раз в условиях, приведенных выше. Находят среднее значение площадей пиков (Scp, мм2) для всех смесей и строят график зависимости: площадь пика — концентрация метилциклопентана (циклогексана) в смеси. Полученный график используют для нахождения концентрации метилциклопентана (циклогексана) в продуктах реакции.
Контрольные вопросы
1. Назначение и технологические параметры процесса изомеризации.
2. Сырье установки изомеризации в промышленных условиях.
3. Реакции изомеризации на примере пентана, октана, гексадиена.
Литература
Одабашян Г.В. Лабораторный практикум по химии ТООНХС. М., Химия, 1982, с. 90-94.
Воскресенский П.И. Техника лабораторных работ. 10-е изд. М.. Химия, 1973, 717 с.
Паушкин Я.М., Вишнякова Т.П., белов П.С. Практикум по нефтехимическому синтезу. М.. Химия, 1965. 208 с.
Лабораторная работа №4
ПИРОЛИЗ УГЛЕВОДОРОДОВ
Теоретическая часть
Углеводороды подвергаются наиболее глубоким химическим превращениям в процессах пиролиза, которые проводят при температурах выше 700°С. В таких условиях углеводороды подвергаются дегидрированию и расщеплению по углерод-углеродным связям с образованием газообразных, жидких и твердых продуктов. Например, первичным продуктом расщепления н-гексадекана могут быть следующие соединения, которые, в свою очередь, подвергаются дальнейшему распаду по аналогичной схеме.
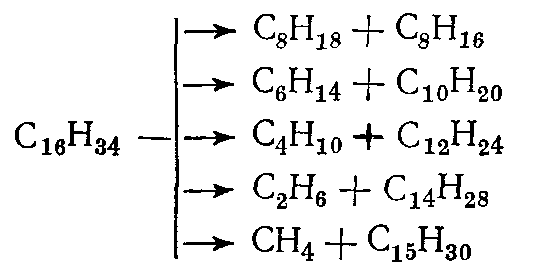
Процессы распада усиливаются с повышением температуры и времени контакта, при этом в продуктах пиролиза накапливаются вещества, более стабильные в данных условиях. При пиролизе любого углеводородного сырья в интервале 750— 850 °С целевыми веществами в газообразных продуктах реакции являются этилен, пропилен и бутилен, а в жидких — ароматические углеводороды. При дальнейшем повышении температуры пиролиза в газообразных продуктах появляется заметное количество ацетилена, усиливается выделение водорода и образование кокса, так: как выше 850 °С заметно возрастают скорости разложения углеводородов на элементы и дегидроконденсации (уплотнения) ароматических углеводородов:
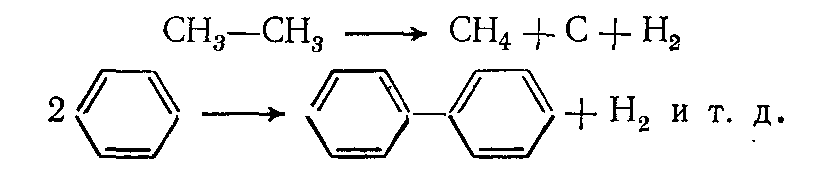
В условиях пиролиза все реакции углеводородов протекают через образование свободных радикалов, которые возникают в результате расщепления связей С — С иод воздействием высокой температуры:
![]()
Свободные радикалы, в свою очередь, инициируют радикально-цепные реакции превращения углеводородов:
![]()
![]()
Пиролиз углеводородов, как правило, проводят в присутствии паров воды, что значительно смягчает условия процесса, снижает долю вторичных реакций и препятствует образованию кокса. Расход водяного пара на пиролиз колеблется от 25 до 100% от массы исходного углеводородного сырья.
Цель работы
Изучение влияния температуры и объемной скорости подачи исходного сырья на выход и состав газообразных и жидких продуктов пиролиза углеводородов.
Реактивы
н-Октан (бензин, лигроин)
Азот (из баллона)
Хлорид кальция (безводный)
