
- •Методичні вказівки щодо виконання самостійної роботи
- •1. Пояснювальна записка
- •2 Тематичний план самостійної роботи
- •1 Поняття про географічну оболонку і її складові
- •2 Атмосфера
- •3 Літосфера
- •4 Гідросфера
- •Питання для самоконтролю
- •Біосфера
- •1 Біосфера, її структура і межі
- •2 Загальні та екологічні властивості біосфери
- •3 Техносфера
- •Питання для самоконтролю
- •Колориметр кол-1м
- •Питання для самоконтролю
- •Нефелометри
- •Питання для самоконтролю
- •Спектрофотометри
- •Питання для самоконтролю
- •Поляриметрія
- •Питання для самоконтролю
- •Спектрографи
- •Питання для самоконтролю
- •Спектрометри
- •Питання для самоконтролю
- •Кондуктометри
- •Питання для самоконтролю
- •Установки для електрогравіметричного аналізу
- •Питання для самоконтролю
- •Прилади для полярографічних вимірювань
- •Питання для самоконтролю
- •Кулонометрія
- •Питання для самоконтролю
- •Використана література Основна
- •Допоміжна
Питання для самоконтролю
У чому полягає принцип роботи кондуктометрів?
Поясніть технічні характеристики кондуктометра GМН 3430
Установки для електрогравіметричного аналізу
Схема установки для електролізу
Метод вагового електроаналізу полягає у точному вимірюванні маси речовини, що визначається або її складових частин, які виділяються в хімічно чистому стані на занурених в аналізований розчин електродах при проходженні через розчин електричного струму.
В електрогравіметричному аналізі аналізовану речовину кількісно виділяють з розчину електролізом і по масі металу, що виділився, або його оксиду розраховують вміст визначуваного елементу в пробі. Схема установки для проведення електролізу показана на рис. 2.25. Для отримання постійного струму зазвичай використовують випрямляч змінного струму або батарею акумуляторів 1. Ковзаючий контакт 2 дозволяє регулювати напругу, що подається, яку вимірюють вольтметром. Сила струму контролюється амперметром. При виділенні металів катод 5 зазвичай виготовляють з платинової сітки, анод 4 з платинової спіралі або пластинки. При виділенні оксидів знаки електродів змінюються: платинова сітка стає анодом, а спіраль - катодом. Розчин перемішується механічною або магнітною мішалкою 3.
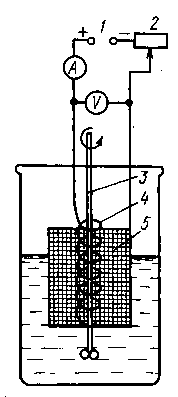
Рис. 2.25. Схема установки для проведення електролізу
Електрогравіметричний аналіз можна розглядати як один з видів гравіметричного аналізу, в якому як осаджувачі| виступають електрони. Електролітично отримувані осідання металів і оксидів є і формою осадження і гравіметричною формою.
Найважливішими вимогами до форми осадження є її мала розчинність і чистота, тобто відсутність забруднень. Ці вимоги в електрогравіметричному методі виконуються ідеально, оскільки більшість металів і вказані оксиди практично нерозчинні| у воді, а при електролітичному виділенні металів або оксидів співосадження| не відбувається або його майже завжди можна попередити шляхом вибору умов електролізу. Отриманий осад металу або оксиду зручний для промивання і зважування.
Схема ще однієї установки для електроаналізу зображено на рис. 2.26.

Рис. 2.26. Схема установки для електроаналізу:
1- джерело постійного струму; 2- амперметр; 3- вольтметр; 4-катод; 5- анод; 6-реостат;
7-запобіжник; 8-вимикач
Відома методика визначення в одному розчині методом електрогравіметричного аналізу Cu2+, Bi3+, Pb2+, Sn2+.
В нейтральному середовищі при потенціалі -0,20, -0,40 та -0,60 В почергово виділяються на катоді і зважуються мідь, вісмут, свинець, після чого розчин підкислюється для руйнування тартратного комплексу та виділяється олово.
Завдання для самоконтролю знань:
1. Вивчити і коротко законспектувати зміст питання.
2. Схематично зобразити схему установки для проведення електролізу
Рекомендована література /1.1, 2.6, 2.8/
Питання для самоконтролю
У чому полягає суть методу вагового електроаналізу?
Які елементи можна визначати електрогравіметричним методом аналізу?
Поясніть схему установки для електроаналізу
