- •Основні поняття та визначення в метрології
- •Вимірювання
- •Похибки
- •Засоби вимірювання та їх основні види
- •Похибки засобів вимірювальної техніки
- •Основні властивості засобів вимірювання та їхні метрологічні характеристики
- •Основні принципи побудови дсп
- •Класифікація виробів за дсп
- •Системи дистанційних передач сигналів вимірювальної інформації
- •Вимірювальні перетворювачі
- •Класифікація вимірювальних перетворювачів За принципом дії
- •У залежності від виду вихідного сигналу
- •Термометри розширення, механічні та манометричні
- •Термоелектричні термометри
- •М ілівольтметри потенціометри
- •Потенціометр
- •Термометри опору
- •Зрівноважені автоматичні мости та логометри
- •Прилади вимірювання тиску Види тиску
- •Дифманометри
- •Змінний і постійний перепад тиску
- •Електромагнітний витратомір
- •Переваги
- •Недоліки
- •Рівнеміри
- •Дифманометричний рівнемір
- •Буйкові та ємнісні рівнеміри
- •Контактна кондуктометрія
- •Поляризація електродів
- •Безконтактна кондуктометрія
- •Рефрактометричний метод
- •Густиноміри
- •Термокондуктометричні газоаналізатори
- •Магнітні газоаналізатори
- •Оптико-акустичний метод газового аналізу
Контактна кондуктометрія
Кондуктометричний метод контролю якості харчових продуктів
ґрунтується на вимірюванні електропровідності розчинів. Хімічний склад розчину визначається по залежності його електропровідності від концентрації та природи заряджених частинок. Питома електропровідність рідин, в залежності від концентрації і природи розчинених в ній речовин, може змінюватись на декілька порядків (від10-4 см/м- особо чисть иоди до 100 см/м (сильні електроліти)).
 Контактні
кондуктометричні аналізатори -
ґрунтуються на безпосередньому контакті
електронів з аналізуємим розчином.
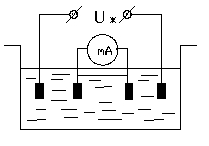
Первинний вимірювальний перетворювач
(ПВП) складається з вимірювальної мірки
, яка має два електроди площиною S
на певній відстані L один від одного і
розміщених в розчині. Опір комірки R
визначається тільки електропровідністю
розчину. Вимірювання проводять на
лінійних дільницях залежності 9.2 та за
таких умов:
Контактні
кондуктометричні аналізатори -
ґрунтуються на безпосередньому контакті
електронів з аналізуємим розчином.
Первинний вимірювальний перетворювач
(ПВП) складається з вимірювальної мірки
, яка має два електроди площиною S
на певній відстані L один від одного і
розміщених в розчині. Опір комірки R
визначається тільки електропровідністю
розчину. Вимірювання проводять на
лінійних дільницях залежності 9.2 та за
таких умов:
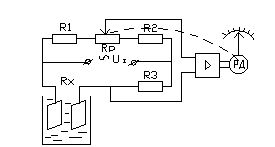
1). Використовують зрівноважений міст, який живлять напругою змінного струму, що зменшує вплив явища електролізу контрольованого середовища та поляризації електронів; 2). Електроди виготовляють із стійких малоактивних матеріалів (прототипи графіту). 3). Вимірювання проводять при малій силі струму в вимірювальному ланцюгу та підвищеній частоті напруги живлення (до 1кГц), але більшість працює на промисловій частоті 50 Гц.
На розглянутому принципі та за мостовою схемою рис. 11.2,б, випускаються кондуктометри типу КК3, КК4-Е для експрес аналізів та метрологічних провірок. Діапазон вимірювання електродних кондуктометрів до 10 См/м за температури розчину в межах 25±15 0С при класі точності 2,5
Вплив температури на електропровідність
Температура аналізованого розчину робить істотний вплив на вимірювані величини питомої електропровідності. В даний час не існує способу задовільного опису впливу температури на електропровідність. Причина такого становища справ криється в занадто великому вплив індивідуальної природи розчинених речовин на температурний коефіцієнт. З упевненістю можна сказати тільки одне: при підвищенні температури на один градус питома електропровідність розчину в середньому збільшується на 1-2,5%.
Для слабкоконцентрованих розчинів прослідковується лінійна залежність їх електропровід-ності від температури при значеннях αt = 0,01 ÷0,025 і βt = 0. Контактні методи змінного струму високої частоти кондуктометрії дають можливість вимірювати електропровідність розчинів з високою точністю, однак похибки все ж залишаються за рахунок теплових і поляризаційних процесів при протіканні електричного струму через електролітичні комірки ЕК. Поляризаційні явища при вимірюваннях опору ЕК з використанням змінного струму проявляються значно слабше ніж при постійному струмі і залежать від частоти струму, концентрації розчинів і конструктивних особливостей електродів ЕК.
Поляризація електродів
Поляризація, зумовлена виникненням гальванічного елемента, називається хімічною. Це приводить до того, що деяка кількість водню і кисню адсорбується на електродах, унаслідок чого утворюється гальванічний елемент ЕРС якого напрямлена протилежно прикладеній. Існують різні способи зменшення поляризації електродів, але звести її до нуля неможливо. Наприклад, енергійним перемішуванням розчину можна значно послабити концентраційну поляризацію. Хімічну поляризацію зменшують додаванням речовин, які називаються деполяризаторами. Деполяризаторами можуть бути окисники (катодне виділення водню) і відновники (у випадку анодного виділення кисню).
При використовуванні кондуктометрів з концентратоміри в швидкокристалізуємих забруднених середовищах, наприклад, в цукровому виробництві на ділянках І і ІІ-ї сатурації, застосовують і 4-електродій ПВП для зменшення впливу поляризації струмових електродів і впливу електричного опору залишків на електродах. В цих ПВП функції між електродами розділені і крайні використовуються для підведення живлення, з середніх – знімають напругу, яка пропорційна електричному опору аналізуємого розчину.