
- •1.Биохимия, её задачи. Значение биохимия для медицины.
- •Задачи биохимии:
- •Значение биохимии для медицины.
- •2.Аминокислоты, их классификация. Строение и биологическая роль аминокислот.
- •Строение:
- •Функции аминокислот:
- •3.Строение белков. Уровни структурной организации белка. Характеристика связей, стабилизирующих их. Доменные белки.
- •Структурная организация белков.
- •4.Электро-химические свойства белков как основа методов их исследования. Электрофорез белков крови.
- •5.Коллоидные свойства белков. Гидратация. Растворимость. Денатурация, роль шаперонов.
- •Гидратация
- •Растворимость
- •6. Принципы классификации белков. Простые и сложные белки. Характеристика простых белков: гистоны, протамины, альбумины, глобулины.
- •Простые белки.
- •7.Современные представления о структуре и функциях нуклеиновых кислот. Первичная и вторичная структуры днк. Строение мономеров нуклеиновых кислот. Нуклеопротеины. Методы исследования днк (пцр).
- •Первичная структура днк.
- •Вторичная структура днк.
- •Нуклеопротеины
- •Полимеразная цепная реакция.
- •8. Хромопротеины. Строение и функции гемоглобина. Типы гемоглобина. Миоглобин.
- •Гемоглобин.
- •9. Липид-белковые комплексы. Строение липидных компонентов. Структурные протеолипиды и липопротеины, их функции.
- •Свободные липопротеины
- •Структурные протеолипиды
- •10. Ферменты, их химическая природа, структурная организация. Активный центр ферментов, его свойства.
- •Строение ферментов.
- •11. Коферменты и их функции в ферментативных реакциях. Витаминные коферменты. Примеры реакций с участием витаминных коферментов. Тиаминовые коферменты, тдф.
- •Тиаминовые коферменты, тдф.
- •12. Никотинамидные коферменты. Структура над, надф. Примеры реакций.
- •13. Флавиновые коферменты. Структура фмн,фад. Примеры реакций.
- •14. Пиридоксиновые коферменты. Строение пф, примеры реакций.
- •15. Роль фолиевой кислоты и в12 в реакциях трансметилирования, s-аденозилметионин, его образование. Пример реакции с цчастием фолиевой кислоты и в12.
- •16. Свойства ферментов. Лабильность конформации, влияние температуры и pH среды. Специфичность действия ферментов, примеры реакций.
- •17. Номенклатура и классификация ферментов. Характеристика класса оксидоредуктаз, примеры реакций.
- •6 Классов:
- •18. Характеристика класса трансфераз и гидролаз. Примеры реакций.
- •19.Лиазы, изомеразы, лигазы. Характеристика, примеры реакций с участием ферментов этих классов.
- •20. Современные представления о механизме действия ферментов. Стадии ферментативного катализа, молекулярные эффекты, примеры.
- •21. Ингибирование ферментов. Конкурентное и неконкурентное ингибирование, примеры реакций. Лекарственные вещества, как ингибиторы ферментов.
- •22. Понятие об изоферментах. Характеристика изоферментов Лактатдегидрогеназы (лдг) и креатинкиназы (кк). Использование ферментов в медицине. Энзимодиагностика, энзимотерапия. Энзимопатология, примеры.
- •23. Обмен веществ и энергии. Этапы обмена веществ. Общий путь катаболизма. Окислительное декарбоксилирование пирувата.
- •Окислительное декарбоксилирование пвк
- •24. Цитратный цикл, химизм процесса, его биологическое значение.
- •25.Сопряжение реакций цикла цтк с дыхательной цепью ферментов.
- •По укороченной цепи фад→ фадн2
- •26. Современные представления о биологическом окислении. Первичные акцепторы водорода. Электронно-транспортная цепь.
- •Первичные акцепторы протонов и электроногв.
- •Электронно-транспортная цепь
- •27.Характеристика компонентов электрон-транспортной цепи
- •28. Пути синтеза атф. Субстратное фосфорилирование (пример). Молекулярные механизмы окислительного фосфорилирования (теория Митчелла). Разобщение окисления и фосфорилирования.
- •Механизм окислительного фосфорилирования
- •29. Альтернативные пути биологического окисления, оксигеназный путь. Микросомальные монооксигеназы.
- •30. Свободнорадикальное окисления. Токсичность кислорода. Активный формы кислорода. Антиокислительная защита. Роль сро в патологии.
- •31. Белки: роль, потребность, биологическая ценность. Строение незаменимых ак. Превращение белков в желудке, роль соляной кислоты. Действие пептид гидролаз. Анализ желудочного содержимого.
- •Переваривание белков
- •32.Превращение белков в желудке. Роль соляной кислоты в переваривании белков. Показать действие пепсина на конкретном примере.
- •33. Переваривание белков в кишечнике.
- •34. Гниение белков и аминокислот в кишечнике. Пути образования продуктов гниения. Примеры.
- •1.Декабоксилирование
- •35. Механизм обезвреживания продуктов гниения белков. Роль фафс и удф-гк.
- •36. Трансаминирование и декарбоксилирование аминокислот.
- •37. Декарбоксилирование аминокислот, образование биогенных аминов. Роль в этом процессе пф.
- •38. Реакции дезаминирования аминокислот.
- •1. Неокислительное
- •2. Внутримолекулярное:
- •39.Оринтиновый цикл.
- •40. Особенности катаболизма пуриновых нуклеотидов. Их строение и распад. Образование мочевой кислоты. Подагра.
- •41. Генетический код и его свойства.
- •Свойства:
- •42. Механизмы репликации днк. Условия необходимые для репликации. Основные этапы репликации.
- •Основы для репликации:
- •Условия репликации:
- •Этапы репликации:
- •43. Биосинтез рнк (транскрипция). Условия и этапы транскрипции.
- •Условия транскрипции:
- •Этапы Транскрипции:
- •44. Процессинг рнк. Альтернативный сплайсинг.
- •45.Биосинтез белка. Белково-синтетический ферментативный комплекс.
- •Белковые факторы:
- •46. Этапы трансляции и их характеристика.
- •47. Посттрансляционный процессинг. Виды химической модификации, фолдинг, роль шаперонов.
- •48. Строение оперона. Регуляция биосинтеза белка у прокариотов. Функционирование лактозного и гистидинового оперонов.
- •Регуляция оперона по методу индукции.
- •Регуляция оперона по методу репрессии
- •49. Особенности и уровни регуляции биосинтеза белка у эукариотов. Амплификация генов, энхансерные и сайленсерные элементы.
- •1. На уровне генов:
- •6. Регуляция на уровне трансляции:
- •50. Современные представления о структурно-функциональной организации днк. Основные направления молекулярной биологии: геномика, транскриптомика, рн-омика, протеомика.
- •51. Ингибиторы белковых синтезов. Действие антибиотиков и токсинов. Биологическая роль теломер и теломераз.
- •Токсины
- •Теломеры и теломеразы. Их роль в развитии опухолевого роста.
- •52. Виды молекулярных мутаций и их биологические последствия.
- •1. Замена:
- •2. Вставка:
- •53. Биохимический полиморфизм и его биологическая роль. Непереносимость пищевых веществ и лекарств.
- •54. Основные углеводы, их строение и классификация, биологическая роль.
- •Гомополисахариды
- •Гетерополисахариды
- •55. Роль углеводов в питании. Переваривание и всасывание углеводов в органах пищеварительной системы. Написать реакции.
- •56. Катаболизм глюкозы в анаэробных условиях. Химизм процесса, биологическая роль.
- •57. Катаболизм глюкозы в тканях в аэробных условиях. Гексозодифосфатный путь превращения глюкозы и его биологическая роль. Эффект Пастера.
- •1. Этапы аэробного гликолиза
- •Эффект Пастера
- •58. Гексозомонофосфатный путь превращения глюкозы в тканях и его биологическая роль. Химизм реакций окислительной стадии.
- •1. Транскетолазные реакции:
- •2. Трансальдолазная реакция:
- •59. Биосинтез и распад гликогена в тканях. Биологическая роль этих процессов
- •Распад гликогена
- •1. Основной фосфоролитический путь
- •2.Неосновной амилолитический.
- •60. Глюконеогенез. Возможные предшественники, последовательность реакций, биологическая роль.
- •61.Характеристика основных липидов организма человека, их строение, классификация, суточная потребность и биологическая роль.
- •62. Эйкозаноиды - регуляторы обмена веществ; химическая природа, биологические эффекты эйкозаноидов.
- •1.Простагландины:
- •63.Биологическая роль липидов пищи. Переваривание, всасывание липидов в органах пищеварительной системы. Жёлчные кислоты. Их строение, биологическая роль
- •64. Характеристика липопротеинов крови, их биологическая роль.
- •65.Окисление высших жирных кислот в тканях. Химизм реакций, биологическая роль
- •66.Окисление глицерола. Химизм реакций, биологическая роль.
- •67. Биосинтез высших жирных кислот в тканях. Химизм реакций, биологическая роль.
- •68.Холестерол. Его химическое строение, биосинтез и биологическая роль.
- •69. Образование кетоновых тел в тканях. Биологическое значение кетоновых тел. Кетоацидоз.
- •70. Сигнальные молекулы, их классификация. Виды регуляторных эффектов сигнальных молекул. Понятие о клетке мишени.
- •Задачи:
- •Особенности сигнальных молекул:
- •Виды регуляторных эффектов:
- •Классификация сигнальных молекул:
- •Общие этапы действия сигнальных молекул:
- •72. Механизм действия липофильных сигнальных молекул. Механизм действия nо. Действие сигнальных молекул через тирозинкиназные рецепторы.
- •73. Гормоны и их отличительные признаки. Классификация гормонов. Роль гипоталамуса в гормональной регуляции.
- •Классификация гормонов и бав по химической структуре:
- •Функциональная классификация гормонов:
- •Общие свойства гормонов:
- •Гипоталамус
- •Либерины
- •Статины
- •74. Гормоны передней доли гипофиза, классификация, их химическая природа. Гормоны - простые белки, участие в регуляции метаболизма. Гормон роста.
- •75. Гормоны передней доли гипофиза – гликопротеины, их характеристика, участие в регуляции метаболизма (ттг,фсг,лг).
- •76. Семейство пептидов проопиомеланокортина. Гормоны задней доли гипофиза, место их образования, химическая природа, влияние на функции органов-мишеней.
- •Гормоны задней доли гипофиза:
- •77. Тиреоидные гормоны: синтез, строение, транспорт и механизм действия на метаболические процессы.
- •78. Тиреокальцитонин, паратиреоидный гормон. Химическая природа, участие в регуляции обмена веществ.
- •79. Инсулин, схема строения, участие в регуляции метаболических процессов. Специфика в действии на рецепторы органов мишеней.
- •80. Глюкагон: химическая природа и механизм действия. Влияние на обмен веществ. Соматостатин.
- •Соматостатин
- •81. Участие адреналина в регуляции обмена веществ. Структура, механизм гормонального действия, метаболические эффекты.
- •82. Кортикостероидные гормоны. Структура кортизола, механизм действия. Участие гормонов коры надпочечников в обмене веществ.
- •Кортикостероиды.
- •1. Глюкокортикоиды (кортикостерон, кортизол, кортизон).
- •2. Минералокортикоиды (альдостерон).
- •Механизм действия.
- •1. Глюкокортикоиды:
- •2. Минералокортикоиды:
- •83.Гормоны половых желез: эстрадиол, прогестерон и тестостерон, их строение, механизм действия и биологическая роль.
- •Эстрадиол
- •Механзм действия эстрогена:
- •Прогестерон
- •Механизм действия
- •Тестостерон
- •84. Межклеточный матрикс, его компоненты, функции. Характеристика коллагена, строение тропоколлагена. Полиморфизм коллагеновых белков.
- •Тропоколлаген:
- •Полиморфизм коллагеновых белков:
- •85. Этапы синтеза и созревания коллагена. Роль ферментов и витамина с в этом процессе. Катаболизм коллагена
- •Роль ферментов и витамина с.
- •Катаболизм коллагена
- •86. Особенности строения и функции эластина. Неколлагеновые структурные белки: фибронектин и ламинин.
- •Фибронектин
- •Ламинин
- •87.Протеогликаны межклеточного матрикса, их строение, функции. Образование надмолекулярных комплексов.
- •Малые протеогликаны
65.Окисление высших жирных кислот в тканях. Химизм реакций, биологическая роль
Окисление ВЖК в тканях изучалось Ф. КНООПОМ (1904г.), который назвал окисление ВЖК бета-окислением. Он показал, что процесс этот циклический, что все ВЖК, имеющие чётное количество углеродных звеньев в цепи обязательно проходят окисление, когда цепь периодически укорачивается на 2 углеродных звена.
β-Окисление - специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно отделяется по 2 атома углерода в виде ацетил-КоА. Метаболический путь - β-окисление - назван так потому, что реакции окисления жирной кислоты происходят у β-углеродного атома. Реакции β-окисления и последующего окисления ацетил-КоА в ЦТК служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования. β-Окисление жирных кислот происходит только в аэробных условиях.
Перед тем, как вступить в различные реакции, жирные кислоты должны быть активированы, т.е. связаны макроэргической связью с коферментом А:
RCOOH + HSKoA + АТФ → RCO ~ КоА + АМФ + PPi.
Реакцию катализирует фермент ацил-КоА синтетаза. Выделившийся в ходе реакции пирофосфат гидролизуется ферментом пирофосфатазой: Н4Р2О7 + Н2О → 2 Н3РО4.
β-Окисление жирных кислот, происходит в матриксе митохондрий, поэтому после активации жирные кислоты должны транспортироваться внутрь митохондрий. Жирные кислоты с короткой и средней длиной цепи (от 4 до 12 атомов углерода) могут проникать в матрикс митохондрий путём диффузии. Активация этих жирных кислот происходит в матриксе митохондрий. Жирные кислоты с длинной углеводородной цепью переносятся через плотную внутреннюю мембрану митохондрий с помощью карнитина. Карнитин поступает с пищей или синтезируется из незаменимых аминокислот лизина и метионина. В реакциях синтеза карнитина участвует витамин С.
В наружной мембране митохондрий находится фермент карнитинацилтрансфераза I (карнитин-пальмитоилтрансфераза I), катализирующий реакцию с образованием ацилкарнитина.
Образовавшийся ацилкарнитин проходит через межмембранное пространство к наружной стороне внутренней мембраны и транспортируется с помощью карнитинацилкарнитинтранс-локазы на внутреннюю поверхность внутренней мембраны митохондрий, где фермент карнитинацилтрансфераза II катализирует перенос ацила на внутримитохондриальный КоА. Таким образом, ацил-КоА становится доступным для ферментов β-окисления. Свободный карнитин возвращается на цитозольную сторону внутренней мембраны митохондрий той же транслоказой.
На внутренней поверхности внутренней мембраны находится фермент карнитинацил трансфераза II, катализирующий обратный перенос ацила с карнитина на внутримитохондриальный КоА. После этого ацил-КоА включается в реакции β-окисления.
![]()
β-Окисление жирных кислот - специфический путь катаболизма жирных кислот, протекающий в матриксе митохондрий только в аэробных условиях и заканчивающийся образованием ацетил-КоА. Водород из реакций β-окисления поступает в ЦПЭ, а ацетил-КоА окисляется в цитратном цикле, также поставляющем водород для ЦПЭ. Поэтому β-окисление жирных кислот - важнейший метаболический путь, обеспечивающий синтез АТФ в дыхательной цепи.
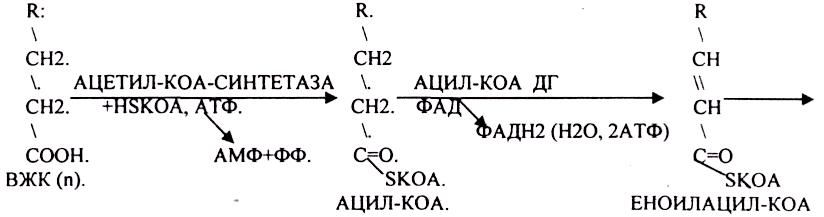
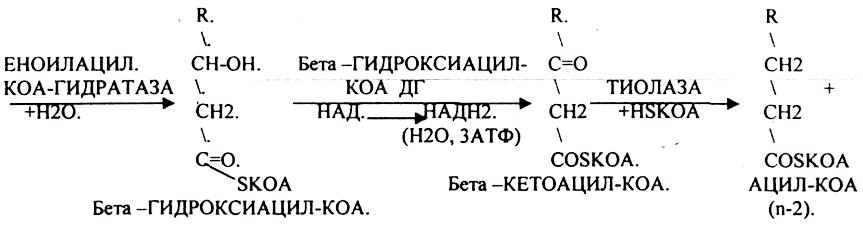
β-Окисление начинается с дегидрирования ацил-КоА FAD-зависимой ацил-КоА дегидрогеназой с образованием двойной связи между α- и β-атомами углерода в продукте реакции - еноил-КоА. Восстановленный в этой реакции кофермент FADH2 передаёт атомы водорода в ЦПЭ на кофермент Q. В результате синтезируются 2 молекулы АТФ. В следующей реакции р-окисления по месту двойной связи присоединяется молекула воды таким образом, что ОН-группа находится у β-углеродного атома ацила, образуя β-гидроксиацил-КоА. Затем β-гидроксиацил-КоА окисляется NАD+-зависимой дегидрогеназой. Восстановленный NADH, окисляясь в ЦПЭ, обеспечивает энергией синтез 3 молекул АТФ. Образовавшийся β-кетоацил-КоА подвергается тиолитическому расщеплению ферментом тиолазой, так как по месту разрыва связи С-С через атом серы присоединяется молекула кофермента А. В результате этой последовательности из 4 реакций от ацил-КоА отделяется двухуглеродный остаток - ацетил-КоА. Жирная кислота, укороченная на 2 атома углерода, опять проходит реакции дегидрирования, гидратации, дегидрирования, отщепления ацетил-КоА. Эту последовательность реакций обычно называют "циклом β-окисления", имея в виду, что одни и те же реакции повторяются с радикалом жирной кислоты до тех пор, пока вся кислота не превратится в ацетильные остатки.
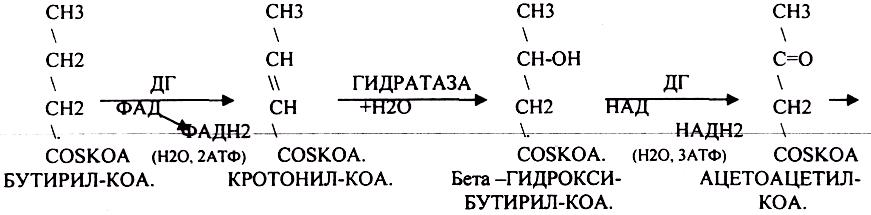
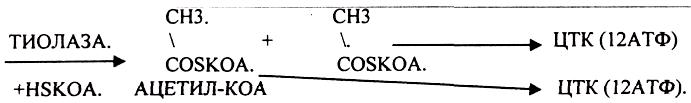
Продуктами каждого цикла β-окисления являются FADH2, NADH и ацетил-КоА. Хотя реакции в каждом "цикле" одни и те же, остаток кислоты, который входит в каждый последующий цикл, короче на 2 углеродных атома. В последнем цикле окисляется жирная кислота из 4 атомов углерода, поэтому образуются 2 молекулы ацетил-КоА, а не 1, как в предыдущих.
Энергетический эффект окисления ВЖК: АТФ = n/2 * 17 - 6, где n - число углеродных звеньев в цепи ВЖК, 17 - количество молекул АТФ, которые выделяются в результате окисления 2 углеродных звеньев цепи до конечных продуктов 5АТФ+12АТФ, 6 - то количество АТФ, которое не выделяется, поскольку 1 АТФ тратится на активацию ВЖК, а 5 АТФ не выделяются на последнем этапе - превращения молочной кислоты.
Около половины жирных кислот в организме человека ненасыщенные. β-Окисление этих кислот идёт обычным путём до тех пор, пока двойная связь не окажется между третьим и четвёртым атомами углерода. Затем фермент еноил-КоА изомераза перемещает двойную связь из положения 3-4 в положение 2-3 и изменяет цис-конформацию двойной связи на транс-, которая требуется для р-окисления. В этом цикле Р-окисления первая реакция дегидрирования не происходит, так как двойная связь в радикале жирной кислоты уже имеется. Далее циклы β-окисления продолжаются, не отличаясь от обычного пути.
α-Окисление жирных кислот. В липидах мозга и других отделах нервной ткани преобладают жирные кислоты с очень длинной цепью - более 20 углеродных атомов. Они окисляются по типу α-окисления, при котором от жирной кислоты отщепляется по одному атому углерода, выделяющемуся в виде СО2.
Этот путь катаболизма жирных кислот не связан с синтезом АТФ.
ВЖК, имеющие нечётное количество углеродных звеньев, поступают в организм человека в составе пищи. Окисление таких ВЖК происходит также как и ВЖК, имеющих чётное количество углеродных звеньев в цепи, но только до последней стадии - стадии превращения ПРОПИОНИЛ-КОА. которая имеет свои особенности:
Т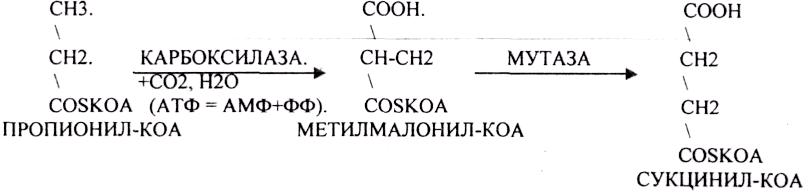 .о.
образованная молекула сукцинил-КОА,
которая для дальнейшего окисления в
митохондриях поступает в ЦТК, одним из
основных субстратов которого она
является.
.о.
образованная молекула сукцинил-КОА,
которая для дальнейшего окисления в
митохондриях поступает в ЦТК, одним из
основных субстратов которого она
является.
