
- •1.Биохимия, её задачи. Значение биохимия для медицины.
- •Задачи биохимии:
- •Значение биохимии для медицины.
- •2.Аминокислоты, их классификация. Строение и биологическая роль аминокислот.
- •Строение:
- •Функции аминокислот:
- •3.Строение белков. Уровни структурной организации белка. Характеристика связей, стабилизирующих их. Доменные белки.
- •Структурная организация белков.
- •4.Электро-химические свойства белков как основа методов их исследования. Электрофорез белков крови.
- •5.Коллоидные свойства белков. Гидратация. Растворимость. Денатурация, роль шаперонов.
- •Гидратация
- •Растворимость
- •6. Принципы классификации белков. Простые и сложные белки. Характеристика простых белков: гистоны, протамины, альбумины, глобулины.
- •Простые белки.
- •7.Современные представления о структуре и функциях нуклеиновых кислот. Первичная и вторичная структуры днк. Строение мономеров нуклеиновых кислот. Нуклеопротеины. Методы исследования днк (пцр).
- •Первичная структура днк.
- •Вторичная структура днк.
- •Нуклеопротеины
- •Полимеразная цепная реакция.
- •8. Хромопротеины. Строение и функции гемоглобина. Типы гемоглобина. Миоглобин.
- •Гемоглобин.
- •9. Липид-белковые комплексы. Строение липидных компонентов. Структурные протеолипиды и липопротеины, их функции.
- •Свободные липопротеины
- •Структурные протеолипиды
- •10. Ферменты, их химическая природа, структурная организация. Активный центр ферментов, его свойства.
- •Строение ферментов.
- •11. Коферменты и их функции в ферментативных реакциях. Витаминные коферменты. Примеры реакций с участием витаминных коферментов. Тиаминовые коферменты, тдф.
- •Тиаминовые коферменты, тдф.
- •12. Никотинамидные коферменты. Структура над, надф. Примеры реакций.
- •13. Флавиновые коферменты. Структура фмн,фад. Примеры реакций.
- •14. Пиридоксиновые коферменты. Строение пф, примеры реакций.
- •15. Роль фолиевой кислоты и в12 в реакциях трансметилирования, s-аденозилметионин, его образование. Пример реакции с цчастием фолиевой кислоты и в12.
- •16. Свойства ферментов. Лабильность конформации, влияние температуры и pH среды. Специфичность действия ферментов, примеры реакций.
- •17. Номенклатура и классификация ферментов. Характеристика класса оксидоредуктаз, примеры реакций.
- •6 Классов:
- •18. Характеристика класса трансфераз и гидролаз. Примеры реакций.
- •19.Лиазы, изомеразы, лигазы. Характеристика, примеры реакций с участием ферментов этих классов.
- •20. Современные представления о механизме действия ферментов. Стадии ферментативного катализа, молекулярные эффекты, примеры.
- •21. Ингибирование ферментов. Конкурентное и неконкурентное ингибирование, примеры реакций. Лекарственные вещества, как ингибиторы ферментов.
- •22. Понятие об изоферментах. Характеристика изоферментов Лактатдегидрогеназы (лдг) и креатинкиназы (кк). Использование ферментов в медицине. Энзимодиагностика, энзимотерапия. Энзимопатология, примеры.
- •23. Обмен веществ и энергии. Этапы обмена веществ. Общий путь катаболизма. Окислительное декарбоксилирование пирувата.
- •Окислительное декарбоксилирование пвк
- •24. Цитратный цикл, химизм процесса, его биологическое значение.
- •25.Сопряжение реакций цикла цтк с дыхательной цепью ферментов.
- •По укороченной цепи фад→ фадн2
- •26. Современные представления о биологическом окислении. Первичные акцепторы водорода. Электронно-транспортная цепь.
- •Первичные акцепторы протонов и электроногв.
- •Электронно-транспортная цепь
- •27.Характеристика компонентов электрон-транспортной цепи
- •28. Пути синтеза атф. Субстратное фосфорилирование (пример). Молекулярные механизмы окислительного фосфорилирования (теория Митчелла). Разобщение окисления и фосфорилирования.
- •Механизм окислительного фосфорилирования
- •29. Альтернативные пути биологического окисления, оксигеназный путь. Микросомальные монооксигеназы.
- •30. Свободнорадикальное окисления. Токсичность кислорода. Активный формы кислорода. Антиокислительная защита. Роль сро в патологии.
- •31. Белки: роль, потребность, биологическая ценность. Строение незаменимых ак. Превращение белков в желудке, роль соляной кислоты. Действие пептид гидролаз. Анализ желудочного содержимого.
- •Переваривание белков
- •32.Превращение белков в желудке. Роль соляной кислоты в переваривании белков. Показать действие пепсина на конкретном примере.
- •33. Переваривание белков в кишечнике.
- •34. Гниение белков и аминокислот в кишечнике. Пути образования продуктов гниения. Примеры.
- •1.Декабоксилирование
- •35. Механизм обезвреживания продуктов гниения белков. Роль фафс и удф-гк.
- •36. Трансаминирование и декарбоксилирование аминокислот.
- •37. Декарбоксилирование аминокислот, образование биогенных аминов. Роль в этом процессе пф.
- •38. Реакции дезаминирования аминокислот.
- •1. Неокислительное
- •2. Внутримолекулярное:
- •39.Оринтиновый цикл.
- •40. Особенности катаболизма пуриновых нуклеотидов. Их строение и распад. Образование мочевой кислоты. Подагра.
- •41. Генетический код и его свойства.
- •Свойства:
- •42. Механизмы репликации днк. Условия необходимые для репликации. Основные этапы репликации.
- •Основы для репликации:
- •Условия репликации:
- •Этапы репликации:
- •43. Биосинтез рнк (транскрипция). Условия и этапы транскрипции.
- •Условия транскрипции:
- •Этапы Транскрипции:
- •44. Процессинг рнк. Альтернативный сплайсинг.
- •45.Биосинтез белка. Белково-синтетический ферментативный комплекс.
- •Белковые факторы:
- •46. Этапы трансляции и их характеристика.
- •47. Посттрансляционный процессинг. Виды химической модификации, фолдинг, роль шаперонов.
- •48. Строение оперона. Регуляция биосинтеза белка у прокариотов. Функционирование лактозного и гистидинового оперонов.
- •Регуляция оперона по методу индукции.
- •Регуляция оперона по методу репрессии
- •49. Особенности и уровни регуляции биосинтеза белка у эукариотов. Амплификация генов, энхансерные и сайленсерные элементы.
- •1. На уровне генов:
- •6. Регуляция на уровне трансляции:
- •50. Современные представления о структурно-функциональной организации днк. Основные направления молекулярной биологии: геномика, транскриптомика, рн-омика, протеомика.
- •51. Ингибиторы белковых синтезов. Действие антибиотиков и токсинов. Биологическая роль теломер и теломераз.
- •Токсины
- •Теломеры и теломеразы. Их роль в развитии опухолевого роста.
- •52. Виды молекулярных мутаций и их биологические последствия.
- •1. Замена:
- •2. Вставка:
- •53. Биохимический полиморфизм и его биологическая роль. Непереносимость пищевых веществ и лекарств.
- •54. Основные углеводы, их строение и классификация, биологическая роль.
- •Гомополисахариды
- •Гетерополисахариды
- •55. Роль углеводов в питании. Переваривание и всасывание углеводов в органах пищеварительной системы. Написать реакции.
- •56. Катаболизм глюкозы в анаэробных условиях. Химизм процесса, биологическая роль.
- •57. Катаболизм глюкозы в тканях в аэробных условиях. Гексозодифосфатный путь превращения глюкозы и его биологическая роль. Эффект Пастера.
- •1. Этапы аэробного гликолиза
- •Эффект Пастера
- •58. Гексозомонофосфатный путь превращения глюкозы в тканях и его биологическая роль. Химизм реакций окислительной стадии.
- •1. Транскетолазные реакции:
- •2. Трансальдолазная реакция:
- •59. Биосинтез и распад гликогена в тканях. Биологическая роль этих процессов
- •Распад гликогена
- •1. Основной фосфоролитический путь
- •2.Неосновной амилолитический.
- •60. Глюконеогенез. Возможные предшественники, последовательность реакций, биологическая роль.
- •61.Характеристика основных липидов организма человека, их строение, классификация, суточная потребность и биологическая роль.
- •62. Эйкозаноиды - регуляторы обмена веществ; химическая природа, биологические эффекты эйкозаноидов.
- •1.Простагландины:
- •63.Биологическая роль липидов пищи. Переваривание, всасывание липидов в органах пищеварительной системы. Жёлчные кислоты. Их строение, биологическая роль
- •64. Характеристика липопротеинов крови, их биологическая роль.
- •65.Окисление высших жирных кислот в тканях. Химизм реакций, биологическая роль
- •66.Окисление глицерола. Химизм реакций, биологическая роль.
- •67. Биосинтез высших жирных кислот в тканях. Химизм реакций, биологическая роль.
- •68.Холестерол. Его химическое строение, биосинтез и биологическая роль.
- •69. Образование кетоновых тел в тканях. Биологическое значение кетоновых тел. Кетоацидоз.
- •70. Сигнальные молекулы, их классификация. Виды регуляторных эффектов сигнальных молекул. Понятие о клетке мишени.
- •Задачи:
- •Особенности сигнальных молекул:
- •Виды регуляторных эффектов:
- •Классификация сигнальных молекул:
- •Общие этапы действия сигнальных молекул:
- •72. Механизм действия липофильных сигнальных молекул. Механизм действия nо. Действие сигнальных молекул через тирозинкиназные рецепторы.
- •73. Гормоны и их отличительные признаки. Классификация гормонов. Роль гипоталамуса в гормональной регуляции.
- •Классификация гормонов и бав по химической структуре:
- •Функциональная классификация гормонов:
- •Общие свойства гормонов:
- •Гипоталамус
- •Либерины
- •Статины
- •74. Гормоны передней доли гипофиза, классификация, их химическая природа. Гормоны - простые белки, участие в регуляции метаболизма. Гормон роста.
- •75. Гормоны передней доли гипофиза – гликопротеины, их характеристика, участие в регуляции метаболизма (ттг,фсг,лг).
- •76. Семейство пептидов проопиомеланокортина. Гормоны задней доли гипофиза, место их образования, химическая природа, влияние на функции органов-мишеней.
- •Гормоны задней доли гипофиза:
- •77. Тиреоидные гормоны: синтез, строение, транспорт и механизм действия на метаболические процессы.
- •78. Тиреокальцитонин, паратиреоидный гормон. Химическая природа, участие в регуляции обмена веществ.
- •79. Инсулин, схема строения, участие в регуляции метаболических процессов. Специфика в действии на рецепторы органов мишеней.
- •80. Глюкагон: химическая природа и механизм действия. Влияние на обмен веществ. Соматостатин.
- •Соматостатин
- •81. Участие адреналина в регуляции обмена веществ. Структура, механизм гормонального действия, метаболические эффекты.
- •82. Кортикостероидные гормоны. Структура кортизола, механизм действия. Участие гормонов коры надпочечников в обмене веществ.
- •Кортикостероиды.
- •1. Глюкокортикоиды (кортикостерон, кортизол, кортизон).
- •2. Минералокортикоиды (альдостерон).
- •Механизм действия.
- •1. Глюкокортикоиды:
- •2. Минералокортикоиды:
- •83.Гормоны половых желез: эстрадиол, прогестерон и тестостерон, их строение, механизм действия и биологическая роль.
- •Эстрадиол
- •Механзм действия эстрогена:
- •Прогестерон
- •Механизм действия
- •Тестостерон
- •84. Межклеточный матрикс, его компоненты, функции. Характеристика коллагена, строение тропоколлагена. Полиморфизм коллагеновых белков.
- •Тропоколлаген:
- •Полиморфизм коллагеновых белков:
- •85. Этапы синтеза и созревания коллагена. Роль ферментов и витамина с в этом процессе. Катаболизм коллагена
- •Роль ферментов и витамина с.
- •Катаболизм коллагена
- •86. Особенности строения и функции эластина. Неколлагеновые структурные белки: фибронектин и ламинин.
- •Фибронектин
- •Ламинин
- •87.Протеогликаны межклеточного матрикса, их строение, функции. Образование надмолекулярных комплексов.
- •Малые протеогликаны
3.Строение белков. Уровни структурной организации белка. Характеристика связей, стабилизирующих их. Доменные белки.
Белки - это высокомолекулярные азотсодержащие органические вещества, состоящие из АК ( от 20), соединённых пептидными связями в полипептидную цепь, и имеющие сложную структурную организацию. Совокупность белков организма определяет его фенотипические особенности.
Характерные признаки белков, отличающие их от других соединений:
1 .Белки - АЗОТСОДЕРЖАЩИЕ вещества (до 16 %).
2.Структурной единицей белков являются альфа АК L-РЯДА.
![]()
3-.АК связываются ПЕПТИДНЫМИ связями в ПОЛИПЕПТИДНУЮ цепь.
4.Большая молекулярная масса белков (от 20000 до нескольких миллионов дальтон).
5.Сложная структурная организация.
ФУНКЦИИ БЕЛКОВ.
1.Каталитическая. Многие белки являются ферментами
2.Регуляторная. Некоторые гормоны являются белками
3.Структурная. Во все структуры живой клетки входят белки.
4.Рецепторная. Белки являются обязательным компонентом рецепторов, способны узнавать другие молекулы.
5.Транпортная. Транспорт жиров, лекарственных веществ и д.р.
6.Опорная. Коллаген, белки костной ткани.
7.Энергетическая. Окисление 1 грамма белка сопровождается выделением 17 КДЖ энергии. В сутки 15% энергии образуется за счёт распада Б.
8.Сократительная. Актин, миозин мышц.
9.Генно-регуляторная (ГИСТОНЫ).
10.Иммунологическая. Антитела являются белками.
11 .Гемостатическая. Фибриноген.
Структурная организация белков.
Свойства белков обусловлены их структурой.
ПЕРВИЧНАЯ СТРУКТУРА – линейное последовательное соединение АК в ПОЛИПЕПТИДНОЙ цепи с помощью ПЕПТИДНЫХ связей. Она закодирована в молекуле ДНК, белки имеют уникальную первичную структуру.
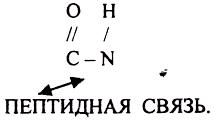
Свойства ПОЛИПЕПТИДНОЙ цепи зависят от составляющих её АК. Порядок АК в цепи устанавливается с помощью СЕКВЕНИРОВАНИЯ - процедура выявления последовательности АК. Впервые было проведено в 1958 г. Ф. СЕНДЖЕРОМ на инсулине.
ВТОРИЧНАЯ СТРУКТУРА - способ укладки в пространстве ПОЛИПЕПТИДНОЙ цепи, который образуется в результате взаимодействия между функциональными группами, входящими в состав пептидного остова. Образуется за счет водородных связей между 1 и 4 АК.
![]()
Выделяют 3 вида вторичной структуры:
1 .Альфа спираль ( Л.ПОЛЛИНГ) - виток составляет от 3 до 6 АК. Терминатором спирали является АК-ПРОЛИН.
2.Бетта складчатый слой.
СУПЕРВТОРИЧНАЯ СТРУКТУРА - промежуточное положение между первичной и вторичной структурами. Она формирует похожие сочетания и взаиморасположения вторичных структур. Например: «цинковый палец» и «Лейциновая молния».
ТРЕТИЧНАЯ СТРУКТУРА – тип конформации, который образуется за счет взаимодействий между радикалами аминокислот. Осуществляется за счёт водородных, ионных, ДИСУЛЬФИДНЫХ и гидрофобных связей. В результате формируются глобулярные и фибриллярные структуры. Например: Глобулярные – миоглобин, гемоглобин; Фибриллярные - коллаген, эластин.
Конформация – это конфигурация полипептидной цепи в пространстве.
ЧЕТВЕРТИЧНАЯ СТРУКТУРА – способ укладки в пространстве нескольких полипептидных цепей с формированием единого структурно-функционального образования - олигомера.
Домены - это фрагменты ПОЛИПЕПТИДНОЙ цепи, сходные по свойствам. Домен автономен. Домены возникают в результате слияния нескольких генов отдельных белков.
