
- •Домашня робота
- •«Сертифікаційні випробування бма»
- •Завдання
- •Теоретичні відомості
- •Практична частина
- •Загальні вимоги до безпеки медичних виробів та ознайомлення з класифікацією бма.
- •2.2.1.Об’єкт випробувань:
- •Загальні положення:
- •Об'єм випробування.
- •Вказівки щодо заходів безпеки
- •Правила зберігання та транспортування
- •Можливі несправності і способи їх усунення
- •Безпечність.
- •Випробування на електромагнітну сумісність
- •Вимірювання опору заземлення. Обладнання.
- •Значення опору заземлення
- •Висновок по роботі
Практична частина
Загальні вимоги до безпеки медичних виробів та ознайомлення з класифікацією бма.
Відповідно до ДСТУ 3798-98. Вироби медичні електричні. Частина 1. Загальні вимоги безпеки (ІЕС 60601-1:1988), загальні вимоги до безпеки медичних виробів має наступний зміст.
Медичні вироби при експлуатації не повинні створювати на робочих місцях медичного персоналу та інших користувачів рівні шкідливих факторів (фізичних, хімічних і біологічних), що перевищують гранично допустимі, відповідно до вимог санітарного законодавства.
Вироби повинні забезпечувати безпеку пацієнта або безпеку і здоров'я користувачів або, у відповідних випадках, інших осіб, і будь-який ризик пов'язаний з їх застосуванням, повинен бути прийнятним у порівнянні з користю для пацієнта і рівнем забезпечення здоров'я та безпеки.
Технічні характеристики та експлуатаційні властивості виробу не повинні чинити такий шкідливий вплив, яке піддавав би ризику безпеку пацієнтів і медичного персоналу або інших осіб протягом терміну служби виробу, зазначеного виробником, при експлуатації відповідно до інструкцій виробника.
На кожен вид вироби медичного призначення, вихідної сировини і матеріалів для їх виготовлення підприємство-виробник оформляє і затверджує в установленому порядку нормативно-технічну документацію, в тому числі рецептуру або склад. У нормативній документації та інших, які подаються для санітарно-гігієнічної оцінки матеріалах на медичні вироби зазначаються:
- Призначення продукції і область застосування;
- Опис вироби із зазначенням (за необхідності) виду і тривалості контакту з організмом;
- Склад або рецептура використовуваних матеріалів;
- Гігієнічно значущі технічні параметри та характеристики (для виробів медичної техніки),
- Дата виробництва;
- Рекомендації щодо безпечної експлуатації.
В експлуатаційній документації на вироби медичної техніки вказуються всі можливі види небезпек (тобто фізичні та інші фактори, що генеруються даним обладнанням), їх гігієнічно значущі технічні параметри та характеристики, а також вимоги і засоби забезпечення безпеки при експлуатації та обслуговуванні виробів.
Вироби повинні бути розроблені, виготовлені і упаковані таким чином, щоб їх технічні характеристики та експлуатаційні властивості в період використання виробів за призначенням не відчували шкідливого впливу при транспортуванні і зберіганні виробі.
Вироби медичного призначення і медичної техніки повинні бути забезпечені етикеткою (маркуванням), яка інформує користувача про виробника, області застосування продукції, про терміни і умови застосування та зберігання, а також попереджає про заходи безпеки при експлуатації продукції. За відсутності необхідності прийняття заходів безпеки виробник вказує: «Дотримання заходів безпеки не потрібно». Виробник ІМТ, генеруючого рівні фізичних факторів, що перевищують допустимі, в комплект поставки повинен включати засоби індивідуального захисту (протишумові вкладиші, захисні окуляри, рукавиці) в кількості не менше 2-х шт.
Програма випробувань АПАРАТ ДЛЯ УЗТ-3.02:
Ультразвукова терапія - лікувальне використання ультразвуку шляхом застосування високочастотних ультразвукових хвиль (механічних коливань). Обладнання прилади і апарати для ультразвукової терапії використовують ультразвук з частотою діапазону від 800-3000 кГц.
Зовнішній вигляд апарту наведено на рисунку 1.
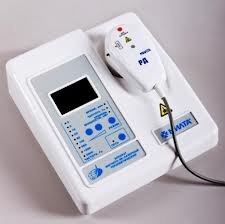
Рисунок 1 - Зовнішній вигляд апарату УЗТ-3.02
