- •Введение
- •1. ДИсперсная система
- •Классификация дисперсных систем в зависимости от размера частиц дисперсной фазы
- •2) Наиболее общая классификация дисперсных систем основана на различии в агрегатном состоянии дисперсионной среды и дисперсной фазы.
- •2. Лиофильные и лиофобные системы
- •3.Суспензии, золи. Гели
- •4. Методы исследования дисперсных систем
- •5. Коллоидные растворы в природе и технике
- •6. Контрольные вопросы
- •7. Индивидуальное задание
- •Литература
- •Оглавление
- •Литература……………………………………………………...22 Белова Светлана Борисовна
- •Диспесные системы
- •109240, Москва, Берниковская наб., 14.
МИНОБРНАУКИ РОССИИ
Федеральное государственное образовательное учреждение высшего профессионального образования
"МАТИ" Российский государственный технологический
университет имени К.Э. Циолковского (МАТИ)
___________________________________________________
Кафедра «Моделирование систем и информационные технологии»
ДИСПЕРСНЫЕ СИСТЕМЫ
Методические указания к практическим занятиям
по курсу «ХИМИЯ»
Составители:
Белова С.Б.
Гришина Н.Д.
Белов С.П.
МОСКВА 2012
Методические указания к практическим занятиям
по курсу «Химия» / сост. С.Б.Белова, Н.Д.Гришина, С.П.Белов ─ М.: МАТИ, 2012 ─ с.24
© Белова С.Б.,
Гришина Н.Д.
Белов С.П.
составление, 2012
© МАТИ, 2011
Введение
Большинство веществ окружающего нас мира существует в виде дисперсных систем: почвы, ткани живых организмов, пищевые продукты и др. Свойства вещества в раздробленном, или дисперсном, состоянии отличаются от свойств того же вещества в недисперсном состоянии. Под дисперсным состоянием понимают состояние системы, в котором одно вещество (дисперсная фаза) распределено в другом (дисперсионная среда или фаза).
Важнейшая особенность дисперсного состояния вещества состоит в том, что энергия системы главным образом сосредоточена на поверхности раздела фаз. Диспергирование (измельчение) вещества приводит к возникновению избытка свободной энергии поверхностных слоев, т. е. тонких слоев вещества на границе соприкосновения тел (сред, фаз). Особые свойства поверхностных слоев отражаются в поверхностных явлениях. Раздел химии, в котором изучаются дисперсные системы и поверхностные явления называется коллоидной химией.
В коллоидной химии изучаются такие явления, как адгезия, адсорбция, смачивание, коагуляция, электрофорез. Разрабатываются технологии строительных материалов, бурения горных пород, зол-гель технологии. Коллоидная химии играет фундаментальную роль в нанотехнологии.
Данные методические указания направлены на ознакомление с классификацией дисперсных систем, а также со строением и свойствами коллоидных растворов.
1. ДИсперсная система
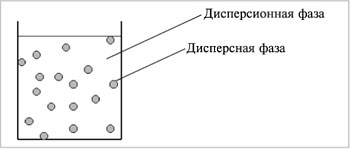
Дисперсные системы – это системы, в которых мелкие частицы вещества, или дисперсная фаза, распределены в однородной среде (жидкость, газ, кристалл), или дисперсионной фазе (дисперсионной среде) (рис.1.1).
|
Рис.1. Дисперсная система |
Существует несколько различных классификаций дисперсных систем: 1) по размеру частиц, 2) по фазовому состоянию дисперсной фазы и дисперсионной среды, 3) по характеру взаимодействия частиц дисперсной фазы с веществом дисперсионной среды, 4) по термодинамической и кинетической устойчивости дисперсных систем и т.п.
1) Размер частиц дисперсной фазы характеризуется дисперсностью.Cтепень раздробленности вещества дисперсной фазы называется степенью дисперсности D:.
D = 1/a см-1…………........................................(1),
где a – размер дисперсных частиц. Под a понимается либо диаметр сферических или волокнистых частиц, либо длина ребра кубических частиц, либо толщине пленок.
Степень дисперсности численно равна числу частиц, которые можно плотно уложить в ряд на протяжении одного сантиметра.
Чем больше степень дисперсности, тем меньше размер частиц.
В зависимости от дисперсности дисперсные системы можно разделить на высокодисперсные, или собственно коллоидные, и низкодисперсные (грубодисперсные).
Высокодисперсные системы в зависимости от размера частиц подразделяют на ультрамикро- и микрогетерогенные системы
Таблица 1.
Классификация дисперсных систем в зависимости от размера частиц дисперсной фазы
Название |
Размер частиц, м |
Ультрамикрогетерогенные |
10−9…10−7 |
Микрогетерогенные |
10−7…10−5 |
Грубодисперсные |
более 10−5 |
Ультрамикрогетерогенные системы также называют коллоидными или золями. В зависимости от природы дисперсионной среды, золи подразделяют на твёрдые золи, аэрозоли (золи с газообразной дисперсионной средой) и лиозоли (золи с жидкой дисперсионной средой).
К микрогетерогенным системам относят суспензии, эмульсии, пены и порошки. Наиболее распространёнными грубодисперсными системами являются системы «твёрдое — газ», например, песок.
Размер частиц высокодисперсных систем как минимум, на порядок больше размера частиц в истинных растворах (т.е. растворах, в которых частицы не могут быть обнаружены оптическим путем). В ионных растворах размер частиц менее 1×10−9 м, частицы в таких растворах невозможно обнаружить оптическими методами; в то время как в коллоидных растворах с размером частиц 1×10−9 м — 5×10−7 м их можно обнаружить при помощи ультрамикроскопа (эффект Тиндаля).
Системы с одинаковыми по размерам частицами дисперсной фазы называются монодисперсными, а с неодинаковыми по размеру частицами — полидисперсными. Как правило, окружающие нас реальные системы полидисперсны.