- •Методическое пособие для студентов нехимических специальностей заочного отделения
- •Подготовлено к печати на кафедре органической химии
- •Редактор
- •1. Введение
- •Свойства ковалентной связи.
- •Понятие об индуктивном и мезомерном эффектах
- •Классификация органических реагентов и реакций.
- •2. Номенклатура органических соединений
- •3. Углеводороды
- •3.1. Алканы (предельные, насыщенные углеводороды)
- •3.1.1. Методы получения алканов.
- •3.1.2. Химические свойства алканов
- •Реакции замещения
- •3.2 Циклоалканы
- •Непредельные или ненасыщенные углеводороды
- •3.3 Алкены
- •3.3.1.Методы получения
- •3.3.2.Химические свойства алкенов
- •3.4. Алкадиены.
- •3.5. Алкины.
- •3.5.1.Химические свойства алкинов
- •Как и в случае алкенов реакция идет в присутствии катализаторов (Pt, Pd, Ni и др.) и может быть остановлена на стадии образования алкена.
- •3.6. Реакция полимеризации алкенов и алкадиенов (синтез высокомолекулярных соединений).
- •4. Функциональные производные углеводородов.
- •4.1. Галогенопроизводные.
- •4.1.1. Методы получения и химические свойства галогенопроизводных.
- •5. Кислородосодержащие соединения.
- •5.1. Алканолы (спирты).
- •5.1.1 . Получение спиртов.
- •5.1.2. Химические свойства спиртов.
- •Реакция со щелочными металлами
- •5.2. Альдегиды, кетоны, карбоновые кислоты.
- •5.2.1. Методы получения альдегидов, кетонов, карбоновых кислот.
- •5.2.2. Химические свойства альдегидов и кетонов.
- •5.2.3. Химические свойства карбоновых кислот
- •6. Азотосодержащие производные углеводородов
- •6.1. Алифатические нитросоединения.
- •6.2. Алифатические амины.
- •6.2.1. Химические свойства аминов
- •Основные свойства
- •6.3. Аминокислоты и их производные.
- •6.3.1. Полиамидные волокна.
- •7. Изомерия органических соединений
- •Структурная изомерия
- •Пространственная изомерия
- •8. Сахариды (углеводы)
- •8.1.Моносахариды
- •8.1.1 Строение, изомерия
- •8.1.2. Химические свойства моносахаридов
- •8.2. Полисахариды
- •9. Арены. Ароматические углеводороды и их производные.
- •9.1. Бензол и его производные. Строение, изомерия.
- •9.1.1. Методы получения углеводородов ряда бензола.
- •9.1.2. Химические свойства углеводородов ряда бензола.
- •Электрофильное замещение.
- •Влияние заместителей в бензольном ядре на реакцию электрофильного замещения.
- •9.3. Ароматические амины.
- •9.3.1. Химические свойства аминов
- •Реакции аминогруппы.
- •Реакции ароматического ядра.
- •9.4. Ароматические азо- и диазосоединения. Азокрасители.
- •9.4.1. Химические свойства солей диазония
- •Реакции с выделением азота.
- •Реакции без выделения азота.
- •Контрольная работа №1.
- •Вариант №1
- •Контрольная работа № 2.
- •Содержание
- •1. Введение…………………………………………….……………...3
5.2.1. Методы получения альдегидов, кетонов, карбоновых кислот.
Некоторые альдегиды, кетоны и кислоты выделяют из природных источников для целей парфюмерной и косметической отраслей.
Основное количество указанных производных получают синтетически, используя реакции: окисления алканов (см. гл. 3.1), гидролиз нитрилов (см. гл. 4.1), и др.
5.2.2. Химические свойства альдегидов и кетонов.
Химические свойства альдегидов и кетонов определяют особенности строения карбонильной группы.
Вследствие высокой электроотрицательности атома кислорода π- связь карбонильной группы сильно поляризована и она легко атакуется нуклеофильными реагентами.
Для карбонильных соединений характерны реакции нуклеофильного присоединения, присоединения – отщепления, замещения карбонильной группы, окисления.
Присоединение.
Синильная кислота присоединяется с образованием нитрилоксидов.
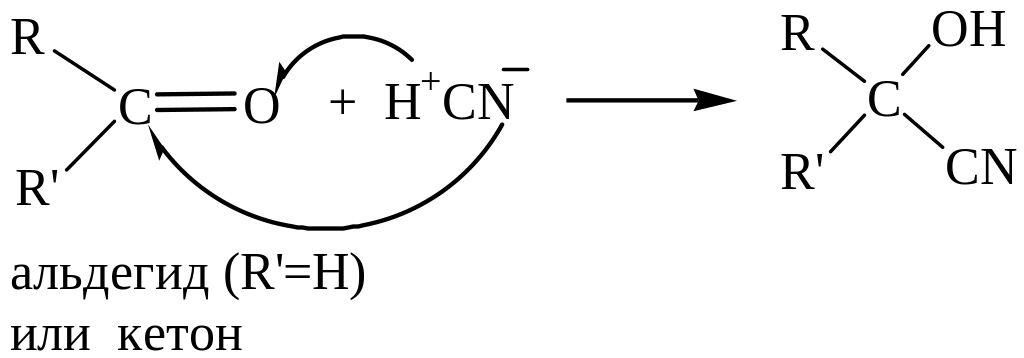
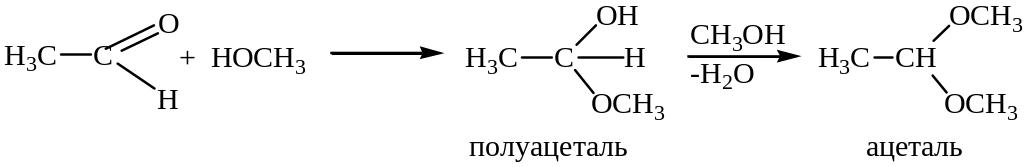
Спирты (в присутствии кислот или оснований) реагируют с альдегидами с образованием полуацеталей, вновь образовавшийся гидроксил в которых имеет повышенную реакционную способность и часто в условиях реакции реагирует со второй молекулой спирта, образуя ацеталь.
Присоединение – отщепление.
Альдегиды и кетоны реагируют с рядом соединений содержащих группу –NH2 по схеме
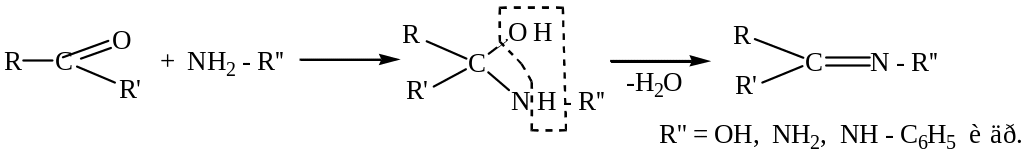
Замещение.
При взаимодействии альдегидов и кетонов с PCl5 происходит замещение карбонильного кислорода на два атома хлора
![]()
Окисление.
Окисление альдегидов идет значительно легче, чем кетонов. Кроме того, окисление альдегидов приводит к образованию кислот без изменения углеродного скелета.
Качественная реакция на альдегиды – реакция серебряного зеркала.
Аммиачный раствор окиси серебра [Ag(NH3)2]OH при легком нагревании с альдегидами окисляет альдегид в кислоту с образованием металлического серебра.
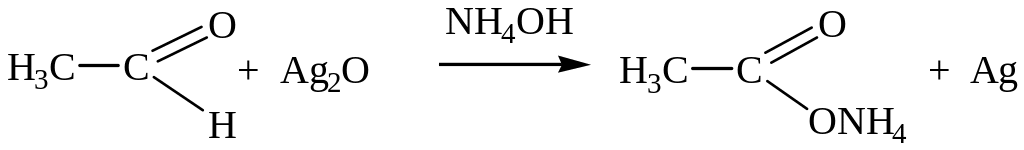
Поскольку у кетонов отсутствует атом водорода у карбонильного углерода, окисление их протекает в значительно более жестких условиях и проходит с разрывом связей С – С углеродного скелета.
Присоединение водорода (восстановление).
Водород присоединяется по двойной связи карбонильной группы в присутствии каталитических количеств Ni, Cо, Cu, Pt. При этом альдегиды превращаются в первичные спирты, а кетоны во вторичные.
5.2.3. Химические свойства карбоновых кислот
Химические свойства карбоновых кислот обусловлены наличием карбоксильной группы. Они имеют ярко выраженный кислотный характер. Это объясняется взаимным влиянием атомов в карбоксильной группе: электронная плотность смещена в сторону наиболее электроноакцепторного атома – кислорода. Тем самым ослаблена связь между атомами кислорода и водорода и облегчена диссоциация по кислотному типу.
+δ
-δ
Органические кислоты образуют соли с металлами, оксидами, гидроксидами.
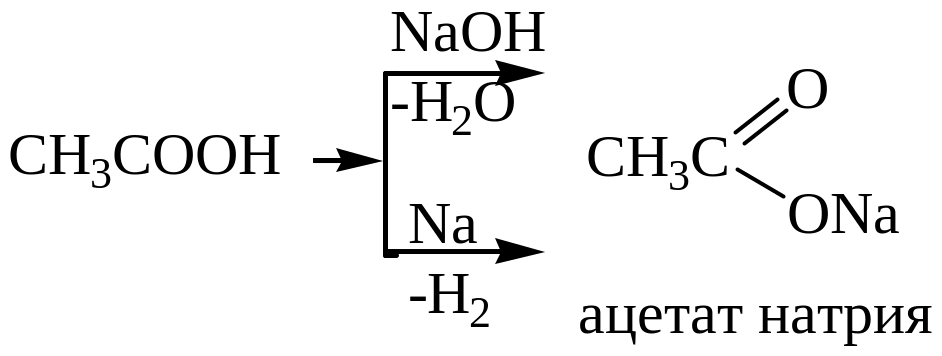
При действии галогенидов фосфора образуются галогенангидриды кислот

Ангидриды кислот образуются при взаимодействии солей кислот с галогенангидридами.
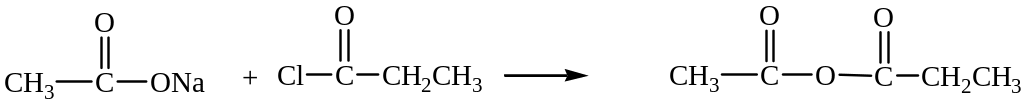
или в присутствии водоотнимающих средств.
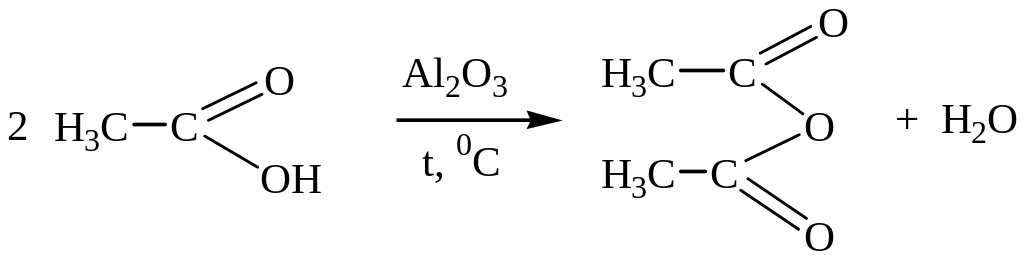
Из производных карбоновых кислот отметим также такие важные соединения как амиды и нитрилы, схемы получения которых приведены ниже.
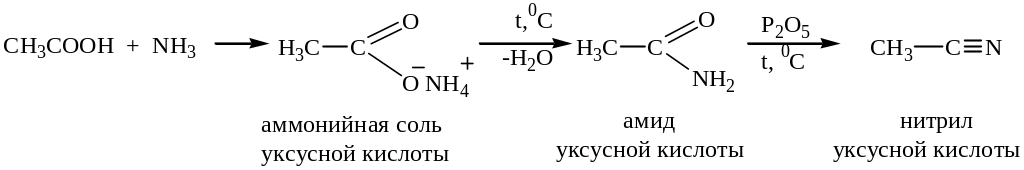
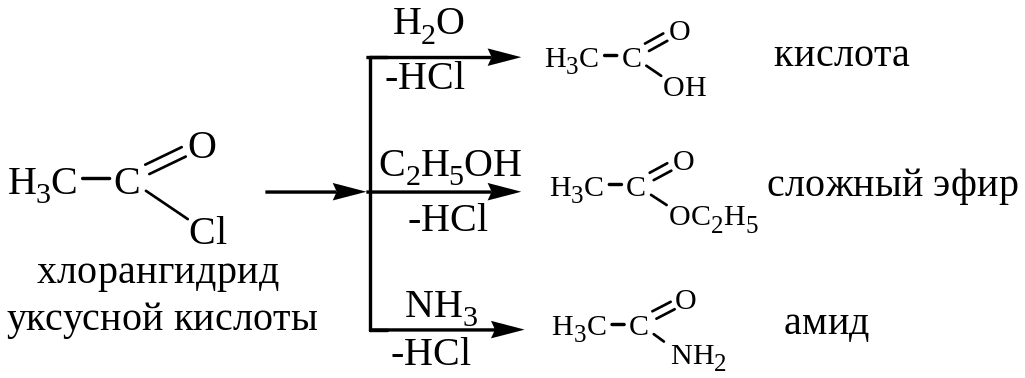
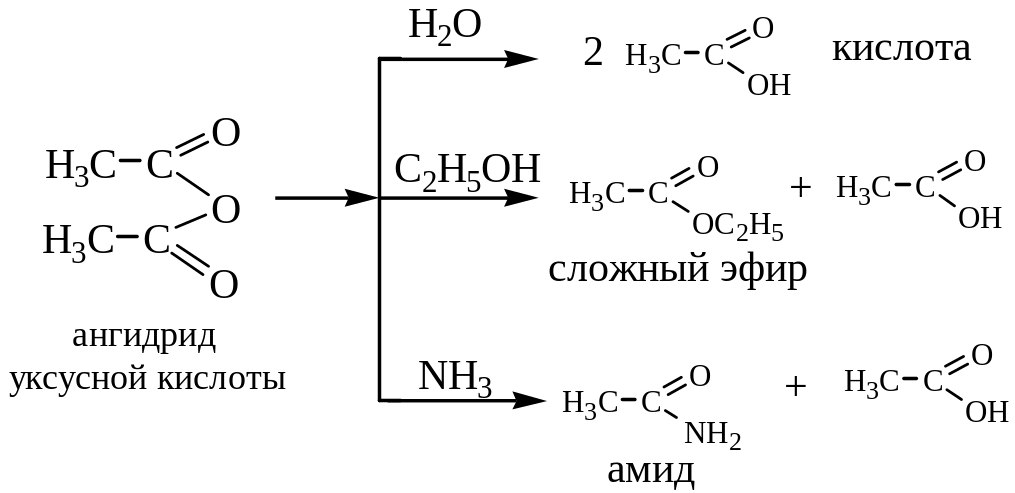
Реакционноспособными производными карбоновых кислот являются галогенангидриды и ангидриды, которые широко используются как в тонком органическом синтезе, так и в производстве лекарственных препаратов, товаров бытовой химии. Уксусный ангидрид в огромных количествах используется в производстве ацетатного волокна (см. гл. 8).
Ниже приведены некоторые реакции указанных производных.