- •Методическое пособие для студентов нехимических специальностей заочного отделения
- •Подготовлено к печати на кафедре органической химии
- •Редактор
- •1. Введение
- •Свойства ковалентной связи.
- •Понятие об индуктивном и мезомерном эффектах
- •Классификация органических реагентов и реакций.
- •2. Номенклатура органических соединений
- •3. Углеводороды
- •3.1. Алканы (предельные, насыщенные углеводороды)
- •3.1.1. Методы получения алканов.
- •3.1.2. Химические свойства алканов
- •Реакции замещения
- •3.2 Циклоалканы
- •Непредельные или ненасыщенные углеводороды
- •3.3 Алкены
- •3.3.1.Методы получения
- •3.3.2.Химические свойства алкенов
- •3.4. Алкадиены.
- •3.5. Алкины.
- •3.5.1.Химические свойства алкинов
- •Как и в случае алкенов реакция идет в присутствии катализаторов (Pt, Pd, Ni и др.) и может быть остановлена на стадии образования алкена.
- •3.6. Реакция полимеризации алкенов и алкадиенов (синтез высокомолекулярных соединений).
- •4. Функциональные производные углеводородов.
- •4.1. Галогенопроизводные.
- •4.1.1. Методы получения и химические свойства галогенопроизводных.
- •5. Кислородосодержащие соединения.
- •5.1. Алканолы (спирты).
- •5.1.1 . Получение спиртов.
- •5.1.2. Химические свойства спиртов.
- •Реакция со щелочными металлами
- •5.2. Альдегиды, кетоны, карбоновые кислоты.
- •5.2.1. Методы получения альдегидов, кетонов, карбоновых кислот.
- •5.2.2. Химические свойства альдегидов и кетонов.
- •5.2.3. Химические свойства карбоновых кислот
- •6. Азотосодержащие производные углеводородов
- •6.1. Алифатические нитросоединения.
- •6.2. Алифатические амины.
- •6.2.1. Химические свойства аминов
- •Основные свойства
- •6.3. Аминокислоты и их производные.
- •6.3.1. Полиамидные волокна.
- •7. Изомерия органических соединений
- •Структурная изомерия
- •Пространственная изомерия
- •8. Сахариды (углеводы)
- •8.1.Моносахариды
- •8.1.1 Строение, изомерия
- •8.1.2. Химические свойства моносахаридов
- •8.2. Полисахариды
- •9. Арены. Ароматические углеводороды и их производные.
- •9.1. Бензол и его производные. Строение, изомерия.
- •9.1.1. Методы получения углеводородов ряда бензола.
- •9.1.2. Химические свойства углеводородов ряда бензола.
- •Электрофильное замещение.
- •Влияние заместителей в бензольном ядре на реакцию электрофильного замещения.
- •9.3. Ароматические амины.
- •9.3.1. Химические свойства аминов
- •Реакции аминогруппы.
- •Реакции ароматического ядра.
- •9.4. Ароматические азо- и диазосоединения. Азокрасители.
- •9.4.1. Химические свойства солей диазония
- •Реакции с выделением азота.
- •Реакции без выделения азота.
- •Контрольная работа №1.
- •Вариант №1
- •Контрольная работа № 2.
- •Содержание
- •1. Введение…………………………………………….……………...3
3.3 Алкены
Гомологический ряд выражен общей формулой CnH2n.
Названия ненасыщенных углеводородов с одной двойной связью – алкенов – образуют, заменяя суффикс -ан в алкане, на -ен в алкене.
![]()
В качестве главной выбирают самую длинную углеродную цепь, содержащую двойную связь, и нумеруют ее так, чтобы двойная связь получила наименьший порядковый номер. Эти правила проиллюстрированы примером.
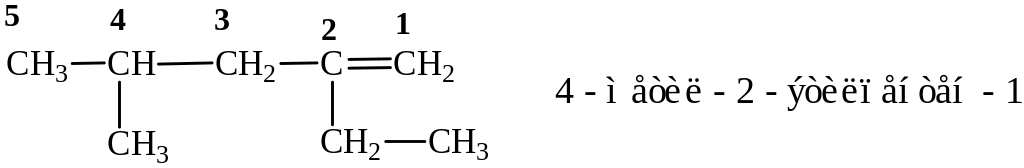
3.3.1.Методы получения
Основные методы образования двойной связи см.: крекинг и дегидрирование алканов (гл. 3.1), дегидрогалогенирование и дегалогенирование алкилгалогенидов (гл. 4.1.), дегидратация спиртов (гл. 5.1.)
3.3.2.Химические свойства алкенов
Особенности строения двойной углерод-углеродной связи см. [1], гл. 3.
В химических реакциях двойная связь выступает как донор электронов, т.е. она легко атакуется электрофильными реагентами.
Как уже отмечалось, наиболее характерны для алкенов реакции присоединения.
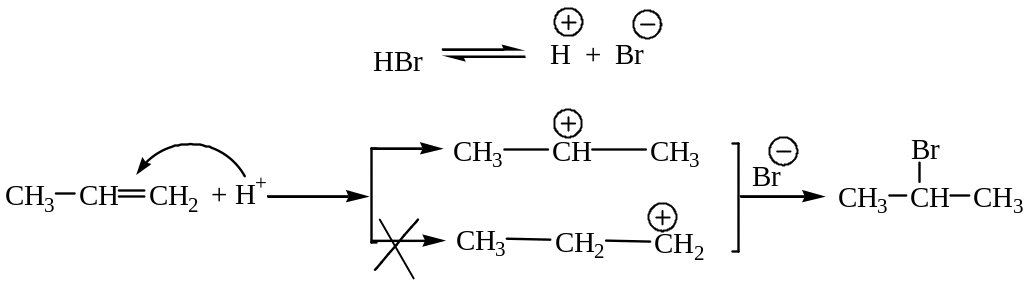
Присоединение галогеноводородов.
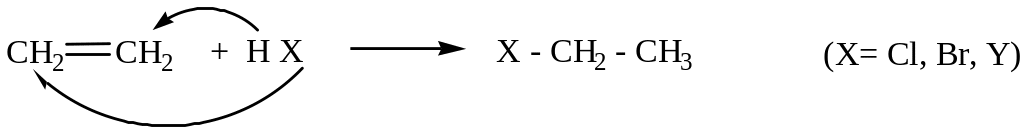
Указанные реакции проходят по механизму электрофильного присоединения, т.к. первая стадия реакции - атака протона (Н+) по двойной связи; вторая стадия - разрыв двойной связи и образование карбкатиона.
Пример - присоединение HBr к несимметричному алкену – пропену. Реакция протекает по правилу Марковникова, в соответствии с которым “водород присоединяется к наиболее гидрогенизированному атому углерода”, т.е. содержащему большее число атомов водорода.
Присоединение водорода (реакция гидрирования).
Реакция идет в присутствии различных катализаторов (Pt, Pd, Ni и др.).
Реакция может рассматриваться как метод получения алканов.
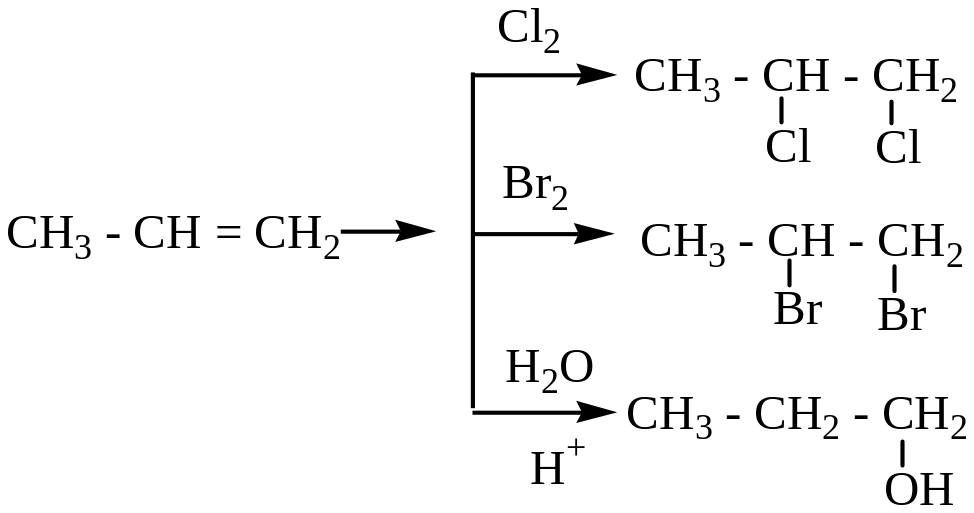
Присоединение галогенов и воды.
Эти реакции также идут по электрофильному механизму.
При присоединении воды соблюдается правило Марковникова.
Присоединение водорода (реакция гидрирования).
Реакция идет в присутствии различных катализаторов (Pt, Pd, Ni и др.).
Реакция может рассматриваться как метод получения алканов.
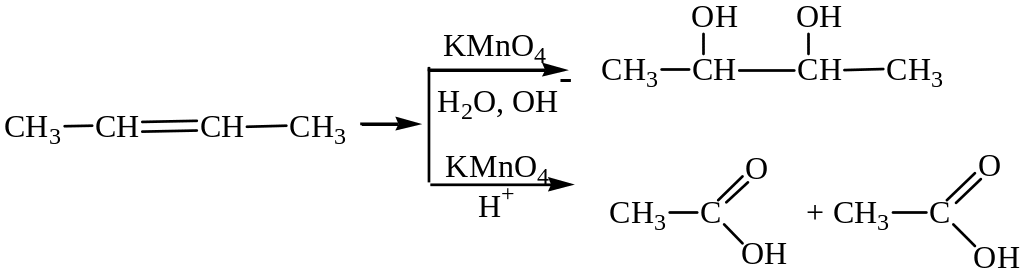
Реакции окисления.
При окислении алкенов реакция идёт по двойной связи. В зависимости от условий реакции образуются различные продукты.
3.4. Алкадиены.
Гомологический ряд выражен общей формулой CnHn.
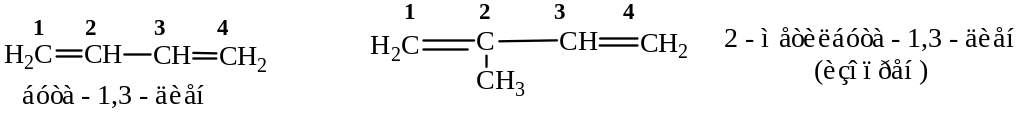
Названия ненасыщенных углеводородов с двумя двойными связями образуют, заменяя суффикс -ан в алкане на -диен в алкадиене.
![]()
Диеновые углеводороды в качестве химических реактивов для научных исследований, лабораторной практики и в промышленных целях получают синтетически. Основные методы их синтеза основаны на тех же реакциях отщепления, что и получение алкенов, например, дегидрогалогенирование алканов или дегидратация спиртов.
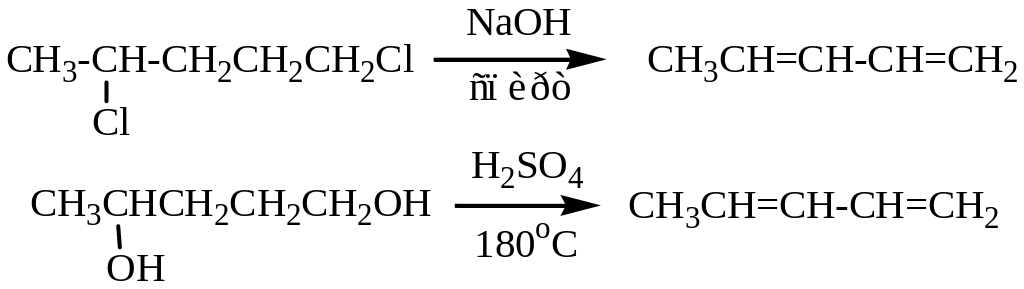
В зависимости от взаимного расположения двойных связей алкадиены заметно различаются по своим физико-химическим свойствам. Наибольшее практическое применение нашли так называемые сопряженные диены, в молекулах которых две двойные связи разделены одной простой.
Особенностью сопряженных алкадиенов является то, что вследствие близкого взаимного расположения π-электронные облака двух двойных связей взаимно перекрываются, образуя единую 4х – электронную систему, которая в реакциях с электрофильными реагентами и других реакциях ведёт себя как “единое целое”.
Для сопряженных диенов характерны реакции как “обычного” 1,2-присоединения, так и “необычного” – 1,4-присоединения.