- •Методическое пособие для студентов нехимических специальностей заочного отделения
- •Подготовлено к печати на кафедре органической химии
- •Редактор
- •1. Введение
- •Свойства ковалентной связи.
- •Понятие об индуктивном и мезомерном эффектах
- •Классификация органических реагентов и реакций.
- •2. Номенклатура органических соединений
- •3. Углеводороды
- •3.1. Алканы (предельные, насыщенные углеводороды)
- •3.1.1. Методы получения алканов.
- •3.1.2. Химические свойства алканов
- •Реакции замещения
- •3.2 Циклоалканы
- •Непредельные или ненасыщенные углеводороды
- •3.3 Алкены
- •3.3.1.Методы получения
- •3.3.2.Химические свойства алкенов
- •3.4. Алкадиены.
- •3.5. Алкины.
- •3.5.1.Химические свойства алкинов
- •Как и в случае алкенов реакция идет в присутствии катализаторов (Pt, Pd, Ni и др.) и может быть остановлена на стадии образования алкена.
- •3.6. Реакция полимеризации алкенов и алкадиенов (синтез высокомолекулярных соединений).
- •4. Функциональные производные углеводородов.
- •4.1. Галогенопроизводные.
- •4.1.1. Методы получения и химические свойства галогенопроизводных.
- •5. Кислородосодержащие соединения.
- •5.1. Алканолы (спирты).
- •5.1.1 . Получение спиртов.
- •5.1.2. Химические свойства спиртов.
- •Реакция со щелочными металлами
- •5.2. Альдегиды, кетоны, карбоновые кислоты.
- •5.2.1. Методы получения альдегидов, кетонов, карбоновых кислот.
- •5.2.2. Химические свойства альдегидов и кетонов.
- •5.2.3. Химические свойства карбоновых кислот
- •6. Азотосодержащие производные углеводородов
- •6.1. Алифатические нитросоединения.
- •6.2. Алифатические амины.
- •6.2.1. Химические свойства аминов
- •Основные свойства
- •6.3. Аминокислоты и их производные.
- •6.3.1. Полиамидные волокна.
- •7. Изомерия органических соединений
- •Структурная изомерия
- •Пространственная изомерия
- •8. Сахариды (углеводы)
- •8.1.Моносахариды
- •8.1.1 Строение, изомерия
- •8.1.2. Химические свойства моносахаридов
- •8.2. Полисахариды
- •9. Арены. Ароматические углеводороды и их производные.
- •9.1. Бензол и его производные. Строение, изомерия.
- •9.1.1. Методы получения углеводородов ряда бензола.
- •9.1.2. Химические свойства углеводородов ряда бензола.
- •Электрофильное замещение.
- •Влияние заместителей в бензольном ядре на реакцию электрофильного замещения.
- •9.3. Ароматические амины.
- •9.3.1. Химические свойства аминов
- •Реакции аминогруппы.
- •Реакции ароматического ядра.
- •9.4. Ароматические азо- и диазосоединения. Азокрасители.
- •9.4.1. Химические свойства солей диазония
- •Реакции с выделением азота.
- •Реакции без выделения азота.
- •Контрольная работа №1.
- •Вариант №1
- •Контрольная работа № 2.
- •Содержание
- •1. Введение…………………………………………….……………...3
Свойства ковалентной связи.
Для понимания особенностей химических свойств органических соединений важно иметь представление о некоторых свойствах ковалентных химических связей.
Длина связи – расстояние между центрами атомов в молекуле. Длина связи зависит от типа связи, типов связанных атомов, влияния соседних атомов и некоторых других факторов. Ниже приведены средние значения для некоторых типов связей.
-
Соединение
Тип связи
Длина связи, нм

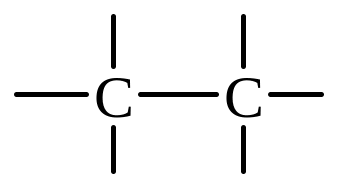
0,154
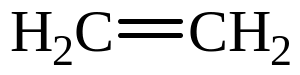
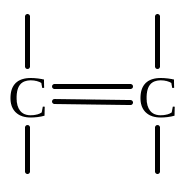
0,134


0,120
Энергия связи – энергия необходимая для разрушения конкретной связи в молекуле в газообразном состоянии, т.е. по сути – прочность связи. Ниже приведены усредненные значения энергии для некоторых типов связи
-
Связь
Энергия, кДж/моль
335
628
837
Полярность связи – характеризует смещение электронной пары, образующей связь, к одному из связанных атомов. Эффект обусловлен различной способностью атомов притягивать электроны (электроотрицательность), а также влиянием соседних со связанными атомами групп, внешними влияниями на молекулу и т. д.
Примеры:
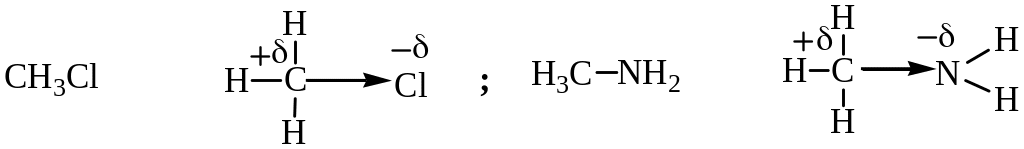
Валентный угол (угол между связями) – определяется в первую очередь типом орбиталей, образующих связь (см. [1] гл.3). Напомним значения валентных углов (α) в некоторых соединениях:
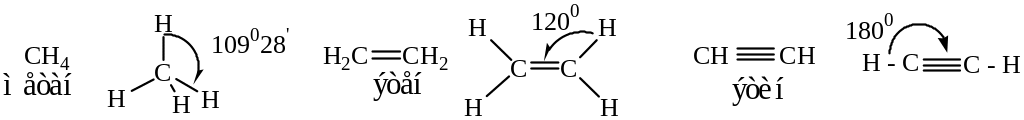
Понятие об индуктивном и мезомерном эффектах
Индуктивный эффект – смещение электронов в молекуле по системе простых (одинарных или σ) связей. Основная причина - различие в электроотрицательностях связанных атомов. Эффект быстро “угасает” по цепочке связей
+δ4
+δ3
+δ2
+δ1
-δ
CH3 → CH2 → CH2 → CH2 → Cl +δ1 > +δ2 >> +δ3 >>> +δ4
Мезомерный эффект (эффект сопряжения) – эффект смещения электронов, в котором участвуют π-электроны двойных и тройных связей, а также свободные электронные пары.
![]()
Классификация органических реагентов и реакций.
Химическая реакция, в которой участвуют органические соединения, представляет собой процесс разрыва связей в реагирующих молекулах и образования новых связей в продуктах реакции.
В зависимости от строения (типа связи) реагирующей молекулы разрыв связи может происходить по гомогенному или гетерогенному механизму.
![]()
Образуются частицы с неспаренным электроном у атома - радикалы
![]()
Образуются положительно (катионы) и отрицательно (анионы) заряженные частицы.
По наиболее общей классификации органические реакции делятся на следующие типы:
Замещение — в результате реакции происходит замещение каких-либо групп или атомов на другие атомы или группы.
![]()
Присоединение — характерно для соединений с двойными или тройными связями. Результат реакции – разрыв кратной связи и присоединение по освободившимся валентностям реагирующих групп.
![]()
Отщепление — отрыв от атомов (как правило соседних) каких-либо групп или атомов с образованием двойной связи
![]()
Перегруппировка — заключается в изменении взаимного положения атомов или групп в молекуле без изменения состава молекулы.
Реагенты, т.е. атакующие частицы в зависимости от электронного строения классифицируются следующим образом:
—радикальные
частицы:
![]()
электрофильные (атакуют место с повышенной электронной плотностью в молекуле):
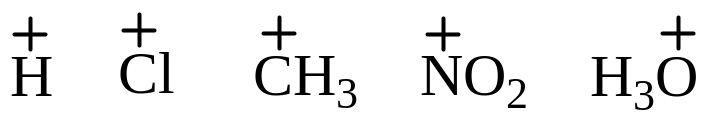
нуклеофильные (атакуют место с пониженной электронной плотностью в молекуле):
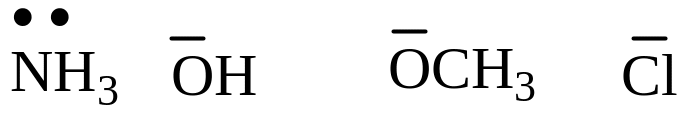
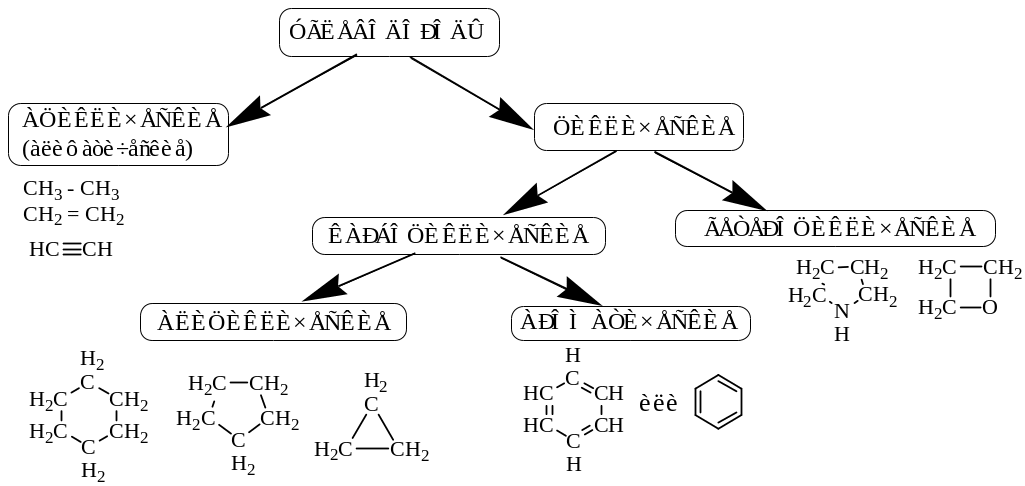
Классификация органических соединений.
Соединения, состоящие только из атомов углерода и водорода, называются углеводородами. В зависимости от строения углеводородной цепи они разделяются на ациклические или алифатические углеводороды (с открытой цепью) и циклические углеводороды (с замкнутой цепью).
Циклические углеводороды делятся на карбоциклические (содержат только атомы углерода) и гетероциклические (содержат другие атомы: N,O,S). Карбоциклические включают два ряда углеводородов: алициклические и ароматические.
Ациклические и циклические углеводороды могут содержать кратные связи (двойные или тройные). Такие углеводороды называют ненасыщенными, в отличие от насыщенных углеводородов, которые не содержат кратных связей.
Ароматические углеводороды хотя и содержат двойные связи, но только формально, поэтому их не относят к ненасыщенным углеводородам, выделяют в самостоятельную группу углеводородов.
В каждом ряду органические соединения делятся на классы в зависимости от состава и строения. Производные углеводородов содержат функциональные группы (галоген, сульфогруппу, кислородсодержащую, азотсодержащую группы), которые определяют химические свойства и определяют направление химических превращений данного класса органических соединений. Названия функциональных групп приведены в таблице 3.