- •Методическое пособие для студентов нехимических специальностей заочного отделения
- •Подготовлено к печати на кафедре органической химии
- •Редактор
- •1. Введение
- •Свойства ковалентной связи.
- •Понятие об индуктивном и мезомерном эффектах
- •Классификация органических реагентов и реакций.
- •2. Номенклатура органических соединений
- •3. Углеводороды
- •3.1. Алканы (предельные, насыщенные углеводороды)
- •3.1.1. Методы получения алканов.
- •3.1.2. Химические свойства алканов
- •Реакции замещения
- •3.2 Циклоалканы
- •Непредельные или ненасыщенные углеводороды
- •3.3 Алкены
- •3.3.1.Методы получения
- •3.3.2.Химические свойства алкенов
- •3.4. Алкадиены.
- •3.5. Алкины.
- •3.5.1.Химические свойства алкинов
- •Как и в случае алкенов реакция идет в присутствии катализаторов (Pt, Pd, Ni и др.) и может быть остановлена на стадии образования алкена.
- •3.6. Реакция полимеризации алкенов и алкадиенов (синтез высокомолекулярных соединений).
- •4. Функциональные производные углеводородов.
- •4.1. Галогенопроизводные.
- •4.1.1. Методы получения и химические свойства галогенопроизводных.
- •5. Кислородосодержащие соединения.
- •5.1. Алканолы (спирты).
- •5.1.1 . Получение спиртов.
- •5.1.2. Химические свойства спиртов.
- •Реакция со щелочными металлами
- •5.2. Альдегиды, кетоны, карбоновые кислоты.
- •5.2.1. Методы получения альдегидов, кетонов, карбоновых кислот.
- •5.2.2. Химические свойства альдегидов и кетонов.
- •5.2.3. Химические свойства карбоновых кислот
- •6. Азотосодержащие производные углеводородов
- •6.1. Алифатические нитросоединения.
- •6.2. Алифатические амины.
- •6.2.1. Химические свойства аминов
- •Основные свойства
- •6.3. Аминокислоты и их производные.
- •6.3.1. Полиамидные волокна.
- •7. Изомерия органических соединений
- •Структурная изомерия
- •Пространственная изомерия
- •8. Сахариды (углеводы)
- •8.1.Моносахариды
- •8.1.1 Строение, изомерия
- •8.1.2. Химические свойства моносахаридов
- •8.2. Полисахариды
- •9. Арены. Ароматические углеводороды и их производные.
- •9.1. Бензол и его производные. Строение, изомерия.
- •9.1.1. Методы получения углеводородов ряда бензола.
- •9.1.2. Химические свойства углеводородов ряда бензола.
- •Электрофильное замещение.
- •Влияние заместителей в бензольном ядре на реакцию электрофильного замещения.
- •9.3. Ароматические амины.
- •9.3.1. Химические свойства аминов
- •Реакции аминогруппы.
- •Реакции ароматического ядра.
- •9.4. Ароматические азо- и диазосоединения. Азокрасители.
- •9.4.1. Химические свойства солей диазония
- •Реакции с выделением азота.
- •Реакции без выделения азота.
- •Контрольная работа №1.
- •Вариант №1
- •Контрольная работа № 2.
- •Содержание
- •1. Введение…………………………………………….……………...3
Влияние заместителей в бензольном ядре на реакцию электрофильного замещения.
Если в бензольном ядре уже имеется какой-либо заместитель, то он влияет как на скорость реакции, так и на направление электрофильной атаки. Закономерности, определяющие направление реакции замещения в бензольном ядре, называются правилами ориентации.
По характеру влияния на реакцию электрофильного замещения заместители, находящиеся в бензольном кольце, можно разделить на три типа:
1. Заместители, активирующие бензольное кольцо. Электрофильное замещение соединений с такими заместителями протекает легче, чем с бензолом, а вступающий заместитель направляется в основном в орто- и пара-положения относительно уже имеющегося заместителя. Активизирующие о- и п- ориентанты:
![]()
2. Заместители, дезактивирующие бензольное кольцо и направляющие электрофильную реакцию в о- и п-положение. Электрофильное замещение для соединений с такими заместителями протекает труднее, чем с бензолом, а вступающий заместитель направляется в основном в о- и п-положения к уже имеющемуся заместителю. Дезактивирующие о- и п-ориентанты: ─I, ─Br, ─Cl, ─F, ─CH2Cl.
3. Заместители, дезактивирующие бензольное кольцо и направляющие электрофильную атаку в мета-положение. Дезактивирующие м-ориентанты:
![]()
Примеры реакций с различным ориентирующим действием заместителей:
Заместитель, активирующий бензольное кольцо, о- и п-ориентация.
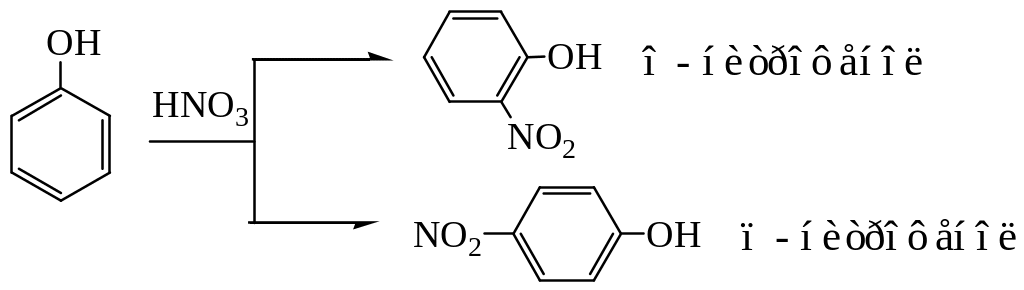
Заместитель, дезактивирующий бензольное кольцо, м-ориентация
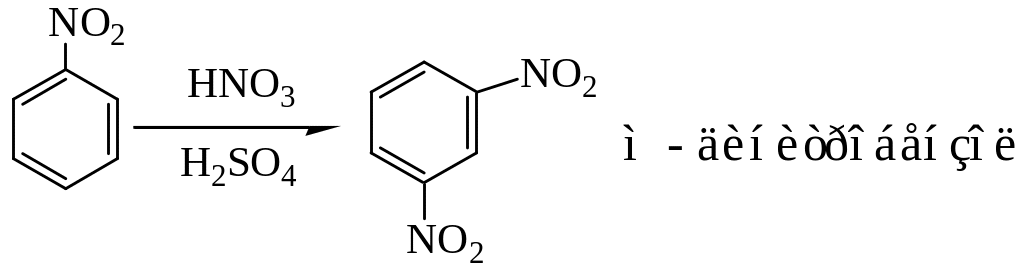
Реакции присоединения.
Гидрирование (присоединение водорода) происходит в присутствии катализатора (Ni, Pt, Pd) при повышенной температуре и давлении.
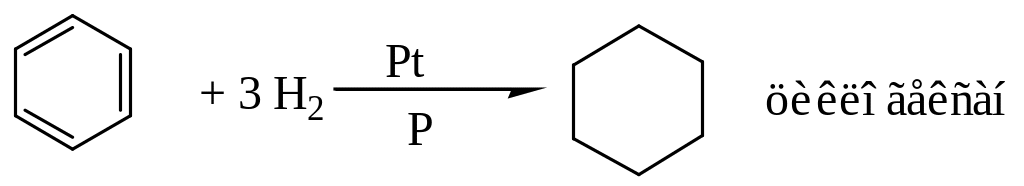
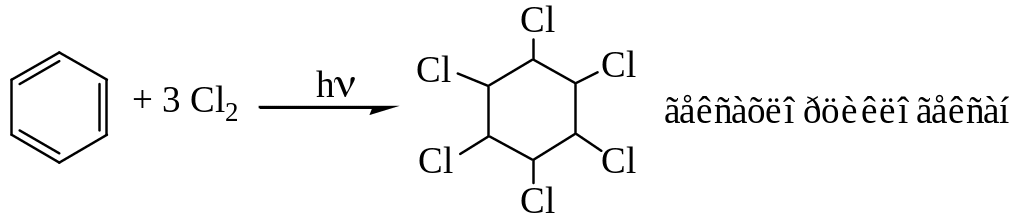
Галогенирование. На солнечном свету (под влиянием ультрафиолетового излучения) бензол присоединяет хлор и бром с образованием гексагалогенидов.
9.2. Фенолы.
Фенолами называют органические соединения, содержащие одну или несколько гидроксильных групп, непосредственно связанных с атомами углерода бензольного кольца.
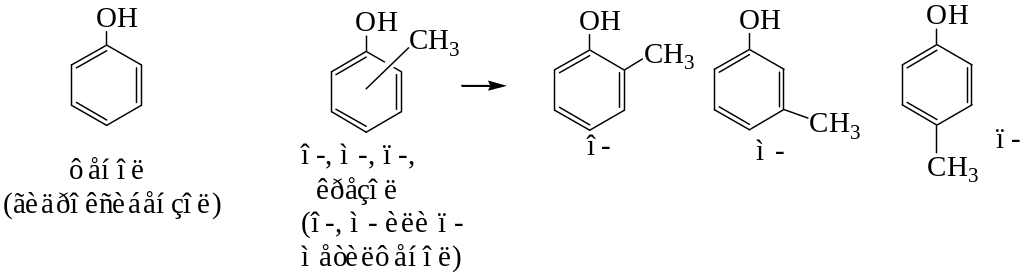
Фенолы – жидкие или кристаллические вещества с характерным запахом. При попадании на кожу вызывают ожоги.
9.2.1. Химические свойства.
Свойства фенолов обусловлены взаимным влиянием гидроксильной группы и ароматического кольца.
Реакции гидроксильной группы.
Фенолы образуют соли (феноляты) при действии водных растворов
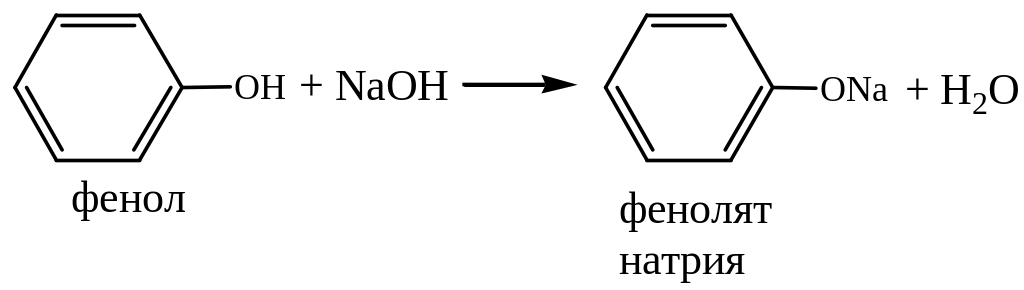
щелочей, тогда как спирты реагируют только со щелочными металлами (гл.5.1). Большая кислотность фенолов по сравнению со спиртами объясняется взаимодействием неподеленных электронных пар кислорода с -электронами ядра. В результате электронная плотность смещается в сторону ароматического кольца и обуславливает большую подвижность протона. Причем, введение электроноакцепторного заместителя (например NO2 – группы) увеличивает кислотность фенолов.
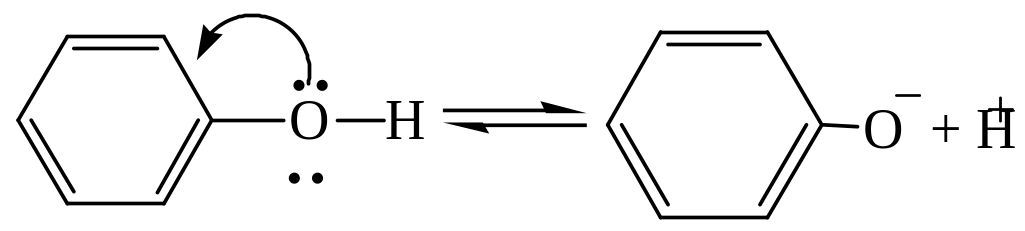
Фенолы легко алкилируются при действии на феноляты алкилгалогенидов.
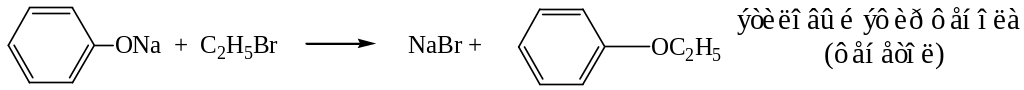
При взаимодействии фенола с хлорангидридами или ангидридами карбоновых кислот образуются сложные эфиры.
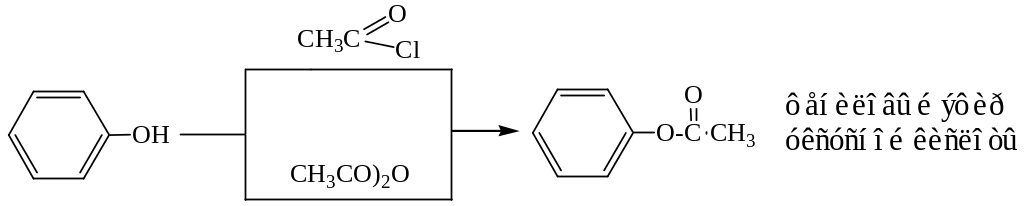
Реакции ароматического ядра.
Гидроксильная группа оказывает большое влияние на ароматическое ядро, увеличивая его реакционную способность в о- и п-положениях. Поэтому фенол легко вступает в реакции электрофильного замещения.
При сульфировании фенола при комнатной температуре образуется смесь о- и п-изомеров.
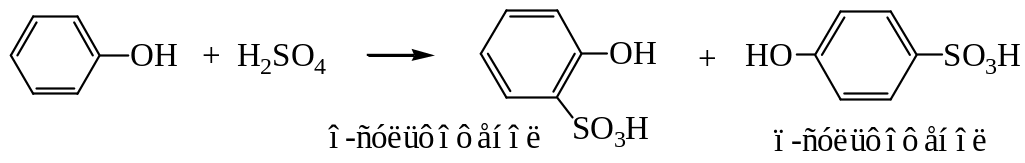
, Благодаря активирующему действию гидроксильной группы, при бромировании и нитровании фенола концентрированной азотной кислотой, реакция идет одновременно в о- и п-положения.