
- •Методическое пособие для студентов нехимических специальностей заочного отделения
- •Подготовлено к печати на кафедре органической химии
- •Редактор
- •1. Введение
- •Свойства ковалентной связи.
- •Понятие об индуктивном и мезомерном эффектах
- •Классификация органических реагентов и реакций.
- •2. Номенклатура органических соединений
- •3. Углеводороды
- •3.1. Алканы (предельные, насыщенные углеводороды)
- •3.1.1. Методы получения алканов.
- •3.1.2. Химические свойства алканов
- •Реакции замещения
- •3.2 Циклоалканы
- •Непредельные или ненасыщенные углеводороды
- •3.3 Алкены
- •3.3.1.Методы получения
- •3.3.2.Химические свойства алкенов
- •3.4. Алкадиены.
- •3.5. Алкины.
- •3.5.1.Химические свойства алкинов
- •Как и в случае алкенов реакция идет в присутствии катализаторов (Pt, Pd, Ni и др.) и может быть остановлена на стадии образования алкена.
- •3.6. Реакция полимеризации алкенов и алкадиенов (синтез высокомолекулярных соединений).
- •4. Функциональные производные углеводородов.
- •4.1. Галогенопроизводные.
- •4.1.1. Методы получения и химические свойства галогенопроизводных.
- •5. Кислородосодержащие соединения.
- •5.1. Алканолы (спирты).
- •5.1.1 . Получение спиртов.
- •5.1.2. Химические свойства спиртов.
- •Реакция со щелочными металлами
- •5.2. Альдегиды, кетоны, карбоновые кислоты.
- •5.2.1. Методы получения альдегидов, кетонов, карбоновых кислот.
- •5.2.2. Химические свойства альдегидов и кетонов.
- •5.2.3. Химические свойства карбоновых кислот
- •6. Азотосодержащие производные углеводородов
- •6.1. Алифатические нитросоединения.
- •6.2. Алифатические амины.
- •6.2.1. Химические свойства аминов
- •Основные свойства
- •6.3. Аминокислоты и их производные.
- •6.3.1. Полиамидные волокна.
- •7. Изомерия органических соединений
- •Структурная изомерия
- •Пространственная изомерия
- •8. Сахариды (углеводы)
- •8.1.Моносахариды
- •8.1.1 Строение, изомерия
- •8.1.2. Химические свойства моносахаридов
- •8.2. Полисахариды
- •9. Арены. Ароматические углеводороды и их производные.
- •9.1. Бензол и его производные. Строение, изомерия.
- •9.1.1. Методы получения углеводородов ряда бензола.
- •9.1.2. Химические свойства углеводородов ряда бензола.
- •Электрофильное замещение.
- •Влияние заместителей в бензольном ядре на реакцию электрофильного замещения.
- •9.3. Ароматические амины.
- •9.3.1. Химические свойства аминов
- •Реакции аминогруппы.
- •Реакции ароматического ядра.
- •9.4. Ароматические азо- и диазосоединения. Азокрасители.
- •9.4.1. Химические свойства солей диазония
- •Реакции с выделением азота.
- •Реакции без выделения азота.
- •Контрольная работа №1.
- •Вариант №1
- •Контрольная работа № 2.
- •Содержание
- •1. Введение…………………………………………….……………...3
6. Азотосодержащие производные углеводородов
6.1. Алифатические нитросоединения.
Нитросоединения – производные алканов, в которых атомы водорода (один или несколько) замещены на нитрогруппу (см. гл. 3.1).
В зависимости от типа атома углерода, с которым связана нитрогруппа, различают первичные (I), вторичные (II) и третичные (III) нитросоединения.
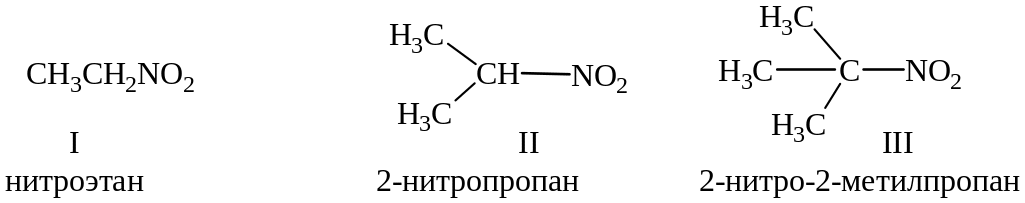
Основной метод получения нитроалканов – парофазное нитрование (см. гл. 3.1).
Нитрогруппа легко восстанавливается многими восстановителями, превращаясь в аминогруппу, т.е. нитросоединения переходят в соответствующие амины.
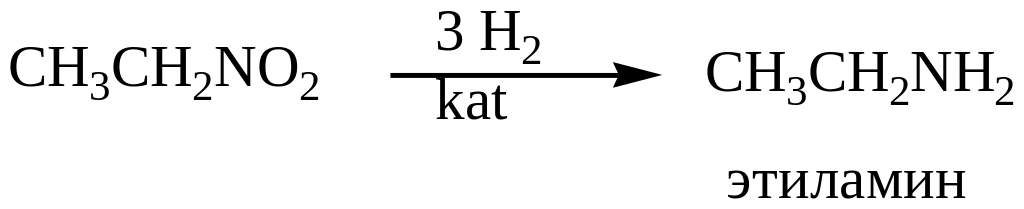
6.2. Алифатические амины.
Амины можно рассматривать как соединения, образующиеся в результате замещения водородных атомов в аммиаке алкильными радикалами.
В зависимости от того, сколько атомов водорода замещено радикалами, различают амины: первичные RNH2, вторичные R2NH, третичные R3N.
По систематической номенклатуре названия аминов образуются добавлением суффикса – амин к соответствующему радикалу.
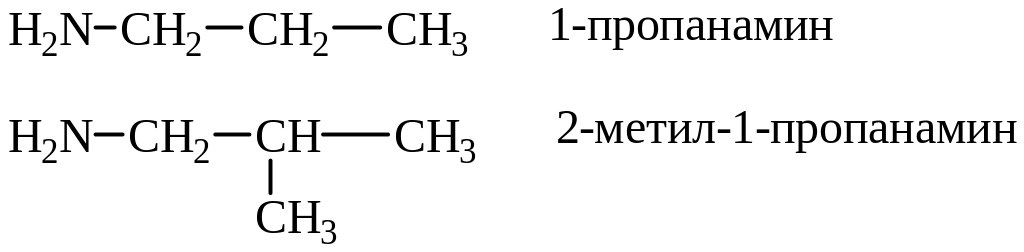
6.2.1. Химические свойства аминов
По химическим свойствам амины сходны с аммиаком.
Основные свойства
Взаимодействуют с минеральными кислотами с образованием солей, т.е. амины проявляют свойства оснований.
![]()
Алкилирование аминов является замещением атомов водорода на органические радикалы.
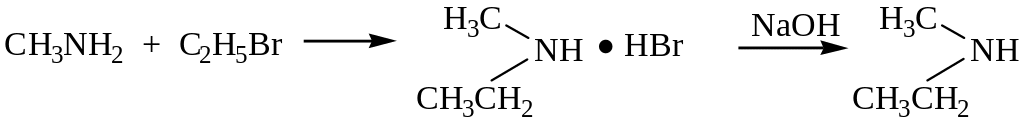
Ацилирование аминов (взаимодействие с ангидридами и галогенангидридами карбоновых кислот) также замещение атомов водорода, но на ацильный радикал.
![]()
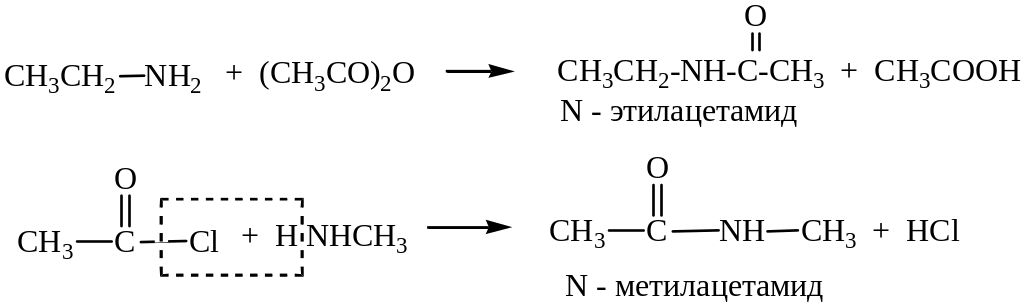
6.3. Аминокислоты и их производные.
Аминокислоты – органические соединения, содержащие в молекуле карбоксильную и аминогруппу. Аминокислоты имеют огромное значение, т.к. из остатков аминокислот построены белковые вещества.
Аминокислоты называют как замещенные соответствующих карбоновых кислот.
Аминокислоты проявляют свойства и кислот и аминов, в ряде превращений сказывается взаимное влияние двух функциональных групп. Прежде всего, это сказывается на свойствах самих аминокислот в растворах.
Так как в аминокислотах есть две функциональные группы, одна из которых (карбоксильная) обладает кислотными свойствами, а другая (аминогруппа) – основными, то в растворах эти группы взаимодействуют, образуя ион (биполярный), так называемую внутреннюю соль – биполярный ион.
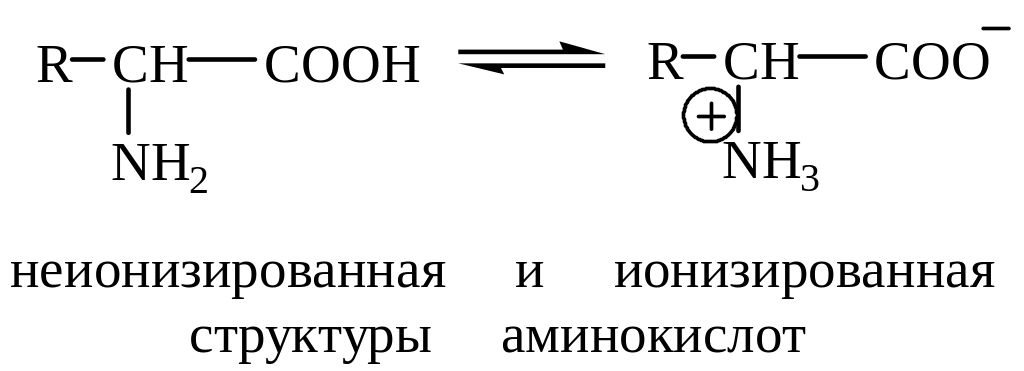
Значение рН раствора, при котором положительный и отрицательный заряды в молекуле аминокислоты точно компенсируют друг друга, называют изоэлектрической точкой.
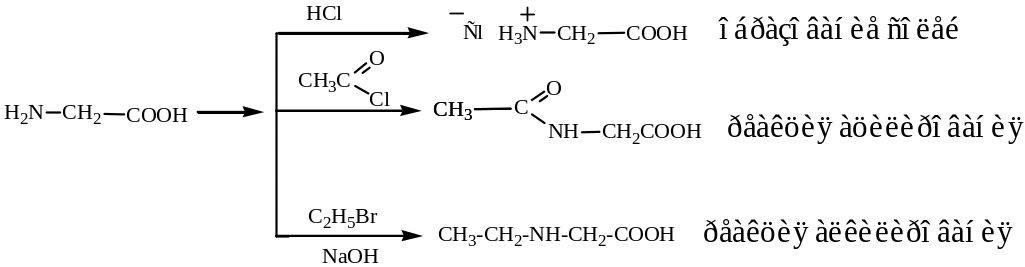
Аминокислоты – соединения со смешанными функциями, в химических превращениях могут проявлять свойства как кислот, так и оснований.
Свойства кислот (см. гл. 5.2)
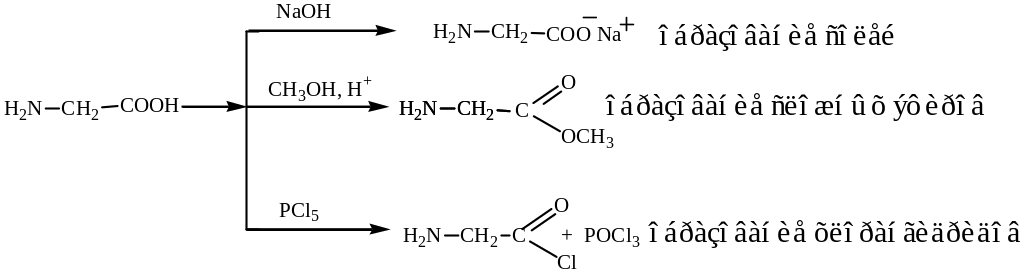
Свойства аминов (см. гл. 6.2)
Аминокислоты являются основной составной частью белков, имеющих общую формулу:
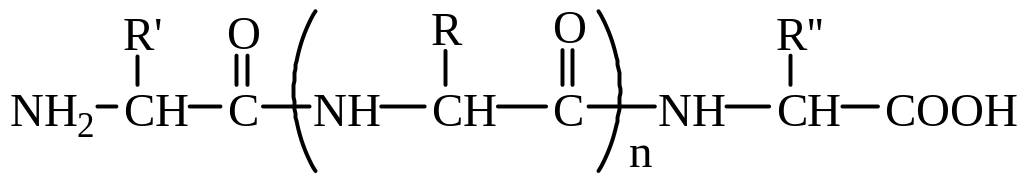
Аминокислоты
связаны между собой в макромолекуле
белка пептидными (амидными) связями
![]() .
.
Если число аминокислот, входящих в состав макромолекулы невелико, то такие низкомолекулярные полимеры называют пептидами. В их составе может быть от двух до 20 аминокислот. В то же время молекулярная масса белков составляет обычно 107 – 108, т.е. это высокомолекулярные соединения.
Роль белков трудно переоценить. Белки – основная составная часть мягкой структуры ткани животных.
Белки (ферменты) – биокатализаторы клеточных реакций.
Белки отвечают за транспорт кислорода в крови и иммунный ответ, контролируют метаболическую активность клетки и т.д.
Белок кератин – основная составная часть шерстяного волокна, а белок фиброин - основа коконовой нити тутового шелкопряда, т.е. шелкового волокна.
