
- •1 Сущность, назначение и классификацияия деструктивных (химических) процессов переработки нефти. Глубина переработки нефти.
- •2 Классификация по назначению
- •2 Особенности технологии химических (деструктивных) процессов переработки нефти. Химические реакции. Скорость химических реакций. Обратимые и необратимые химические реакции.
- •1. Равновесие реакций
- •1. Скорость процессов
- •3 Глубина (степень) превращения сырья в процессах переработки нефти. Способы повышения глубины превращения сырья. Равновесный и фактический выход продуктов процесса. Рециркуляция.
- •4 Понятие о факторах химических процессов технологии топлива. Тепловые эффекты в химических процессах. Назначение и роль технологических факторов в основных результатах процессов.
- •5 Термические процессы переработки углеводородного сырья. Теоретические основы термических процессов. Основные факторы термических процессов.
- •1) Качество сырья
- •2) Температура
- •3) Давление
- •4) Время пребывания в реакционной зоне
- •5) Кратность циркуляции сырья
- •6 Термический крекинг гудрона - технологическая схема двухпечной установки тк. Характеристика сырья, материальный баланс и качество продуктов процесса. Термический крекинг дистиллятного сырья.
- •7 Процесс висбрекинга тно. Разновидности висбрекинга. Технологические схемы. Процесс деструктивно-вакуумной перегонки.
- •8 Сущность процессов коксования нефтяных остатков. Химизм основных реакций углеводородов и факторы процесса. Варианты промышленного осуществления.
- •10 Термоконтактное коксование нефтяных остатков. Принципиальная схема установки. Особенности процессов Флюид-кокинг и Флексикокинг.
- •11 Сущность процесса пиролиза нефтяного и газового сырья. Основные факторы процесса. Характеристика сырья, материальный баланс и качество продуктов процесса. Разновидности процесса.
- •1 Сырьё Любая углеводородная фракция
- •2 Температура и продолжительность процесса (время пребывания сырья в змеевике печи)
- •3 Давление
- •4 Водяной пар
- •12 Принципиальная схема установки пиролиза бензина - эп-300. Примерный материальный баланс процесса, качество продуктов и их применение.
- •3 Давление
- •4 Расход воздуха
- •1 Окислительная колонна – для производства дорожных битумов
- •2 Трубчатый реактор – для производства строительных битумов
- •14 Производство нефтяных пеков. Производство технического углерода.
- •15 Роль и значение термокаталитических процессов переработки нефти в нефтепереработке и в нефтехимии. Основные свойства катализаторов нефтепереработки. Основные стадии каталитических реакций.
- •16 Преимущества каталитических процессов и классификация катализаторов. Требования к катализаторам. Краткая характеристика каталитических реакций.
- •17 Отравление катализаторов и их регенерация. Периодические и непрерывные процессы.
1. Равновесие реакций
- Все реакции обратимы
- Во многих реакциях равновесие смещено полностью в сторону продуктов реакции
Технологические процессы делят на: - Обратимые - Необратимые
Необратимые процессы протекают лишь в одном направлении
Все обратимые процессы стремятся к равновесию (Wпр=Wобр)
-Соотношение компонентов во взаимодействующих системах остается постоянным до изменения параметров технологического процесса (температура, давление, концентрация)
-Влияние основных параметров на равновесие определяется принципом Ле Шателье-Брауна «В системе, выведенной внешним воздействием из состояния равновесия, самопроизвольно происходят изменения, стремящиеся вернуть систему к новому состоянию равновесия»
1. Скорость процессов
С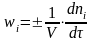 корость
гомогенных реакций Wi
– количество одного из реагентов или
продуктов ni,
прореагировавшее или образовавшееся
в единицу времени в единице реакционного
пространства V
корость
гомогенных реакций Wi
– количество одного из реагентов или
продуктов ni,
прореагировавшее или образовавшееся
в единицу времени в единице реакционного
пространства V
- Скорость химической реакции пропорциональна концентрациям реагентов;
- Суммарная скорость последовательных превращений определяется скоростью наиболее медленной стадии
Температура (технологический параметр) описывается уравнением Аррениуса, где k – константа скорости
Е - энергия активации, это минимальный избыток энергии, который необходим для протекания химической реакции
- В области более низких температур кинетические реакции более чувствительны к изменению температуры
- При изменении температуры скорость
реакции с более высокой энергией
активации меняется в большей степени
При изменении температуры скорость
реакции с более высокой энергией
активации меняется в большей степени
Скорость гетерогенного процесса
Wа – скорость процесса по реагенту А
а- стехиометрический коэффициент реагента А
S – площадь полифазной (реакционной) поверхности
В гомогенных процесса при хорошем перемешивании диффузия протекает очень быстро и не влияет на суммарную скорость
В гетерогенных системах – диффузия самая медленная стадия, определяет общею скорость всего процесса
Способы увеличения скорости процесса
Увеличение константы скорости процесса
Увеличение движущей силы процесса
Увеличение поверхности соприкосновения (контакта) фаз
3 Глубина (степень) превращения сырья в процессах переработки нефти. Способы повышения глубины превращения сырья. Равновесный и фактический выход продуктов процесса. Рециркуляция.
Выход продукта – в зависимости от условий процесса определяется как степень превращения, равновесный выход и фактический выход.
С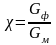 тепень
превращения (степень конверсии)
– отношение
фактически полученного продукта Gф
к максимальному (или теоретическому)
количеству Gм,
которое можно было бы получить их данного
исходного вещества
тепень
превращения (степень конверсии)
– отношение
фактически полученного продукта Gф
к максимальному (или теоретическому)
количеству Gм,
которое можно было бы получить их данного
исходного вещества
Р

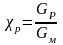 авновесный
выход –
отношение количества основного исходного
вещества, фактически превращенного в
продукт Gр,
к общему его количеству Gм
авновесный
выход –
отношение количества основного исходного
вещества, фактически превращенного в
продукт Gр,
к общему его количеству Gм
Для необратимых процессов Для обратимых процессов
Фактический выход – отношение фактически полученного продукта Gф к его количеству, которое получалось бы в состоянии равновесия Gр (в долях или %)
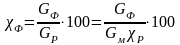
Выход продукта – единственная мера оценки скорости и полноты протекания процесса
Глубина процесса (степень превращения сырья) – характеризуется долей превращенного сырья
« Условно
непревращенное сырье» -
та часть жидких продуктов процесса,
которая выкипает в пределах испарения
исходного сырья
Условно
непревращенное сырье» -
та часть жидких продуктов процесса,
которая выкипает в пределах испарения
исходного сырья
Доля «условно непревращенного сырья»
Процесс с рециркуляцией – процесс, сопровождаемый возвращением «условно непревращенного сырья» в зону реакции
Рециркулят (рисайкл) - «условно непревращенная» часть сырья, которая возвращается в зону реакции
Коэффициент рециркуляции – отношение количества рециркулята к количеству свежего сырья (К)
Коэффициент загрузки – отношение общей загрузки реактора к количеству свежего сырья (К1) К1=К+1
