
Трехфазные системы
Мы рассмотрели поверхностную энергию в системах, состоящих из двух объемных фаз с одной границей раздела (поверхностным слоем). Большой интерес и практическое значение представляют более сложные, а именно трехфазные системы, например, капля жидкости на твердой поверхности или пористое тело, частично заполненное жидкостью. В таких системах сосуществуют три объемные фазы, разделенные и в то же время связанные тремя поверхностными слоями, каждый из которых характеризуется собственным, независимым от других значением (или ). Их соотношение определяет условия сосуществования объемных фаз, в частности условия механического равновесия. От этих величин зависит и поведение жидкости на поверхности твердого тела, — будет ли она растекаться или, наоборот, собираться в капли.
Возможность предвидения этих явлений и управления ими составляет научную основу крашения тканей, гидрофобизации твердых тел, флотации и многих других производственных процессов.
1.3 Смачивание
Рассмотрим сначала качественную картину явления. Если на поверхность твердого тела нанесена капля жидкости, то в такой системе присутствуют три различные поверхности раздела фаз: между твердым телом и газом (ТГ), жидкостью и газом (ЖГ) и твердым телом и жидкостью (ТЖ) с соответствующими натяжениями (ТГ, ЖГ, ТЖ). Линию пересечения всех трех поверхностей раздела называют линией смачивания (замкнутая линия смачивания образует периметр смачивания). Исследуем два различных варианта поведения жидкой капли на твердой поверхности (рис. 4). Пусть в начальный момент капля имеет форму полусферы.
Условие самопроизвольного растекания капли определяется неравенством
ТГ > ТЖ
(при котором замена поверхности с большей свободной энергией на поверхность с меньшей свободной энергией в процессе растекания приведет к уменьшению запаса свободной энергии в системе).
Поскольку в этом процессе увеличивается свободная энергия поверхностного слоя на границе ЖГ, качественное рассмотрение позволяет предсказать возможность остановки процесса (рис. 5а) при значениях
ТГ - ТЖ ЖГ
или неограниченного растекания при
ТГ - ТЖ > ЖГ
а в
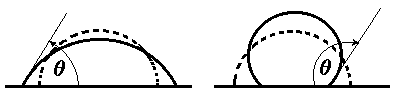
Рис. 5. Растекание капли на твердой поверхности. а – смачивание, в – несмачивание.
Штрихом показано положение капли в начальный момент
Во втором варианте, при
ТГ < ТЖ
очевидно, что уменьшение свободной поверхностной энергии системы S приводит к самопроизвольному уменьшению площади контакта в процессе стягивания капли (рис. 5в).
В первом случае происходит смачивание, а во втором — несмачивание твердого тела жидкостью.
Мерой смачивания является краевой угол (), определяемый как угол между твердой поверхностью и касательной в точке соприкосновения трех фаз. Поскольку этому определению удовлетворяют два угла, условились отсчитывать в сторону жидкой фазы.
В системах типа ТЖ1Ж2 и отсчитывают в сторону более полярной из двух жидких фаз (воды). Очевидно, что в случае смачивания и < 90°, а при несмачивании > 90°.
Таким образом, смачивание (рис. 5), измеряемое величиной зависит от соотношения величин на границах соприкасающихся фаз.
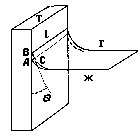
Рис. 6. Схема вывода формулы Юнга для краевого угла |
Для получения количественной связи рассмотрим состояние равновесия для жидкости, смачивающей вертикальную твердую стенку (рис. 6) и химически с ней не взаимодействующую. При бесконечно малом смещении периметра смачивания l вниз на величину АВ = dh затрата работы на увеличение поверхности ТГ составляет (сила · расстояние или сила/длину · площадь) l dh ТГ (*) В то же время энергия системы уменьшается за счет уменьшения поверхностей ТЖ и ЖГ на величину: |
l dh ТЖ + l BC ЖГ или l dh ТЖ + l dh cos ЖГ (**)
В состоянии равновесия изменение свободной энергии dF = 0 и, приравнивая эти выражения (* и **), получаем:
l dh ТГ = l dh ТЖ + l dh cos ЖГ
Или после деления на l dh :
ТГ = ТЖ + cos ЖГ
откуда
![]() (1.18)
(1.18)
Уравнение (1.18), определяющее условия смачивания, — математическое выражение закона Юнга. Анализ его подтверждает следствия, полученные на основе качественных представлений:
ТГ > ТЖ cos > 0 < 90 (смачивание)
ТГ < ТЖ cos < 0 > 90 (несмачивание) (1.19)
ТГ = ТЖ cos = 0 = 90
Поскольку величины ТГ и ТЖ , входящие в уравнение (1.8), обычно неизвестны, целесообразно рассмотреть молекулярные силы и их работу, определяющую значения всех ij , а следовательно и .
а б
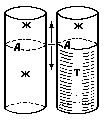
Рис. 7. Иллюстрация понятия когезии и адгезии. |
Назовем силами когезии (слипания) те, которые действуют между молекулами внутри фазы, а адгезии (прилипания) между молекулами, находящимися в разных фазах. В соответствии с этим работа когезии Wc определяется как работа, необходимая для разрыва однородной объемной фазы. Относят ее к единице площади разрыва. Как видно из рис. 7а, эта работа разрыва (в плоскости А) равна Wc = 2 ЖГ (1.20) поскольку при этом образуются две новых поверхности ЖГ. |
Работа адгезии Wa, также относимая к единице площади, определяется как работа разрыва межфазного поверхностного слоя (рис. 7б). Затрачивается она на образование двух новых поверхностей и выигрывается за счет исчезновения свободной энергии исходной межфазной границы. Для системы ТЖ эта работа (рис. 7б) равна:
Wa = ЖГ + ТГ - ТЖ (1.21)
Это выражение называется уравнением Дюпре. Из него вытекает заключение, что межфазное натяжение ТЖ тем меньше, чем больше межфазное взаимодействие на этой границе раздела. Физический смысл этого утверждения заключается в том, что свободная энергия уменьшается за счет работы сил взаимодействия.
Из уравнений (1.18) и (1.20) получаем для работы адгезии следующее выражение:
Wa = ЖГ (1 + cos ) (1.22)
Используя уравнение (1.22), можно вычислить Wa по экспериментально измеренным значениям ЖГ и cos . Оно показывает, что чем больше адгезия, тем больше cos , т.е. смачивание. Таким образом, силы межфазного взаимодействия (адгезионные силы) стремятся растянуть каплю, в то время как силы когезии стягивают каплю до полусферы, препятствуя растеканию, поскольку с ростом знаменателя уравнения (1.18), пропорционального Wc, уменьшается абсолютная величина cos . Уравнение (1.22) позволяет выразить условие смачивания (cos ) в терминах работы. С учетом уравнения (1.20) находим:
Wa > 0,5 Wc (1.23)
Для случая полного несмачивания ( = 180°, cos = -1) уравнение (1.22) дает: Wa = 0. Этот результат не имеет физического смысла, поскольку нельзя представить себе полное отсутствие взаимодействия между двумя соприкасающимися фазами. Действительно, не известны случаи, когда измеренные краевые углы > 150°.
При Wa = Wc и тем более при Wa > Wc растекание становится неограниченным, поскольку = 0, согласно (1.22), и ТГ > ТЖ + ЖГ. Разность Wa – Wc называют коэффициентом растекания.
Уравнения (1.20 - 1.22) позволяют оценить искомую величину и на основании значений параметров Wa и Wc, которые можно всегда связать (хотя бы качественно) с природой фаз, с их полярностью. Так, вода хорошо смачивает стекло, алюмосиликаты, ионные кристаллы и другие поверхности, несущие ионы или образующие их в процессе гидратации. В этих случаях ион-дипольное взаимодействие (Wa) больше диполь-дипольного (Wc). В то же время вода не смачивает парафин и другие неполярные вещества, т.к.у Wc для воды, сильно полярной жидкости, весьма значительна. Гептан, этиловый спирт, бензол и другие жидкости с низкими значениями ЖГ и Wc смачивают практически любую твердую поверхность. Наоборот, ртуть (ЖГ 485 эрг/см2), как правило, не смачивает твердые поверхности, за исключением некоторых металлов.
Р |
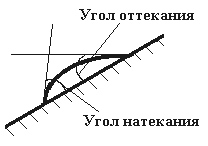
Закономерности смачивания выполняются для всех поверхностях жидкостей только на идеально гладких и однородных поверхностях твердых тел. На поверхности реальных тел обязательно имеются шероховатости (поры, трещины, впадины, выпуклости, загрязнения), которые сказываются на величине измеряемого краевого угла. Также на величину влияет и размер капли. При увеличении капли формируется предельный угол - краевой угол натекания (н), а при ее уменьшении - предельный угол - краевой угол оттекания (от). Наглядная демонстрация этого процесса при наклоне |
пластинки представлена на рис. 8. Эти отклонения от равновесных (истинных) значений
н > от
ист. называются гестерезисом краевого угла. Сравнивая измеренные величины при различных условиях можно оценить загрязнение и шероховатость поверхности:
cos R = R cos ист. (1.24)
где R - реальный краевой угол для данной поверхности,
ист. – краевой угол идеальной поверхности,
R – мера шероховатости (загрязненности).
Для приближенной оценки иногда считают, что равновесный (истинный) угол смачивания равен полусумме предельных углов натекания и оттекания.

 ис.
8.
Формирование краевых углов натекания
и оттекания
ис.
8.
Формирование краевых углов натекания
и оттекания