
- •Навчально-методичний посібник
- •Ужгород–2011
- •Вступ. Предмет колоїдної хімії
- •Тема 1. Поверхневі явища. Адсорбція
- •1.1.Визначення поверхневого натягу і адсорбції поверхнево-активних речовин на межі рідина–повітря
- •Хід роботи
- •1.2.Дослідження поверхневої активності речовин гомологічного ряду
- •Хід роботи
- •1.3.Визначення питомої поверхні вугілля методом вимірювання ізотерм адсорбції поверхнево-активної речовини
- •1.4.Адсорбція оцтової кислоти вугіллям
- •1.5.Вплив адсорбційних шарів на змочування твердих поверхонь
- •Хід роботи
- •1.6. Визначення критичної концентрації міцелоутворення в розчинах пар
- •А) Визначення ккм по поверхневому натягу
- •Хід роботи
- •Б) Кондуктометричне визначення ккм
- •Хід роботи
- •Тема 2. Утворення дисперсних систем
- •2.1.Одержання золей методом заміни розчинника
- •2.1.1.Одержання золю каніфолі
- •2.1.2.Одержання золю сірки
- •2.1.3.Одержання етерозолю хлориду натрію
- •2.2.Одержання золей при проходженні хімічної реакції
- •2.2.1.Одержання золей галогенідів срібла
- •Хід роботи
- •2.2.2.Одержання золю гідрату оксиду заліза (по методу Крекке)
- •2.2.3.Одержання золю гідрату оксиду заліза (по методу Грема)
- •2.3.Одержання золей методом пептизації
- •2.3.1.Одержання золю гідроксиду алюмінію
- •2.3.2.Одержання золю оксиду ванадію (V)
- •2.3.3.Одержання золю сірчистого кадмію
- •2.3.4.Одержання золю берлінської лазурі
- •2.3.5.Одержання золю гідроксиду хрому (III)
- •2.3.6.Одержання золю фосфату алюмінію
- •2.3.7.Одержання золю фосфату заліза
- •2.5.2.Одержання гелю хлориду свинцю
- •2.6.Діаліз розчину желатину
- •Тема 3. Електроповерхневі властивості дисперсних систем з.1.Визначення величини електрокінетичного потенціалу методом електрофорезу
- •3.2.Визначення знаку заряду колоїдної частинки (капілярний аналіз)
- •3.3.Аналіз суміші барвників
- •3.4.Визначення ізоелектричної точки білків
- •3.5.Вплив домішок солей на положення ізоелектричної точки казеїну
- •Тема 4. Стійкість і коагуляція дисперсних систем
- •4.1.Коагуляція колоїдних розчинів електролітами
- •4.2.Визначення порогу коагуляції золів гідроксиду заліза і йодиду срібла
- •Хід роботи
- •4.3.Визначення коагуляції золю каніфолі хлоридом алюмінію (перезарядження золю і неправильні ряди)
- •4.4.Порівняння висолюючої дії електролітів на розчин желатини
- •4.5.Захисна дія желатини
- •Хід роботи
- •Тема 5. Молекулярно-кінетичні та оптичні властивості дисперсних систем
- •5.1.Визначення концентрації золю каніфолі
- •Візуальний нефелометр
- •Хід роботи
- •5.2.Вивчення кінетики утворення золю сірки
- •Хід роботи
- •5.3.Визначення середнього розміру частинок золю нефелометричним методом
- •Хід роботи
- •5.4.Седиментаційний аналіз
- •Хід роботи Методика аналізу на седиментометрі Фігуровського
- •Методика аналізу на торзійних терезах
- •Тема 6. Структуроутворення дисперсних систем
- •6.1.Визначення молекулярної маси полімерів віскозиметричним способом
- •Хід роботи
- •6.2.Вплив нагрівання на в’язкість суспензії крохмалю
- •6.3.Визначення часу тиксотропного застуднівання гелей гідрату оксиду заліза
- •6.4.Набухання гелів
- •Хід роботи
- •6.5.Дослідження швидкості набухання желатини
- •6.6.Утворення кристалів йодиду свинцю в студні кремніевої кислоти
- •Тема 7. Грубодисперсні системи, їх властивості та застосування
- •7.1.Методи визначення фаз в емульсії
- •А) Метод змішування
- •Б) Метод електропровідності
- •В) Метод забарвлення
- •7.2.Приготування емульсії бензолу у воді
- •7.3.Одержання і дослідження емульсій типу м/в та в/м
- •7.4.Одержання розведених емульсій різних масел у воді методом заміни розчинника
- •7.5.Одержання прозорої емульсії гліцерину в оцтовоаміловому ефірі
- •7.6.Тиксотропні властивості емульсій
- •7.7.Дослідження стійкості піни
- •7.8.Визначення “часу життя” крапель на поверхні розділу масло-вода
- •Перелік питань для підготовки до колоквіумів вступ. Предмет колоїдної хімії
- •Тема 1. Поверхневі явища
- •Тема 1. Адсорбція
- •Тема 2. Утворення дисперсних систем. Методи їх очищення
- •Тема 3. Електроповерхневі властивості дисперсних систем
- •Тема 4. Стійкість і коагуляція дисперсних систем
- •Тема 5. Оптичні та молекулярно-кінетичні властивості дисперсних систем
- •Тема 6. Структуроутворення в дисперсних системах
- •Тема 7. Грубодисперсні системи, їх властивості та застосування
- •Рекомендована література
Хід роботи
Скляна ложечка, на яку кладуть пластинки, закріплюють в тримачі за допомогою гвинта. Включають лампу освітлювача, об’єктив приладу переміщують безпосередньо до круглого столика і повертанням кільця оправи об’єктиву одержують різке зображення контурів ложечки на екрані (матовому склі). Підготовлену алюмінієву пластинку кладуть на скляну ложечку і за допомогою встановлюючих гвинтів: круглого і гвинта тримача, який змінює кут нахилу ложечки, знаходять таке положення пластинки, щоб її зображення на екрані мало вигляд різко окресленої горизонтальної лінії, розташованої приблизно посередині екрану. Потім за допомогою піпетки обережно наносять краплину води на поверхню пластинки біля самого краю її, повернутого до екрану. Остаточно регулюють об’єктив для одержання найбільш різкого зображення контурів краплі та пластинки. Звільнивши верхні аретуючі гвинти тримача транспортиру обережно, щоб не пошкодити матового скла, рухають транспортир від руки так, щоб центр його – точка перетину перпендикулярних ліній була зміщена до повного співпадання з вершиною крайового кута на зображенні краплини. Остаточне встановлення здійснюється за допомогою мікрометричних гвинтів - з лівого боку екрану (який переміщує транспортир в горизонтальному положенні) і нижнього, на стелажі екрану (який пересуває весь екран вертикально).
Горизонтальна лінія транспортиру повинна співпадати із зображенням поверхні пластинки і по його конусу роблять перший відлік – 0. Відлік роблять тричі і з них виводять середнє значення 0. Потім транспортир повертають в таке положення, щоб його вертикальна лінія стала б дотичною до зображення поверхні краплі і по конусу транспортиру здійснюють другий відлік (тобто відліки знову повторюють тричі). Різниця середніх значень –0= дає величину крайового кута. Таким же чином визначають крайовий кут на другому боці зображення краплі і з двох його значень (які повинні бути близькими) беруть середнє. Відліки по шкалі транспортира досить брати з точністю до 10. Після вимірювання відразу ж виключають лампу, щоб уникнути її перегрівання. Для невеликих крапель, які помітно не деформуються під дією сили тяжіння, можна визначити крайовий кут, вимірюючи на зображенні краплі на екрані висоту h сегменту і його діаметр. Ці вимірювання здійснюють за допомогою міліметрових шкал, нанесених на обидві перпендикулярні лінії транспортиру. Розрахунки крайового кута в цьому випадку здійснюють таким чином (рис.1.8):
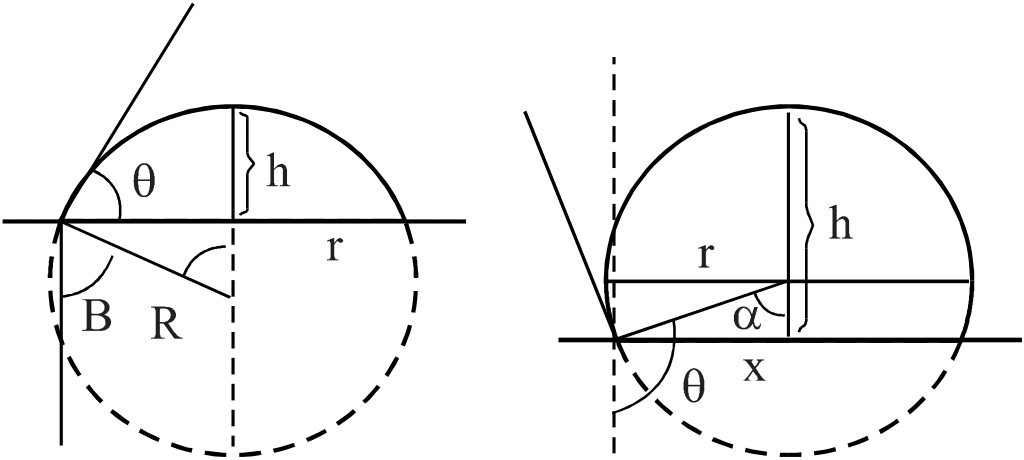
а) б)
Рис.1.8. Схема визначення крайового кута:
а – для кутів 900; б – для кутів 900.
Для кутів 900 (рис.1.8.а), враховуючи, що діаметр рівний 2r:
![]() і
і ![]()
звідки
![]() ;
;
![]() ;
;
![]()
Для кутів 900 , коли крапля не змочує поверхні (рис.1.8.б):
![]()
![]()
![]()
звідки
![]()
Користуючись таблицею тригонометричних величин, знаходять значення та cos.
Якщо вимірювати змочування на межі тверде тіло–крапля, яка знаходиться у повітрі, то в цих умовах часто крапля може утворювати крайовий кут, величина якого не відповідає стану рівноваги. Це явище, яке називається гістерезисом змочування, пояснюється тим, що повітря заважає рідині змочувати тверду поверхню. Для усунення гістерезису змочування методика вимірювання крайового кута іноді видозмінюється так, що досліджувану тверду поверхню занурюють в рідину, яка знаходиться в посудині з плоскопаралельними стінками, і знизу підводять за допомогою піпетки із загнутим капілярним кінцем бульбашку повітря. За цих умов гістерезис практично відсутній, оскільки тверда поверхня до досліду знаходиться в тривалому контакті з рідиною.
Крайовий кут прийнято відраховувати завжди так, щоб дотична була спрямована у водну фазу.
Особливе значення при вимірюваннях крайового кута має чистота пластинок та посуди, оскільки випадкові забруднення дуже змінюють його величину. Тому у всіх дослідах пластинки необхідно брати тільки пінцетом за ребро або кут пластинки. Піпетки при зміні розчину слід кожен раз ретельно промивати.
Суть даної роботи полягає у вивченні впливу адсорбційних дарів на змочуваність алюмінію (тобто гідрофілізація і гідрофобізація поверхні алюмінієвих пластинок) та одержанні “мокрого” парафіну (тобто гідрофілізація парафінових пластинок).
Для виконання першої частини роботи алюмінієві пластинки, вирізані з одного листа металу, вирівнюються пресом і ретельно обезжирюються ватою, змоченою бензолом. Для роботи необхідно відібрати декілька пластинок, які дають крайові кути, що відрізняються не більше, ніж на 4-5°.
Для гідрофілізації поверхні алюмінію готують водні розчини сапоніну слідуючих концентрацій: 0,01; 0,1; 0,5; 1%. Алюмінієві пластинки занурюють на 10–15 хв в розчини сапоніну і тим самим гідрофілізують їх поверхню.
Гідрофілізувча роль сапоніну пояснюється здатністю цієї речовини утворювати при адсорбції на поверхнях гелеподібні сітчаті структури. Утворення таких жорстких структур ускладнює повну орієнтацію всіх багаточисельних полярних груп сапоніну до полярної поверхні алюмінію (покритого оксидною плівкою Al2O3), внаслідок чого поверхня стає достатньо гідрофілізованою за рахунок залишкових неорієнтованих до алюмінію гідроксильних груп. При адсорбції на неполярній (гідрофобній) поверхні молекули сапоніну адсорбуються своїми вуглеводневими частинками.
Гідрофобізацію поверхні алюмінію здійснюють шляхом занурення пластинок в розчини стеаринової кислоти в бензолі. Для досліду готують розчини стеаринової кислоти таких концентрацій: 0,01; 0,1; 0,5; 1%. Алюмінієві пластинки витримують в цих розчинах також протягом 10–15 хв.
Після того, як пластинки, витримані певний час (необхідний для встановлення рівноважної адсорбції) у відповідних розчинах, спочатку пінцетом виймають пластинки, які знаходяться в розчинах сапоніну. Для того, щоб висушити ці пластинки і не пошкодити утворений адсорбційний шар, необхідно їх розташувати похило на скляну паличку, підклавши під них фільтрувальний папір. Після цього виймають пластинки з розчинів стеаринової кислоти і висушують (бензол випаровується швидко). Потім висушені пластинки по черзі поміщають на тримач приладу, наносять на них краплю води (діаметр краплі не повинен перевищувати 2-3 мм) і визначають крайові кути.
Дані всіх вимірювань записують в таблицю і розраховують середнє значення крайового кута для кожної концентрації розчинів:
Речовина |
Концентрація розчину, % |
справа, град |
зліва, град |
середнє, град |
В=cos, град |
Сапонін |
|
|
|
|
|
Стеаринова кислота |
|
|
|
|
|
“Мокрий” парафін |
|
|
|
|
|
На основі одержаних даних будують ізотерми змочування В=f(С).Обидві ізотерми починаються з однієї точки, що відповідає величині В для чистої пластинки, тобто коли концентрація гідрофілізуючого або гідрофобізуючого розчину рівна нулю.
Для виконання другої частини роботи – гідрофілізації парафіну – алюмінієва пластинка занурюється на декілька секунд в розплавлений парафін і виймається з нього обережно пінцетом. На пластинку з парафіновим шаром наносять краплю води і вимірюють крайовий кут змочування. Потім вода замінюється розчинами сапоніну вищевказаних концентрацій. Для кожної концентрації вимірюють крайовий кут. Перед тим, як розпочати вимірювання, необхідно зачекати 5–10 хв., після нанесення краплі розчину сапоніну, для встановлення адсорбційної рівноваги.
Одержані результати зображають також у вигляді ізотерми змочування В=f(С).
Визначають, при якій концентрації поверхнево-активної речовини парафін гідрофілізується, тобто стає “мокрим" і таким чином знаходять точку інверсії.
