
- •2. Обзор литературы
- •2.1. Блок-сополимеры этиленоксида и пропиленоксида
- •Фосфатидилхолин
- •1ДК (набор кислот по отношению к основанию 1)
- •3. Постановка задачи
- •4.2. Методы
- •5. Результаты и их обсуждение
- •5.1.1. Изучение солюбилизующей способности мицелл плюроника р85 и Вгу 35 с помощью флуоресцентной спектроскопии
- •Перилен Нафтохинон
- •0 10 20 30 40 (СБридж35-ккм)-1,%-1
- •5.2. Влияние плюроника на транспорт низкомолекулярных соединений через модельные липидные мембраны
- •5.2.2. Влияние плюроника на мембранный транспорт соединений, не обладающих собственной флуоресценцией
- •Гидроксигиппуровая кислота (нна)
- •200 НМ грамицидина а 5 мкМ валиномицина
- •6. Выводы
61:07-2/573
МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ им. М.В .ЛОМОНОСОВА Химический факультет
Нд правах рукописи УДК 541.(49+64+18)
Бугрин Владимир Сергеевич
СВЯЗЬ МЕЖДУ СТРУКТУРОЙ НИЗКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ И ИХ ВЗАИМОДЕЙСТВИЕМ С ПЛЮРОНИКАМИ
02.00.06 - высокомолекулярные соединения по химическим наукам
ДИССЕРТАЦИЯ на соискание ученой степени кандидата химических наук
Научный руководитель к.х.н. Мелик-Нубаров Н.С.
МОСКВА-2007
СОДЕРЖАНИЕ
Бугрин Владимир Сергеевич 1
(б) 13
(а) 13
мультифаза (везикулы и мицеллы) 13
о 13
"0 5 10 15 20 25 30 35 40 и 2 4 6 8 10 12 Содержание плюроника, % (масс.; Содержание плюроника, % (мах.) 13
рН 77
где /„ - соответствует стационарному уровню, Л1 - амплитуда тушения флуоресценции и £ - константа скорости первого порядка.(а) 120
1 125
Триблок-сополимеры этиленоксида (ЭО) и пропиленоксида (ПО), известные под торговой маркой Пигошсв® (плюроники) или РоЬхатеге® (полоксамеры) [1], представляют собой семейство амфифильных сополимеров, широко востребованных в технологии добычи нефти [2], эмульсионной полимеризации [3], создании моющих средств [4] и т.д. В конце 80-х годов было обнаружено, что плюроники обладают относительно низкой токсичностью. Это открыло широкие перспективы использования этих полимеров в качестве биосовместимых ПАВ [5]. Дальнейшие исследования поведения плюроников в биологическом окружении показали, что они способны усиливать иммунный ответ [6], влиять на метаболизм холестерина [7], ингибировать белковые насосы, обусловливающие множественную лекарственную устойчивость раковых клеток [8-9].
Физиологические эффекты плюроников в основном определяются их взаимодействием с липидными компонентами биологических мембран [9]. Поэтому в настоящей работе было исследовано взаимодействие сополимеров этого класса с модельными липидными структурами. Ранее было показано, что встраивание плюроников в липидные мембраны вызывает уменьшение микровязкости бислоя [10], увеличивает скорость трансбислойной миграции липидов [11] и ускоряет мембранный транспорт противоопухолевого антибиотика доксорубицина [11-13]. Оказалось, что эффект полимеров на перенос лекарств через биологические мембраны зависит как от структуры самого полимера [11, 13], так и от липидного состава мембран [14].
Однако до настоящего времени совершенно не исследованным остается вопрос о том, в какой степени химическая структура переносимого через мембрану вещества влияет на его взаимодействие с плюрониками. Для ответа на этот вопрос на первом этапе настоящей работы была исследована солюбилизация низкомолекулярных соединений в мицеллах плюроника, что позволило получить информацию о силах, участвующих в этом взаимодействии. На втором этапе работы было исследовано влияние плюроника на проникновение слабых кислот и оснований через модельные липидные мембраны, и была проанализирована связь между структурой низкомолекулярных соединений и ускорением их транспорта через липидную мембрану под действием сополимера.
2. Обзор литературы
2.1. Блок-сополимеры этиленоксида и пропиленоксида
(ПЛЮРОНИКИ) 2.1.1. Синтез и применение плюроников
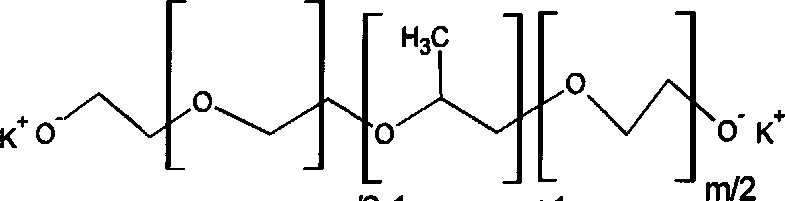
Блок-сополимеры этиленоксида (ЭО) и пропиленоксида (ПО), (плюроники, проксанолы или полоксамеры) - полимеры общей формулы:
НОССНгСНгОЫСНСВДп (СН2СН20)т/2Н ctHs
Обычно коммерческим препаратам плюроников приписывают буквенно- цифровое обозначение, в котором закодирована информация об агрегатном состоянии и составе полимера (табл. 1). Название плюроников состоит из буквы (F, L или Р в зависимости от того, являются ли они твердыми хлопьями (Flakes), жидкими (Liquid) или пастообразными (Paste)) и цифр. Первые 1-2 цифры указывают длину гидрофобного блока полимера, деленную на 5, а последняя - равна массовому процентному содержанию ЭО в молекуле, деленному на 10.
Плюроники были впервые синтезированы в середине 50-х годов с помощью анионной полимеризации пропиленоксида и этиленоксида с раскрытием эпоксидного цикла [15]:
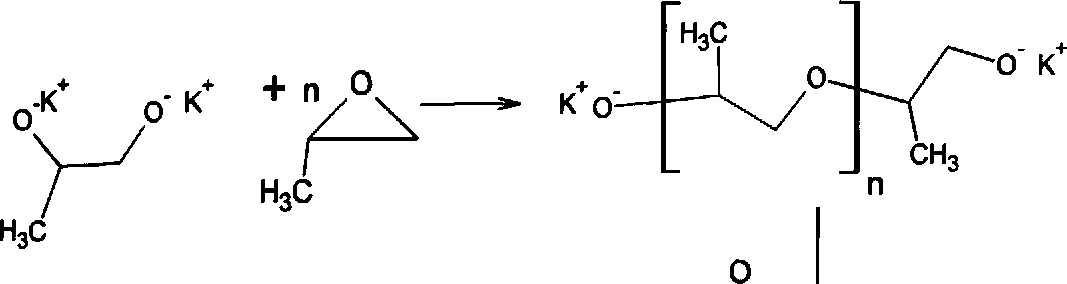
На первой стадии полимеризуют пропиленоксид, используя в качестве инициатора дикалиевую соль 2,3-пропиленгликоля. После исчерпании мономера в реакционную смесь вводят этиленоксид и продолжают полимеризацию в оба конца с образованием трехблочного сополимера типа ABA (А - ЭО, Б - ПО). Простота синтеза этих полимеров и низкая стоимость мономеров стимулировала активные исследования использования этих соединений в различных областях науки и технологии.
Первые исследования свойств плюроников в водных растворах показали, что эти полимеры обладают поверхностно-активными свойствами, причем варьирование соотношеня ЭО/ПО позволяет тонко «настраивать» полимер, для различных сфер применения. Так, полимеры с соотношением ЭО/ПО~1:1 хорошо растворимы в воде, и легко образуют мицеллы. Уменьшение этого соотношения до 0.1 резко снижает их растворимость в воде, однако при этом у плюроников появляется способность к образованию полимерных везикул. Гидрофильные представители семейства плюроников с ЭО/ПО>1 способны стабилизировать эмульсии органических растворителей в воде (эмульсии типа «вода в масле»), а гидрофобные - наоборот, стабилизируют эмульсии воды в органических растворителях (эмульсии типа «вода в масле») [16]. Благодаря таким свойствам плюроники нашли свое применение в качестве эмульгаторов при эмульсионной полимеризации [17], экстракции и разделения биологически-активных соединений [18], создании моющих средств [4] и даже в технологии добычи нефти [2].
Еще в начале 80-х годов было обнаружено, что плюроники обладают довольно низкой токсичностью и поэтому могут использоваться для получения лекарственных форм. Одним из первых применений плюроников в медицине стала эмульсия перфторана (перфтордекалина) в воде, используемая в качестве кровезаменителя. В этом препарате был использован плюроник F68, который характеризуется чрезвычайно низкой токсичностью, но при этом довольно эффективно стабилизирует эмульсию нерастворимых в воде перфторированных углеводородов [19]. Более гидрофобный плюроник L121 также нашел применение в медицине для получения вакцин. Функция этого плюроника состояла не столько в эмульгировании препарата, сколько в образовании крупных коллоидных частиц (полимерных везикул), которые способствовали представлению антигена макрофагам, в результате чего иммунный ответ резко усиливался [20,21].
Дальнейшие исследования взаимодействия плюроников с клетками показали, что некоторые полимеры этого семейства способны облегчать проникновение лекарств через биологические барьеры. Так было обнаружено, что плюроник Р85 облегчает транспорт нейролептиков из кровотока в мозг [22], а плюроники Р85, L61 и ряд других увеличивают накопление лекарств в опухолевых клетках, проявляющих устойчивость к химиотерапии [23]. Лекарственная форма SP1049c, основанная на противоопухолевом антибиотике доксорубицине и двух плюрониках, включая плюроник L61, в настоящее время успешно прошла вторую фазу клинических испытаний, и проявила высокую эффективность в лечении опухолей, проявляющих лекарственную устойчивость.
Широкое использование плюроников для решения различных практических задач требует подробного исследования их способности взаимодействовать с различными соединениями. Ниже мы имеющиеся в литературе данные по взаимодействию плюроников с низкомолекулярными веществами, поверхностями и надмолекулярными ассоциатами в водном растворе.
2.1.2. Взаимодействие плюроников с ионами металлов
Еще в средине 60-х годов было обнаружено, что полиэтиленоксид способен координировать ионы щелочных и щелочно-земельных металлов. Было установлено, что добавление иодида калия к концентрированному раствору полиэтиленоксида в метаноле (2-10 мае. %) приводит к сдвигу полосы поглощения этиленовых протонов в спектре ЯМР почти на 0.05 ррт. Причем кажущаяся константа образования комплекса увеличивалась с ростом молекулярной массы полиэтиленоксида и уменьшалась с увеличением степени заполнения полимерной матрицы ионами металла от 5 М до 0.2 М. [24]. Ионы натрия, по всей видимости, также способны взаимодействовать с полиалкиленоксидами, причем это взаимодействие проявляется даже в водном растворе. Так, введение уже 0.1 М NaCl приводит к снижению температуры гелеобразования плюроника F127 в водном растворе на 5°С, а повышение концентрации хлорида натрия до 0.6 М снижает эту температуру более чем на 15°С. Данный эффект едва ли может быть объяснен высаливающим действием хлорида натрия, поскольку, во-первых, ни ионы натрия, ни хлорид-анионы не проявляют космотропные свойства (и тот и другой ионы находятся в середине рядов Гофмейстера [25]. Во-вторых, указанные эффекты наблюдаются при довольно низкой концентрации соли, когда ее влияние на структуру воды пренебрежимо мало и вряд ли может объяснить изменение агрегатного состояния плюроника. Ионы \л, характеризующиеся еще меньшим ионным радиусом, чем ионы натрия и калия, не взаимодействовали в водном растворе с полиэтиленоксидом. По всей видимости, это обусловлено формированием вблизи этих катионов очень прочной гидратной сферы, которая препятствует координированию иона кислородными атомами полиэтиленоксида [26].
Координация двухвалентных катионов полиалкиленоксидами происходит с заметно большей эффективностью и наблюдается уже в довольно разбавленных
водных растворах полимера (0.001-0.00001%). Так, полиэтиленоксид способен
1+
координировать ионы Щ в водном растворе, причем эти комплексы обладают достаточно высокой стабильностью и формируют гелевую фазу [27]. Аналогично ведут себя комплексы плюроника Ь35 ((ЭО)п(ПО)1б(ЭО)ц) с С<ЗС12. При введении 2 % насыщенного раствора (около 62 мае. %) к жидкому низкомолекулярному плюронику наблюдается образование геля, и формирование нанокристаллов С<Ю2 на полимерной матрице [28].
Комплексообразование полиалкиленоксидов с ионами бария в водном растворе нашло свое применение для высокочувствительного способа анализа полиалкиленоксидов в водных растворах и даже в биологических жидкостях. В
этом случае для повышения чувствительности анализа к разбавленному водному
2+
раствору комплекса Ва с полиалкиленксидами добавляют водный раствор К13. Гидрофобные анионы I3" взаимодействуют с положительно заряженным комплексом полиалкиленоксида и Ва2+, в результате чего комплекс выпадает в осадок и может детектироваться в растворе нефелометрически [29]. Комплексообразование ионов бария с ПЭО в водном растворе было также использовано в создании волюмометрического метода определения полиэтиленоксида, основанного на потенциометрическом титровании комплекса натриевой солью тетрафенилбора [30].
Координирование ионов металлов полиалкиленоксидами объясняет способность плюроников облегчать транспорт малых ионов через липидные мембраны. Известно, что проницаемость мембран по отношению к малым ионам чрезвычайно низка [31]. В работах [32, 33] было обнаружено, что сополимеры этиленоксида и пропиленоксида способны на несколько порядков увеличивать проницаемость липидных мембран по отношению к малым ионам. При этом плюроники обнаруживают катионную селективность: в их присутствии облегчается транспорт именно катионов щелочных и щелочно-земельных металлов, а транспорт анионов не меняется [33].
Таким образом, имеющиеся в литературе данные показывают, что полиалкиленоксиды способны проявлять свойства комплексообразователей, взаимодействуя с катионами металлов. Очевидно, что в этом взаимодействии принимают участие п-электроны атомов кислорода простых эфирных групп, образуя координационные связи с вакантными орбиталями ионов щелочных и щелочно-земельных металлов. Могут ли полиалкиленоксиды образовывать водородные связи с донорами протонов? На этот вопрос мы ответим в следующем разделе.
2.1.3. Взаимодействие полиалкиленоксидов с протонодонорными соединениями.
Взаимодействие полиалкиленоксидов с протонодонорными соединениями ранее изучалось в основном на примере образования комплексов полиэтиленгликолей с поликислотами. В работах В.Ю. Барановского и др. было показано, что при рН<5 полиакриловая и полиметакриловая кислоты образуют нерастворимые комплексы с полиэтиленгликолями, которые растворяются при повышении рН или в избытке одного из полимеров [34]. Было показано, что водородные связи между протонированными карбоксильными группами поликислоты и простыми эфирными группами полиэтиленоксида вносят основной вклад в стабилизацию этих комплексов. Оказалось также, что такие комплексы имеют гидрофобное ядро, которое способно солюбилизовать пирен. При этом резко снижается доля эксимеров пирена, что свидетельствует о торможении диффузии зонда при его включении в интерполимерный комплекс [35]. Введение дополнительных гидрофобных заместителей, таких как ацетоксибензоат [36], 5- нитрохинолинокси-группа [37], производные фенола или окганола [38] усиливает взаимодействие полиэтиленоксида с поликислотами.. Аналогичные закономерности наблюдались и при взаимодействии слабых поликислот с этоксилированными нонилфенолами [39].
Образование комплексов полиэтиленоксида с поликислотами является кооперативным процессом. Установлено, что взаимодействующие полимеры должны иметь достаточно высокую степень полимеризации. При этом критическая степень полимеризации ПЭО, ниже которой он не образует комплексы с полиакриловой и полиметакриловой кислотами составляет 200 и 40 звеньев ЭО соответственно [40]. Показано также, что введение даже небольшого количества неспособных к образованию водородных связей звеньев в молекулу поликислоты может полностью разрушить комплекс.
Формирование комплексов полиэтиленгликоля с поликислотами недавно было использовано для образования полимерных послойных покрытий. Так, покрытие поверхности чередующимися слоями полиэтиленоксида и полиакриловой кислоты позволило получать полимерные пленки, стабильные в водных растворах. Стабильность таких пленок увеличивается в присутствии соли, но резко снижается в щелочной среде [41]. Оказалось, что пленки, полученные по данной технологии обладают проводимостью в присутствии минимальных количеств влаги [42].
Вся имеющаяся в литературе информация касается в основном именно гомополимеров полиэтиленоксида. Склонность плюроников к гидрофобным взаимодействиями и их самоассоциация в водных растворах с образованием мицелл должны способствовать дегидратации и формированию комплексов, стабилизированных водородными связями. В следующем разделе мы рассмотрим закономерности мицеллообразования плюроников и особенности структуры образуемых ими мицелл.
2.1.4. Самоассоциацш плюроников в водных растворах Водные растворы плюроников относятся к системам, характеризующимся нижней критической температурой растворения (НКТР). Это означает, что плюроники растворяются в воде при температурах, ниже некоторого предельного значения, которое и называют НКТР. Понятие НКТР тесно связано с явлением гидрофобной гидратации - формированием ледоподобных кластеров воды на поверхности неполярных фрагментов растворенного соединения. Из теории гидрофобных взаимодействий, развитых ЫешеШу и Scheraga еще в середине 60-х годов, известно, что вклад гидрофобной гидратации в свободную энергию растворенного вещества плавно увеличивается с ростом температуры. Это связано с тем, что с ростом температуры в воде уменьшается количество водородных связей. Поэтому формирование ледоподобных структур в непосредственной близости от неполярных групп становится с ростом температуры все более и более неблагоприятным с точки зрения энтропии фактором.
В случае, если растворенное в воде соединение представляет собой цепную молекулу, обладающую значительной конформационной подвижностью, рост температуры одновременно приводит и к увеличению конформационной энтропии. Поэтому амфифильные полимеры очень часто оказываются растворимы в воде при низких температурах. Однако, в случае, если молекула обладает значительной гибкостью, и при этом, наряду с гидрофильными фрагментами, содержит неполярные группы, увеличение ее конформационной энтропии с ростом температуры может быть не столь резким, как увеличение гидрофобной гидратации, приводящее к уменьшению энтропии системы. Температура, при которой свободные энергии воды и полимерной цепочки становятся равны является 6-температурой. Дальнейшее повышение температуры приводит к тому, что снижение энтропии воды за счет гидрофобной гидратации начинает вносить решающий вклад в свободную энергию системы и полимер резко утрачивает растворимость в воде.
Данная интерпретация явления НКТР является довольно общей. Применительно к полиалкиленоксидам существует и другая альтернативная теория, согласно которой дегидратация этих макромолекул в водном растворе с повышением температуры вызвана различиями гидратации их различных диастереомерных конфигураций. Возможность вращения в молекуле этиленоксида вокруг связей -С-С- и -С-О- приводит к существованию, по меньшей мере, двух возможных конфигурааций каждой связи в полимере - транс или гош. В гош- конформации атомы кислорода находятся по одну сторону от связи -С-С-, а в /ярднс-конформации - по разные стороны. Связь С-С не имеет дипольного момента, а связь С-0 - сильно поляризована, и избыток отрицательного заряда находится на кислороде. В кристаллическом состоянии полиэтиленоксид находится в транс-гош-трагнс-конформацш, причем цепи упаковываются в виде спиралей (длина шага около 7 А). При плавлении или в результате растворения в воде полиэтиленоксид переходит в более полярную гош-гош-трянс-конформацию. При этом, очевидно, гидратация полимера должна увеличиваться.
Расчет электрического потенциала, возникающего вблизи молекулы полиэтиленоксида в транс-гош-транс (тгт) конформации, проведенный в работе [43], показал, что вблизи простых эфирных связей полимера возникает зона с избытком отрицательного заряда, с которой эффективно взаимодействуют молекулы воды, причем с каждым звеном ПЭГ' может взаимодействовать 3-4 молекулы воды. Эти данные прекрасно соответствуют экспериментальным результатам, полученным ВагепЬо1г с сотр. с помощью сканирующей микрокалориметрии, денситометрии и ультразвуковой спектроскопии [44, 45]. Авторам удалось экспериментально показать, что одна цепь полиэтиленоксида с молекулярным весом около 2000 (т.е. 45 звеньев) связывает 136±4 молекул воды, т.е. на каждое звено приходится около 3 молекул воды.
При растворении в воде при комнатной температуре полиэтиленоксид принимает в основном именно ггт-конформацию, в результате чего в этих условиях он сильно гидратирован. Повышение температуры до 100°С нивелирует энергетическое предпочтение ггт-конформации, в результате чего гидратация полимера уменьшается, и он теряет растворимость в воде (т.е. наблюдается НКТР) [46]. При переходе от полиэтиленоксида к полипропиленоксиду, когда к одной из метиленовых групп присоединяется метальная группа, энергетическое предпочтение полярной гг/я-конформации в значительной мере снижается. Вследствие этого НКТР полипропиленоксида оказывается значительно ниже, чем НКТР полиэтиленоксида, и для полимера со степенью полимеризации около 20 составляет 10°С [47].
Таким образом, в области температур выше 10° и ниже 100°С вода является селективным растворителем для сополимеров ЭО и ПО. Поэтому в водных растворах эти сополимеры стремятся образовать надмолекулярные ассоциаты, в которых блоки ППО экранируются от контакта с водой цепями ПЭО. Форма и размер этих ассоциатов зависят от размеров блоков ППО и ПЭО, входящих в макромолекулу.
Из теории упаковки амфифильных соединений известно, что форма надмолекулярных ассоциатов, образуемых в воде амфифильной молекулой, зависит от соотношения объема макромолекулы V, ее длины Ь и площади поверхности полярной части 5. Соотношение У/БЬ носит название критического фактора упаковки. В том случае, если соотношение У/1>1 меньше 0.3, амфифильное соединение образует истинные растворы в воде и не стремится агрегировать. Когда величина У/БЬ составляет 0.3-0.5, соединение образует сферические мицеллы, 0.5-1 - цилиндрические (стержнеобразные) мицеллы, а когда это соотношение превышает 1 - амфифильное вещество проявляет склонность к образованию ламеллярных фаз. Дальнейшее увеличение гидрофобной составляющей вещества может приводить к получению молекул соединений, склонных к образованию обращено-гексагональных фаз (У/8Ь~1.5-2) и кубических фаз (У/8Ь>2). Ламеллярная, гексагональные и кубические фазы представляют собой анизотропные системы, оптические и электрические свойства которых изменяются в зависимости от направления распространения электромагнитных волн [48].
Размеры гидрофобных и гидрофильных блоков в молекулах плюроников изменяется в широких пределах, поэтому их критические параметры упаковки также изменяются от 0.35 - для плюроников серии 'Т", до 2-3 - для плюроников серии "Ь". Так как гидратация пропиленоксида сильно зависит от температуры, то и реальный критический фактор упаковки макромолекул плюроников может зависеть от температуры. Поэтому, в зависимрости от температуры и концентрации плюроники могут образовывать различные надмолекулярные структуры. Например, плюроник Р85 при температуре выше 20°С и концентрации до 20 мае. % образует сферические мицеллы (рис. 1). Нагревание этого раствора до 60°С приводит к образованию цилиндрических мицелл. При повышении концентрации до 30% и температуры - выше 30°С образуется гексагональная фаза, в которой молекулы упакованы в контактирующие друг с другом гидрофобными частями стержнеобразные мицеллы. Дальнейшее повышение температуры концентрированного раствора этого полимера приводит к образованию кубичебской фазы [49].
Плюроник Ь61, значительно более гидрофобный, чем плюроник Р85, не растворяется в воде при концентрации выше 12%. Тем не менее, при температуре ниже 20°С во всем интервале концентраций он не агрегирует. При достижении температуры около 25-30°С в растворе наблюдается образование надмолекулярны
х
ассоциатов, представляющих собой полидисперсную по размерам смесь цилиндрических мицелл и везикул.
Приведенные на рис. 1 фазовые диаграммы показывают, что при температуре выше 30°С плюроники характеризуются довольно низкими критическими концентрациями мицеллообразования (ККМ). При этом увеличение температуры приводит к снижению ККМ, поскольку, как отмечалось выше, при этом уменьшается гидратация полипропиленоксидного блока, а значит, гидрофобность полимера увеличивается. Зависимость параметров мицеллообразования от темпе-
40
35 30 25 20
15 10.
100 80
60
40
20
О
о
ВЫТЯНУТЪЕ
МИЦЕЛЛЫ ¡УБИЧЕСКАЯ
СФЕРИЧЕСКИЕ
МИЦЕЛЛЫ
I ГЕКСАГОНАЛЬНАЯ
(а)
мультифаза (везикулы и мицеллы)
о
о
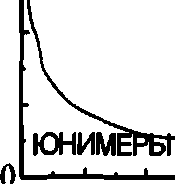
ЮНИМЕРЫ ПЛЮРОНИКА
I . I
"0 5 10 15 20 25 30 35 40 и 2 4 6 8 10 12 Содержание плюроника, % (масс.; Содержание плюроника, % (мах.)
Рис. 1. Фазовые диаграммы плюроников Р85 (а) и L61 (б).
ратуры не характерно для ПАВ, содержащих в гидрофобной части углеводородные радикалы и является отличительной чертой соединений, гидрофобная часть которых содержит гидрофобные полиалкиленоксиды. Критическая температура, ниже которой мицеллы не образуются, т.е. критическая температура мицеллообразования (КТМ), также зависит от концентрации полимера. Для гидрофобных полимеров, серии "L" КТМ резко уменьшается с ростом концентрации. В таблице 1 показаны значения КТМ разных плюроников при концентрации полимеров порядка 1%. В этой же таблице приведены значения ККМ разных плюроников, их состав и молекулярные массы.
Видно, что плюроники обладают довольно низкими значениями ККМ, что говорит об их высокой способности к мицеллообразованию. ККМ плюроников резко уменьшается с ростом длины гидрофобного блока и в значительно меньшей степени зависит от длины гидрофильного блока. Зависимость ККМ плюроников от
их состава описывается эмпирическими корреляционным уравнением, полученным в работах Loh с сотр. для 15 плюроников (коэффициент корреляции 0.93, дисперсия 1.13, критерий Фишера 36.9) [50]:
RTlnKKM = -7,68-0.016n-0,15m. (1)
Согласно этому уравнению, увеличение степени полимеризации и гидрофобного (т), и гидрофильного (п) блоков способствует понижению ККМ, т.е. благоприятствует образованию мицелл. Так же, как и ККМ, КТМ плюроников
|
Таблица 1. Основные характеристики плюроников. Плюроник |
Молекулярный |
Среднее число звеньев |
КТМ, |
ккм,м1 |
%ПЭО |
||||
|
вес1 |
ПО, п2 |
ЭО, т3 |
°С |
(масс.) |
||||
L61 |
2090 |
30 |
4 |
15 |
1.1 X Ю-4 |
10 |
|||
L64 |
2900 |
30 |
26 |
31.5 |
4.8 х Ю-4 |
40 |
|||
L81 |
2750 |
43 |
6 |
14 |
2.3x10° |
10 |
|||
L101 |
3800 |
59 |
9 |
10 |
2.1x10* |
10 |
|||
L121 |
4400 |
68 |
10 |
8 |
1.0 х 10"6 |
10 |
|||
Р84 |
4200 |
43 |
38 |
16 |
7.1 х 10° |
40 |
|||
Р85 |
4500 |
40 |
52 |
29.5 |
6.5 х Ю-0 |
50 |
|||
Р105 |
6500 |
56 |
74 |
21.7 |
8.1x10* |
50 |
|||
F68 |
8400 |
30 |
153 |
45 |
4.8 х 10"4 |
80 |
|||
F87 |
7700 |
40 |
122 |
40 |
9.1x10° |
70 |
|||
F108 |
14600 |
50 |
265 |
30 |
2.2x10° |
80 |
|||
F127 |
12600 |
65 |
200 |
22 |
2.8x10"0 |
70 |
|||
уменьшается с увеличением количества звеньев ПО, что говорит о том, что плюроники с более длинным гидрофобным фрагментом образуют мицеллы при более низких температурах. В то же время, влияние длины гидрофильного полиэтиленоксидного блока на критические параметры мицеллобразования оказалось менее выражено. При постоянной длине полипропиленоксидного блока увеличение длины блоков полиэтиленоксида приводит к незначительному возрастанию ККМ и КТМ. Это означает, что длина полипропиленоксида является
решающим фактором в процессе мицеллобразования. Показано также [53, 54], что при постоянном соотношении пропиленоксид/этиленоксид в составе сополимера, увеличение молекулярной массы плюроника приводит к уменьшению ККМ и КТМ. То есть, высокомолекулярные плюроники в большей степени склонны к образованию мицелл в водных растворах.
При
этом в гидрофильной опушке оказывается
некоторое количество пропиленоксидных
звеньев, а в гидрофобном ядре - содержатся
этиленоксидные
Рис.
2. Зависимость объемной доли звеньев
ППО, ПЭО и воды в мицеллах плюроника
(30 масс. % ППО) от номера концентрического
слоя.
звенья. Содержание воды в гидрофобном ядре постепенно снижается от опушки к центру, причем внутренняя часть ядра практически не гидратирована. Однако общее содержание воды в гидрофобном ядре мицеллы может быть довольно высоким (10-15 моль- %), то есть даже при температуре выше КТМ не происходит полной дегидратации полипропиленоксида [61].
Полярность внутренней среды мицелл плюроников была изучена с помощью исследования флуоресценции гидрофобного пиридиний-Ы-феноксид-бетаинового красителя БрЗО (краситель Рейнхардта). Длина волны флуоресценции этого красителя сильно зависит от полярности его микроокружения, и изменяется от 453 нм в водном окружении до 853 нм в дифениловом эфире. При включении в липидный бислой максимум флуоресценции ЕтЗО составляет около 530 нм. Исследование полярности внутренней среды мицелл плюроников с помощью этого красителя показало, что плюроники могут быть разделены на 3 группы. В первую группу, в которой гидрофобность внутренней среды мицелл относительно невысокая (Ямакс~ 480-5 Юнм) попадают либо те плюроники, у которых длина полипропиленоксидного блока маленькая (15-20 звеньев пропиленоксида), либо они содержат большой этиленоксидный блок (Ь31, Р68). Ко второй группе, соответствующей А,макс~ 530-540 нм, относятся плюроники, содержащие 30-40 звеньев пропиленоксида и различное количество полиэтиленоксида. В третьей группе (Хмакс 550-560 нм) - плюроники с 45-50 звеньями полипропиленоксида (Р94, Р103). Т.е. полярность внутренней среды мицелл сильно зависит от длины и гидрофобного, и гидрофильного блоков [50].
Ет30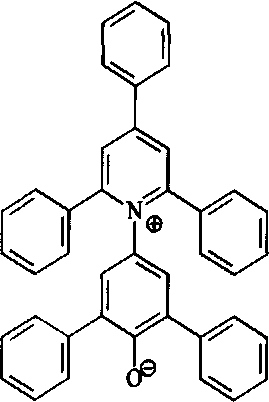
метальных групп, находящихся в гидратированном состоянии, хотя эта доля уменьшается с ростом температуры [62].
Распределение гидратной воды в мицеллах плюроииков было изучено также методом спиновых зондов [63]. Оказалось, что опушка этиленоксида в мицеллах плюроника Р85 сильно гидратирована, однако содержание гидратной воды снижается по направлению к ядру мицеллы. С увеличением температурры наблюдалось уменьшение полярности мицеллы, по всей видимости, за счет перехода ППО и в неполярную тг/я-конфрмацию.
Размер мицелл плюроников, а значит и число агрегации (количество макромолекул в одной мицелле), сильно зависят от их молекулярного веса. Так, по данным малоуглового светорассеяния, при 45°С число агрегации мицелл плюроника L44 (ЕОюРОгзЕОю) составляет 18, плюроника Р84 (ЕО19РО43ЕО19) - 65, а плюроника Р105 (ЕО27РО61ЕО27) - 85 [64]. Число агрегации мицелл плюроников обычно увеличивается с ростом температуры. Например, диаметр мицелл плюроника Р84 изменяется от 10.5 нм при 35°С до 11.8 нм - при 55°С, что соответствует увеличению числа агрегации от 44 до 80. [64]. В некоторых случаях доказано формирование цилиндрических мицелл, которое предшествует образованию ламеллярных, гексагональных или кубических мезофаз [65]. Плюроники L121 и Р123 вместо мицелл образуют бислойные везикулы, имеющие полости, заполненные водой [66-69].
Способность блок-сополимеров этиленоксида и пропиленоксида образовывать мицеллы сильно зависит от расположения блоков в молекуле сополимера (архитектуры макромолекулы) [70]. Методом малоуглового светорассеяния было показано, что двублочные сополимеры характеризуются значительно меньшим значением ККМ, чем трехблочные сополимеры строения ЕОп/гРОщЕОд/г. При этом числа агрегации для мицелл двухблочных полимеров были почти на порядок выше, чем для мицелл трехблочных сополимеров того же состава. Интересно, что сополимеры обращенного строения РОщ/гЕОдРОт/г обладали ещё более низкой способностью к мицеллообразованию, чем сополимеры архитектуры ЕОп/гРОщЕОп/г. По всей видимости, этот факт указывает на важность топологии укладки цепей для формирования мицеллярных структур.
17
о

микровязкости мицелл с
помощью гидрофобного производного
пирена (дипима) показало, что микровязкость
мицелл несколько меньше микровязкости
макрофазы ППО,
Дипим однако существенно превышает микровязкость гидрофоб
ного ядра мицелл обычных ПАВ, ядро которых состоит из углеводородных радикалов. Увеличение степени полимеризации ППО приблизительно в одинаковой степени увеличивает микровязкость объемного ППО и гидрофобного ядра мицелл плюроников.
Повышение температуры приводит к снижению микровязкости мицелл плюроника, однако, это не столь значительное снижение, как в случае макрофазы ППО. Поэтому при повышенной температуре микровязкость мицелл даже превышает микровязкость чистого ППО. Этот факт указывает на то, что с ростом температуры происходит компактизация мицелл, в результате чего микровязкость снижается не столь резко, как в случае объемной фазы, не испытывающей воздействия окружающей водной фазы. Данный вывод был также подтвержден с помощью ЯМР-спектроскопии. Повышение температуры уширяло полосу поглощения ППО, не изменяя время спин-решеточной релаксации. При этом полоса поглощения ПЭО оставалась достаточно узкой, а время спин-решеточной релаксации монотонно возрастало с ростом температуры [71]. В полученном эффекте ярко проявляется полимерная природа внутреннего ядра мицелл плюроников. Таким образом мицелла может быть представлена как жидкая, но вязкая полимерная частица, по своей границе декорированная гидрофильным полимером.
Естественно, что взаимодействие липофильных соединений с такими частицами приводит к солюбилизации, т.е. переходу частиц из водной фазы в ядро мицеллы.
К количественным характеристикам солюбилизации относятся: 1) относительная солюбилизация s, равная отношению числа молей , солюбилизованного вещества Ncon к числу молей ПАВ, находящихся в мицеллярном состоянии NMU1f: s=NC0JNMUH. Рассматривая систему при наличии избытка солюбилизируемого вещества, можно записать [59]
:
ЛЯ
Бугрин Владимир Сергеевич 1
(б) 13
(а) 13
мультифаза (везикулы и мицеллы) 13
о 13
"0 5 10 15 20 25 30 35 40 и 2 4 6 8 10 12 Содержание плюроника, % (масс.; Содержание плюроника, % (мах.) 13
рН 77
где /„ - соответствует стационарному уровню, Л1 - амплитуда тушения флуоресценции и £ - константа скорости первого порядка.(а) 120
1 125
4) термодинамический коэффициент распределения, используется достаточно редко. Так, для изучения солюбилизации летучих органических соединений [73] использовали коэффициент, определяемый как:
К,=ХШ/С!1, (5)
где Хм - молярная доля вещества, солюбилизированного
в мицеллах, а С5/ — его концентрация в воде, в моль/л, К$ имеет размерность л/моль.
Методы изучения солюбилизации. Как правило, изучение солюбилизации состоит в измерении одного из параметров солюбилизации и расчета коэффициента распределения. Для этого необходимо в состоянии равновесия определить концентрацию вещества в мицеллах, и концентрацию несвязанного с мицеллами соединения. Методика определения концентрации вещества в мицеллах выбирается с учетом того, как изменяются характеристики солюбилизуемого вещества при переходе из водной фазы в ядро мицелл.
Наиболее распространенным методом определения коэффициента распределения является флуоресцентная спектроскопия. Флуоресцентные характеристики веществ сильно зависят от полярности (диэлектрической проницаемости) растворителя, что в общем случае описывается уравнением
Липперта. Данный закон
связывает потери энергии флуорофора
с коэффициентом преломления
п и
диэлектрической постоянной среды
е:
![]()
где к - постоянная Планка, с - скорость света, а - радиус полости, занимаемой флуорофором, (//*—//) - изменение дипольного момента при возбуждении, УаИ
- волновые числа поглощения и эмиссии в см'1, соответственно [74]. Как следует
из этого уравнения, при уменьшении полярности растворителя, энергетические потери при возбувдении флуорофора уменьшаются, и квантовый выход флуоресценции увеличивается. Именно это и наблюдается при солюбилизации полиядерных ароматических углеводородов, таких как нафталин, пирен, перилен и других в мицеллах плюроников.
Зависимость интенсивности флуоресценции вещества от концентрации плюроника выходит на насыщение в области больших концентраций. Приняв тогда, что при насыщении весь флуорофор находится в мицеллах, из этой зависимости можно получить соотношение концентраций вещества в мицеллах и воде и рассчитать коэффициент распределения Р [52].
Иногда для определения концентрации связанного с мицеллами вещества используют тушение флуоресценции свободного флуорофора, для чего используют СиБ04 и ВГ [75]. Помимо флуоресценции, можно использовать ЯМР- спектроскопию [76], изменение химических сдвигов также характеризует полярность микроокружения исследуемого вещества.
Для определения коэффициента распределения Р по данным, основанным на флуоресценции, необходимо знать зависимость объемной доли мицеллярной фазы в растворе <9 от концентрации [72]. Эта зависимость определяется выражением 0 = 0.01 (С-ККМ)у, где С - концентрация плюроника в %, а у- парциальный удельный объем мицелл, который является термодинамическим параметром [77] и выражается как:
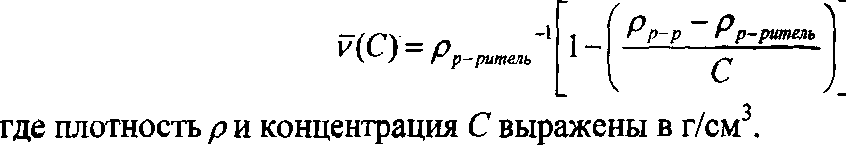
С другой стороны, измерение коэффициента распределения К (см. выше), основанного на молярных соотношениях, а не локальных концентрациях, как Р, может быть проведено без учета объемной доли мицелл. Авторы работы [73] успешно применили параметр К для изучения связывания низкомолекулярных ароматических соединений - бензола, толуола, «-ксилола с мицеллами плюроников. Все изученные соединения были летучими, это позволило легко определить концентрацию их паров над раствором плюроника с помощью газовой хроматографии. Далее, на основании закона Генри и уравнения материального баланса было рассчитано количество вещества в воде и в мицеллах, из чего были полученны значения К. Оказалось, что наибольшие коэффициенты распределения наблюдались для гидрофобных плюроников, имеющих при этом наибольшую молекулярную массу, таких как Р103 и Р123. Сохранение неизменной длины ПЭО блока и увеличение ППО блока приводило к увеличению солюбилизации. В то же время, наоборот, при постоянном блоке ППО увеличение числа ЭО звеньев в гидрофильном фрагменте вызывает уменьшение солюбилизации. Также было показано влияние больших концентраций (от 10" М и выше) солюбилизуемого соединения на структуру мицелл. Так, по предположению авторов, в гидрофобном ядре мицелл имеется значительное количество воды, которая вытесняется при солюбилизации ароматических соединений. В то же время вопрос о присутствии воды оставлен открытым, и предлагается разработать эксприментальный метод (возможно, основанный на ЯМР спектроскопии) для измерения содержания воды в ядрах мицеллы.
Помимо этого, в литературе есть указания [78] на еще одну возможность изучения коэффициентов распределения низкомолекулярных веществ в коллоидных системах. Было предложено осуществлять это путем измерения скорости диализа этих веществ из коллоидного раствора, содержащего эти вещества, в воду через полупроницаемую мембрану.
Для определения коэффициентов распределения в последнее время широко используются мицеллярная электрокинетическая хроматография и капиллярный электрофорез. Методы основаны на увеличении подвижности низкомолекулярных соединений в электрическом поле при их солюбилизации в мицеллах. Следует отметить, что соединения движутся по капилляру тем медленнее, чем больше их коэффициенты распределения между водой и мицеллами. Измерения времен удерживания веществ при различных концентрациях ПАВ в растворе дает возможность определить коэффициенты распределения веществ между водой и мицеллами ПАВ [79].
Влияние природы солюбилизуемого вещества и структуры полимера на коэффициент распределения. Солюбилизация полициклических углеводородов в мицеллах была исследована с помощью проточной системы, основанной на прокачивании водного раствора плюроника известной концентрации через пористый носитель, покрытый слоем солюбилизуемого соединения [80]. Оказалось, что способность полимеров солюбилизовать полициклические углеводороды росла с увеличением длины гидрофобного блока и молекулярной массы плюроника. Мицеллы линейных трехблочных сополимеров обладали более высокой способностью солюбилизовать полициклические углеводороды, чем разветвленные сополимеры этиленоксида и пропиленоксида ТеШнис®. Основной движущей силой солюбилизации углеводородов, очевидно, были гидрофобные взаимодействия: степень солюбилизации нафталина, фенантрена и пирена хорошо коррелировала с их коэффициентами распределения в системе октанол/вода. [80]. При этом локализация углеводородов в гидрофобном ядре таких мицелл была показана на примере бензола с помощью ЯМР-спектроскопии [71].
Добавление алифатических спиртов к мицеллярному раствору плюроника Р85 приводило к солюбилизации и даже способствовало образованию мицелл полимера при концентрации ниже ККМ [63]. При этом наблюдалась солюбилизация спиртов и различных спиновых зондов.
Исследование солюбилизации алифатических производных флуоресцеина в мицеллах различных плюроников позволило оценить свободную энергию переноса метиленовой группы из воды в мицеллу. Оказалось, что увеличение степени полимеризации гидрофобного блока приводило к заметному уменьшению свободной энергии переноса метилновой группы из воды в мицеллы плюроников. При этом наблюдалась обратная зависимость между ККМ плюроников и их способностью к солюбилизации гидрофобных веществ.
В работе [81] было показано, что полярные взаимодействия могут также играть существенный вклад в солюбилизации низкомолекулярных соединений в мицеллах плюроников.
Таким образом, особенность мицелл плюроников проявляется в их высокой гидратированности и полярности внутреннего ядра. Несмотря на то, что гидрофобные взаимодействия определяют солюбилизацию в мицеллах неполярных соединений, с мицеллами могут взаимодействовать и полярные вещества. В настоящей работе мы исследуем вклады различных типов взаимодействий в солюбилизацию низкомолекулярных веществ в мицеллах плюроников.
2.1.5. Адсорбция плюроников на поверхностях раздела фаз
Поверхностная активность плюроника определяется его амфифильным строением. Вода является хорошим растворителем для ПЭО и плохим - для ППО. Поэтому пюроники адсорбируются на границе раздела фаз вода-воздух, при этом поверхностное натяжение снижается с увеличением количества адсорбированного на поверхности раздела фаз полимера. Исследование изотерм поверхностного натяжения плюроника Е88 показало, что уже при концентрации 10 мкМ поверхностное натяжение водного раствора снижалось до 47 мН/м, а в точке, соответствующей критической концентрации мицеллообразования, уже было равно 37 мН/м. Дальнейшее увеличение концентрации полимера в растворе не приводило к изменению поверхностного натяжения [82], что указывает на неспособность мицелл плюроника адсорбироваться на поверхности раздела фаз. При низких концентрациях плюроника изменение его содержания в растворе не вызывало изменения поверхностного давления, причем такая зависимость наблюдалась в широком концентрационном интервале. При концентрации на порядок ниже ККМ давление начинало резко расти, и достигало нового плато в точке ККМ. При этом площадь, приходящаяся на одно звено ЭО в монослое, зависела от степени полимеризации ПЭО блоков и концентрации полимера в растворе. В области концентраций на 2-3 порядка меньше ККМ для плюроника, содержащего 18 звеньев ЭО, на одно звено приходилась площадь около 9 А2, а для полимера, содержащего 46 звена ЭО, первое плато соответствовало 22 А2 на одно звено ЭО. Увеличение концентрации полимера в растворе приводило к большей плотности посадки полимера на границе раздела фаз, в результате чего площади, приходящиеся на одно звено ЭО, снижались до 6 и 12 А2, соответственно. При этом толщина монослоя увеличивалась лишь незначительно, т.е. уменьшение площади, приходящейся на звено ЭО, происходит, по всей видимости, за счет увеличения плотности адсорбированного полимерного слоя на поверхности раздела фаз [83].
Исследовали эластичность адсорбированного на поверхности раздела фаз полимерного монослоя, заставляя подвижную часть ванны Лэнгмюра колебаться с определенной частотой и измеряя в режиме реального времени поверхностное натяжение с помощью пластинки Вильгельми. Модуль упругости монослоя рассчитывали как отношение амплитуды колебаний поверхностного натяжения к амплитуде площади, приходящейся на молекулу полимера. Оказалось, что в условиях разряженного монослоя модуль упругости полимерной пленки увеличивался с ростом концентрации полимера в растворе и достигал значения, близкого к модулю пленки из полиэтиленоксида. Однако при повышении поверхностного давления выше 10 мН/м модуль упругости монослоя начинал снижаться с ростом поверхностного давления. Этот результат указывает на то, что при достижении определенной предельной плотности монослоя блоки ППО начинают вытесняться с поверхности раздела фаз в водный раствор [84].
Адсорбция плюроников на поверхности раздела фаз наблюдалась также и при их добавлении к заранее сформированному монослою липида на границе вода/воздух. В этом случае добавление плюроника приводило к росту поверхностного давления я. Вызываемое плюроником изменение л линейно снижалась с ростом поверхностного давления, при котором находился монослой в момент добавления полимера. При введении 2х10"5% плюроника Ь61 под монослой липида, находящегося при поверхностном давлении 5 мН/м (разреженный монослой), давление повышалось до 23 мН/м, т.е. на 18 мН/м. В том случае, если шпороник добавлялся под монослой, сжатый до давления 15 мН/м, давление повышалось всего лишь на 5 мН/м. При этом плюроник формировал в монослое домены, заметные при исследовании поверхности с помощью эпифлуоресцентного микроскопа. Интересно, что более гидрофильный плюроник Р68 также увеличивал поверхностное давление, но в меньшей степени, чем плюроник Ш. При этом размер доменов, формируемых плюроником Р68, был заметно меньшим, чем в случае с плюроником Ъ61 [85].
Сжатие монослоя, содержащего липид и плюроник, приводило к вытеснению плюроника в водный раствор [85]. Этот результат хорошо согласуется с упомянутым выше фактом о выдавливании плюроника из полимерного монослоя, сформированного чистым полимером.
Таким образом, данные по адсорбции плюроников на границе раздела вода/воздух хорошо согласуются с его амфифильным строением и показывают способность этих сополимеров к гидрофобным взаимодействиям. Аналогичные закономерности наблюдаются и при взаимодействии плюроников с гидрофобными поверхностями. Так, показано, что плюроники с высокой эффективностью адсорбируются на полистирольных микрочастицах. При этом степень заполнения поверхности плюроником Р108 и толщина образующегося полимерного слоя не зависела от размера полистирольных микросфер [86]. Высокая способность плюроников к сорбции на гидрофобных поверхностях также отмечалась и при их взаимодействии с полисульфоновыми ультрафильтрационными мембранами [87], полиэтилентерефталатными [88] и полиуретановыми пленками [89], поверхностях полиметилметакрилата [90], кремния, обработанного плавиковой кислотой [91] и золота [92].
Плюроники адсорбируются не только на гидрофобных, но и на гидрофильных поверхностях. Так, было обнаружено, что плюроник Б127, взятый в концентрации на порядок ниже ККМ, эффективно адсорбируется на гидрофильной поверхности оксида кремния. При этом толщина полимерного слоя оказывается значительно большей, чем толщина слоя, формируемого на гидрофобных поверхностях в аналогичных условиях. По всей видимости, это вызывается тем, что сорбция полимера в этом случае преимущественно обусловлена образованием водородных связей с гидроксильными группами силиката. В результате происходит концентрирование полимера вблизи гидрофильной поверхности, и его локальная концентрация превышает ККМ. Это приводит к формированию мицелл плюроника вблизи гидрофильной поверхности и толщина образовавшегося полимерного слоя значительно превосходит толщину мономолекулярного слоя плюроника, формируемого на гидрофобных поверхностях [93].
Способность плюроника участвовать в различных типах межмолекулярных взаимодействий проявляется также в их взаимодействии с липидными бислоями. Закономерности адсорбции шпороников на легко деформируемых липидных бислойных мембранах сильно отличаются от явлений, наблюдаемых при адсорбции на твердых поверхностях. В то же время некоторые модельные системы позволяют воспроизводить на твердой подложке некоторые физико-химические особенности липидного бислоя. Так в работе [94] была изучена адсорбция плюроника И127 на липосомах, адсорбированных на золотой пластине. Для этого использовались «кварцевые микровесы». Данный метод основан на обратном пьезоэлектрическом эффекте - способности монокристаллов кварца к деформации при приложении электрического поля. Приложение переменного поля к такому монокристаллу вызывает колебания его поверхности, частота которых сильно зависит от массы колеблющегося элемента. В работе [94] к такому кристаллу присоединяли золотую пластину, покрывали ее слоем липидных везикул, погружали в водный раствор и по изменению частоты колебаний кристалла с высокой точностью измеряли количество адсорбированного из раствора вещества с точностью до нескольких сотен нанограмм. Оказалось, что адсорбция плюроника на монослое таких везикул не подчиняется традиционному уравнению Лэнгмюра, а наилучшим образом описывается изотермой Фрейндлиха, предполагающей адсорбцию на мембране молекулярных ассоциатов плюроника. Максимальная степень заполнения поверхности мембран плюроником оказывается почти такой же, как при его адсорбции на гидрофобной поверхности, однако достигается это плато в области более высоких концентраций полимера. Оказалось также, что промывание пластинки водным буфером приводит к быстрой десорбции плюроника с поверхности, что указывает на слабое взаимодействие полимера с липидным бислоем.
Таким образом, приведенные в настоящем разделе данные свидетельствуют о том, что плюроник способен к гидрофобным взаимодействиям. Это проявляется как при его адсорбции на поверхности твердых материалов, так и при взаимодействии с более эластичными мембранами, прикрепленными к твердой подложке. В следующем разделе мы рассмотрим влияние плюроников на свойства
мембран липидных везикул, не связанных с твердыми материалами, находящимися в водном растворе.
2.1.6. Взаимодействие плюроников с липидными бислоями Встраивание плюроников в липидный бислой впервые было продемонстрировано И.Н. Топчиевой и др. с помощью малоуглового рассеяния рентгеновского излучения. Было показано, что блок ППО заглубляется в гидрофобную область мембраны, а блоки ПЭО экспонируются в водный раствор [95]. Дальнейшее изучение локализации плюроников в липидном бислое было проведено в работе Firestone с сотр. с помощью малоуглового рассеяния синхротронного рентгеновского излучения [96]. В данных работах в качестве моделей липидной мембраны были использованы системы с низким содержанием > воды. В этих условиях димиристоилфосфатидилхолин формирует мультислойные структуры с размером гидрофобной области около 20А и расстоянием между ламеллами 57 А. Добавление плюроников, содержащих 30-50 звеньев ПО в гидрофобном блоке, вызывало значительное увеличение расстояния между ламеллами в мультиламеллярной фазе. Дальнейшее увеличение концентрации плюроника вызывало образование гексагональной фазы, т.е. способствовало полному разрушению ламеллярной структуры. Плюроники, содержащие короткие цепи пропиленоксида (15 звеньев), вообще не встраивались в бислой и не вызывали никаких изменений параметров мультислойной структуры. Интересно, что понижение температуры системы ниже температуры фазового перехода в димиристоилфосфатидилхолина приводило к «выдавливанию» плюроников из бислоя, даже если они были до этого в него встроены. Полученные результаты убедительно свидетельствуют в пользу того, что гидрофобный блок ППО локализуется в гидрофобной области липидной мембраны.
В своей более поздней работе те же авторы показали, что двублочные сополимеры этиленоксида и пропиленоксида еще более эффективно встраиваются в бислой, образуя при этом хорошо упорядоченные ламеллярные фазы. В то же время такие сополимеры, содержащие очень короткий блок полипропиленоксида,
нарушали ламеллярную фазу липида и приводили к образованию неупорядоченных структур [97].
Количественная оценка связывания плюроников с липидными везикулами была проведена с использованием плюроника, меченого атомами трития. Это позволило следить за концентрацией полимера с помощью сцинтилляционного счета. Оказалось, что коэффициент распределения плюроника L61 между водным раствором и липидной мембраной составил 45. Эта величина более чем на порядок меньше коэффициентов распределения ПАВ на основе полиэтиленоксида, содержащих в качестве гидрофобной части углеводородные радикалы. Данный результат свидетельствует о довольно низком сродстве плюроников к липидной мембране и хорошо согласуется с данными Olsson и соавторов, из которых следует низкая термодинамическая совместимость ППО и липидного бислоя [67].
Можно предположить, что вследствие низкой совместимости плюроников и липидного бислоя встраивание этих сополимеров в мембрану приводит к заметному изменению ее свойств. Так, показано, что температура фазового перехода дипальмитоилфосфатидилхолина заметно снижается при его взаимодействии с плюроником [95]. Методом просвечивающей электронной микроскопии было выявленно, что адсорбция плюроников F127, F108, F87 с высоким (более 70%) содержанием полиэтиленоксида на малых моноламеллярных липосомах приводит к изменению их формы и превращает сферические везикулы в бислойные диски. Плюроники Р105 и Р85, содержащие около 50% ПЭО, не вызывали изменения формы липосом, но способствовали уменьшению их размеров [98].
С помощью динамического светорассеяния было показано, что адсорбция плюроников на малых моноламеллярных везикулах приводит к изменению их гидродинамического радиуса и уменьшению £-потенциала. Изменение размера везикул в присутствии плюроника зависело от способа смешения липосом и полимера. Более значительные изменения наблюдались в том случае, если плюроник добавлялся к липиду на стадии приготовления везикул. По всей видимости, в этом случае в бислой удается встроить большие количества полимера, чем в том случае, если плюроник смешивается с предварительно сформированными липосомами [99-101].
Изменение структуры бислоя, сопровождающее встраивание в него плюроников, наблюдалось также и по изменению его микровязкости. Эта характеристика мембраны может бьггь определена из измерений анизотропии флуоресценции мембранных зондов, встроенных в гидрофобную область мембраны [74]. Изменение микровязкости свидетельствует об изменении скорости теплового вращения зонда, следовательно, является мерой упорядоченности мембраны. Встраивание плюроников приводит к существенному уменьшению микровязкости липидного бислоя липидных везикул, микросомальных мембран, выделенных из печени мыши, и мембран живых клеток [10].
Увеличение подвижности липидных молекул в мембране под действием плюроников проявляется также и в ускорении трансбислойной миграции липидов (флип-флопа). Известно, что в отсутствие специфических ферментов флип-флоп является очень медленным процессом. В присутствии плюроников скорость флип- флопа линейно увеличивается с ростом концентрации содержащегося в растворе полимера, причем в ряде случаев степень ускорения движения липидов может возрастать более чем на порядок [102]. Интересно, что моноалкиловые эфиры полиэтиленоксида (Вгу) проявляли значительно меньшую способность ускорять флип-флоп в липидных мембранах, несмотря на то, что сродство этих соединений к мембране значительно больше, чем у плюроников [11]. Способность сополимеров ускорять флип-флоп (\gfy-f) возрастала с увеличением объема их гидрофобного блока (V), а для сополимеров с близким значением этого параметра, увеличивалась , с увеличением общей гидрофобности полимера (1ёР), определяемой как коэффициент распределения в системе вода/гексан. Последний параметр, очевидно, связан со сродством полимера к липидному бислою, тогда как первый - является мерой способности макромолекулы нарушать упаковку липидного бислоя. Было предложено корреляционное уравнение, позволяющее предсказывать способность полимера ускорять флип-флоп на основании данных о его гидрофобности и объеме гидрофобного блока [11]:
Щ/= -1.5 + (0.096 ± 0.019)-1§Р+ (0.08810.012) V- (8)
N=12,11=0.93
Вызываемое шпорониками изменение структуры липидного бислоя проявляются также в увеличении его проницаемости по отношению к слабым кислотам и основаниям [12]. Было также обнаружено, что плюроники ускоряют
29
мембранный транспорт противоопухолевого антибиотика доксорубицина, который является слабым основанием и способен проникать через липидные мембраны в незаряженной форме [11, 102, 103]. В работе [33] методом компенсации внутримембранного поля на плоской липидной мембране был определен коэффициент проницаемости доксорубицина через мембрану в присутствии плюроника. Авторам удалось убедительно показать, что канальный механизм вносит лишь незначительный вклад в общее повышение проницаемости мембраны в присутствии плюроника. На основании полученных результатов был предложен механизм действия плюроников на проницаемость мембран, согласно которому плюроники выступают в качестве переносчиков гидрофильных соединений [33]. Данный механизм непротиворечиво объясняет все экспериментальные данные, имеющиеся в литературе результаты, однако он не позволяет различить: действует ли плюроник как переносчик низкомолекулярных веществ, или его эффект определяется разупорядочиванием мембраны, вызывающее ускорение трансмембранной диффузии.
Поскольку в настоящей работе большое внимание было уделено влиянию плюроника на скорость транспорта низкомолекулярных соединений через липидные бислойные мембраны, в следующем разделе мы рассмотрим некоторые вопросы организации и проницаемости липидного бислоя.
2.2. ЛИПИДНЫЙ ВИСЛОЙ КАК МОДЕЛЬ БИОЛОГИЧЕСКИХ МЕМБРАН 2.2.1. Структура липидного бислоя.
Биологические мембраны играют ключевую роль, как в структурной организации, так и в функционировании живых клеток. Основными компонентами биомембран являются белки и липиды. Важнейшая функция мембранных липидов - формирование бислойного матрикса, с которым взаимодействуют белки. Роль липидного бислоя как структурной основы биологической мембраны делает его удобной модельной системой, а физико-химическое исследование бислоев имеет большое значение для понимания процессов, протекающих в более сложных биологических системах.
Основным компонентом липидной части мембран являются глицерофосфолипиды. Наиболее широко распространенным представителем
глицерофосфолипидов является фосфатидилхолин, общая структурная формула которого представлена на рис. 3. Его полярная головка стоит из фосфохолина, который в нейтральной среде является цвитгер-ионом. Очевидно, что фосфатная группа и сложноэфирные группы глицерина склонны к образованию водородных связей в качестве акцепторов протона. При этом фосфатидилхолин в нейтральной среде не проявляет протонодонорных свойств.
