- •1. Идеальные газы. Закон Менделеева-Клапейрона. Параметры вещества.
- •2. Первый закон термодинамики. Формулировка. Математическое выражение.
- •Частные случаи первого закона термодинамики для изопроцессов
- •Формула кпд теплового двигателя:
- •Цикл Карно для тепловой машины
- •2. 2 Закон термодинамики. Формулировка. Понятие процесса, цикла. Прямые и обратные циклы.
- •4. Условия получения работы в тепловых двигателях.
- •.2.Закон Фурье
- •9.3.Коэффициент теплопроводности
- •Условия однозначности процессов теплообмена, закон Ньютона - Рихмана
- •Дифференциальные уравнения теплопроводности в твердом теле
- •Теплопроводность через однослойную и многослойную плоскую стенки при граничных условиях первого рода
- •15. Уравнение теплового потока через плоскую стенку при граничных условиях первого рода
- •16. Уравнение теплового потока через однослойную цилиндрическую стенку при граничных условиях первого рода
- •17. Уравнение теплового потока через однослойную цилиндрическую стенку при граничных условиях третьего рода
- •18. Уравнение теплового потока через многослойную цилиндрическую стенку при граничных условиях первого рода
- •25) Теплоотдача при кипении.
- •26. Теплоотдача при кипении.
- •27. Теплоотдача при конденсации.
- •28. Теплообменные аппараты. Классификация. Схемы движения сред.
- •1. Теплообменные аппараты.
- •2. Классификация теплообменных аппаратов.
- •29. Основы теплового расчета рекуперативных теплообменников.
4. Условия получения работы в тепловых двигателях.
С древнейших времен люди пользовались энергией топлива для приготовления пищи, обогрева жилища и обработки металлов. Но после появления тепловых двигателей особое значение приобрело применение энергии топлива для приведения в движение различных механизмов. Понятно поэтому, насколько важно знать способы наиболее эффективного использования топлива для совершения работы.
Для использования внутренней энергии тела нужно ее "отнять" у тела. Это можно осуществить двумя способами – в процессе теплопередачи, когда тело отдает некоторое количества теплоты, или при совершении телом работы.
Теплопередачей пользуются, например, в ряде технологических процессов, связанных с нагреванием тел, а также для обогрева помещений за счет внутренней энергии горячего пара или воды. Но наибольшее значение имеет использование внутренней энергии тел для совершения работы.
Механическая работа совершается лишь тогда, когда происходит упорядоченное движение – перемещение тела. Внутренняя же энергия – это энергия беспорядочно движущихся молекул. Следовательно, для того чтобы за счет внутренней энергии совершалась работа, необходимо найти способ, позволяющий преобразовать хаотическое движение молекул в упорядоченное движение какого-либо макроскопического тела. И задача эта весьма непростая. Любое упорядоченное движение тел в реальных условиях (при наличии трения) частично "преобразуется" в беспорядочное движение молекул (тела нагреваются). Обратное же преобразование хаотического движения молекул в упорядоченное требует специальных условий.
Такие условия могут быть созданы, например, при использовании цилиндра с поршнем. Беспорядочное перемещение молекул газа в цилиндре вызывает перемещение поршня. Цилиндр с поршнем составляет главную часть огнестрельного оружия. За счет внутренней энергии газов, возникающих при сгорании топлива (пороха) в стволе (цилиндре) совершается механическая работа по перемещению снаряда. Огнестрельное оружие, таким образом, является своеобразным тепловым двигателем. Но это не есть двигатель непрерывного действия. Тепловая машина, для того чтобы быть периодически действующим устройством, должна совершать замкнутый процесс или цикл.
|
|
(4.38) |
где Q1 – количество теплоты, полученной газом на стадии расширения (участок 1а2), Q2 – количество теплоты, отведенное от газа на стадии сжатия (участок 2б1).
Отношение совершенной за цикл работы А к количеству теплоты Q1, полученному за цикл от нагревателя, называется коэффициентом полезного действия машины.
|
(4.39) |
|
Обязательными составляющими тепловой машины являются два тепловых резервуара: нагреватель с температурой Т1 и холодильник с температуройТ2 < T1. Если просто привести нагреватель в тепловой контакт с холодильником, то внутренняя энергия нагревателя будет передаваться холодильнику путем теплопередачи без совершения работы. Для совершения механической работы обязательно должно быть промежуточное звено – так называемое рабочее тело, в качестве которого, например, может быть использован газ в цилиндре.
Отметим еще, что на первых порах охлаждение газа перед сжатием достигалось путем приведения его в контакт с телами более низкой температуры. Но в этом случае энергия хаотического движения молекул газа преобразуется также в энергию хаотического движения молекул других тел, и для совершения работы она будет потеряна. Вот почему первые тепловые двигатели имели очень низкийк.п.д. (~5 %). Очевидно, нужно было найти другой способ охлаждения газа.
Итак, внутренняя энергия, отнятая у нагретого тела при соприкосновении его с более холодным телом, абсолютно бесполезна для совершения работы. Поэтому, если мы хотим получить максимальную работу при расширении газа, надо чтобы газ в этом процессе не соприкасался с телами, имеющими более низкую температуру.
|
Напомним, что при адиабатном расширении газа его внутренняя энергия уменьшается как раз на величину совершенной работы. При этом происходит понижение температуры. Напротив, при адиабатном сжатии газа его внутренняя энергия увеличивается за счет работы, совершенной над газом, вследствие чего температура газа повышается.
Рассмотрим изменение состояния газа в ходе изотермического процесса при условии, что цилиндр, в котором находится газ, соприкасается теплопроводящим дном с телами такой же, как у него, температуры, которая поддерживается постоянной. Предоставим газу возможность расширяться и совершать работу. Так как работа совершается газом за счет внутренней энергии, его температура начнет понижаться. Но тогда температура источника тепла окажется чуть-чуть выше, чем температура газа, и тотчас же от источника к газу будет передаваться такое количество теплоты, которое приведет к выравниванию температур газа и источника. Отдавать же какое-либо количество теплоты газ не может, так как он не соприкасается с телами более низкой температуры. Таким образом, температура газа практически будет всегда оставаться постоянной, постоянной будет и внутренняя энергия (для идеального газа она есть только функция его температуры). Тогда из первого закона термодинамики следует, что Q = A. Не представляет труда рассмотреть процесс изотермического сжатия газа, в ходе которого за счет работы внешних сил внутренняя энергия и температура газа должны повышаться, что приведет к передаче некоторого количества энергии от рабочего тела термостату.
Итак, в адиабатном и изотермическом процессах наиболее полно используется внутренняя энергия для совершения работы. В этих процессах газ отдает энергию только для совершения работы. Очевидно, что для получения максимальной работы цикл тепловой машины должен состоять из адиабатического и изотермического процессов, поскольку только эти процессы позволяют исключить контакт горячего тела с холодным, то есть исключить уменьшение энергии без совершения работы
5. Условия получения холода в холодильных машинах. ( простите. Но ничего другого не было, информация тупо скопирована с сайта http://www.xumuk.ru/encyklopedia/2/5076.html, частично прочитала) я уверенна,что ему нужен совершенно другой ответ. В учебнике по этому поводу ничего нет
ХОЛОДИЛЬНЫЕ ПРОЦЕССЫ, обеспечивают непрерывное искусств, охлаждение разл. в-в (тел) путем отвода от них теплоты. Естеств. охлаждение с помощью холодной воды или воздуха позволяет охладить в-во до т-ры охлаждающей среды и не требует подвода энергии. Охлаждение до более низких т-р происходит в искусств. холодных средах, на создание к-рых расходуется мех., тепловая или хим. энергия. Охлаждение до т-р выше 120 К принято наз. умеренным, ниже - глубоким или криогенным.
Искусственные холодные среды. Для их получения необходим перенос теплоты с низкого на более высокий температурный уровень, к-рым, как правило, является т-ра окружающей среды. Этот перенос осуществляется с использованием т. наз. обратимых круговых термодинамич. циклов, к-рые в пром-сти обычно реализуются в холодильных установках. В последних холодная среда создается с помощью рабочих тел, наз. холодильными агентами или просто хладагентами (вода, NH3, пропан-пропиленовые смеси, хладоны, сжиженные газы - воздух, N2, Н2, Не и др.). В лаб. практике холодные среды получают, приготовляя т. наз. охлаждающие смеси- системы из двух или неск. твердых (либо твердых и жидких) в-в, при смешении к-рых вследствие поглощения теплоты при плавлении или растворении происходит понижение т-ры. Наиб.употребительны смеси изльда и NaCl (достигаемая т-ра от -20 до - 21,2 °С), льда и СаС12 х 6Н2О (-40 °С), твердого СО2 и этанола (-77 °С) и др. Для достижения криогенных т-р в лабораториях применяют сжиженные газы, напр. N2 (см. также Теплообмен).
Термодинамические основы получения холода. Согласно второму началу термодинамики, указанный выше перенос теплоты самопроизвольно не происходит, требуя затрат работы. В термодинамич. процессах подвод или отвод теплоты q описывается через изменение энтропии dS системы: dq = TdS, где Т - т-ра. Отсюда следует, что при подводе к телу теплоты его энтропия возрастает, а при отводе теплоты -уменьшается. В непрерывных холодильных процессах хладагент должен принять теплоту от охлаждаемого тела на ниж. температурном уровне, отдать теплоту на верх.уровне к.-л. теплоприемнику и вернуться в исходное состояние. Поэтому в установившемся процессе суммарная энтропия хладагента не изменяется (dS=0). Поскольку при передаче теплоты от охлаждаемого тела энтропия хладагента повышается, в любой холодильной установке должен проходить иной (компенсирующий) процесс, при к-ром энтропия хладагента уменьшается. В общем случае энтропия м. б. представлена как ф-ция т-ры и к.-л. другого параметра тела (напр., давление, фазовое состояние, степень намагниченности). Поэтому, если имеется изотермич. или близкий к нему процесс, в к-ром наблюдается значит.изменение энтропии при изменении иного параметра, то подобный процесс можно рассматривать как потенциальную основу для создания холодильных установок. К таким процессам относятся, напр., изотермич. процессы сжатия либо адсорбциигазов, намагничивания парамагнетиков и сверхпроводников. При этом низкая т-ра достигается соотв. в адиабатич. процессах расширения идесорбции газов, размагничивания парамагнетиков и сверхпроводников (см. ниже). Перечисленные и иные процессы искусств.охлаждения в большинстве случаев осуществляются: 1) путем теплообмена между охлаждаемыми в-вами и хладагентами - испаряющимися низкокипящими жидкостями, т-ра к-рых за счет уменьшения энтальпии i понижается до т-ры кипения при давлениииспарения; 2) изоэнтальпийным (i = const) расширением газов, предварительно сжатых в компрессорах, или жидкостей при их прохождении через сужение (вентиль, кран, пористая перегородка), т. е. их дросселированием (процесс протекает адиабатически без совершения внеш. работы) с использованием эффекта Джоуля - Томсона, или дроссельного эффекта,- отрицат. либо положит.изменения т-ры тела при отсутствии подвода к телу или отвода от него теплоты; 3) адиабатическим (изоэнтропийным, S = const) расширением газов с совершением внеш. работы в т. наз.детандерах - машинах, устроенных подобно поршневому компрессору или турбокомпрессору (см. Компрессорные машины); 4) сочетанием обоих методов расширения. Эти и другие методы получения холода рассмотрены ниже.
Принцип
работы холодильных установок. Его
удобно иллюстрировать с помощью
идеального (воображаемого) холодильного
процесса (цикла) в координатах р - V (рис.
1; р, V- давление в
системе и ее объем). При сжатии в
компрессоре (процесс ВbА)рабочего тела
его т-ра Т повышается; при этом в окружающую
среду с
т-рой Т0 передается
удельная (на единицу кол-ва хладагента)
теплота q0 (площадь
AbBdcA)и энтропия рабочего
тела понижается; в конце сжатия Т = Т0.
При послед.расширении (процесс
АаВ)хладагента его
т-ра понижается. Затем к нему от охлаждаемой
среды переносится теплота qx(площадь
AaBdcA)и энтропия рабочего
тела возрастает.
Повторяя указанные
процессы, получают непрерывный круговой
холодильный цикл с постоянной
холодопроиз-водительностьюqx (кол-во
теплоты, отнимаемой от охлаждаемого
тела). Расходуемая в цикле мех.работа
lц (площадь
АаВbА), параметры q0 и
qx по закону
сохранения энергии связаны
между собой выражением: q0 =
qx +
lц.
Энергетич. показатели цикла характеризуются
т. наз. холодильным коэффициентом![]() Во
всех идеальных циклах lц минимальна,
а e максимален.
Во
всех идеальных циклах lц минимальна,
а e максимален.
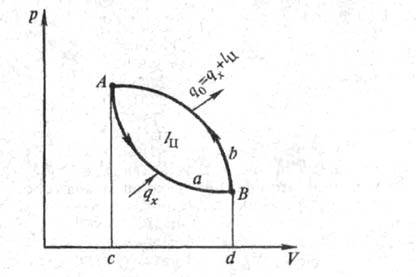
Рис. 1. Идеальный холодильный цикл.
Идеальные холодильные циклы и установки
Термодинамич.
совершенство реального (необратимого)
цикла оценивается сравнением его
параметров с параметрами идеального
(обратимого) цикла. Отношение холодильного
коэф. реального цикла![]() к
холодильномукоэф. соответствующего
идеального цикла
к
холодильномукоэф. соответствующего
идеального цикла![]() наз.
термодинамическим коэффициентом
цикла
наз.
термодинамическим коэффициентом
цикла![]() Известны
схемы и параметры ряда идеальных циклов:
охлаждения, термостатирования, конденсации,
сжижения и др.
Известны
схемы и параметры ряда идеальных циклов:
охлаждения, термостатирования, конденсации,
сжижения и др.
Идеальный цикл охлаждения. Схема установки, работающей по этому циклу, и его изображение в координатах Т -S показаны на рис. 2 (здесь и далее точками 1, 2, 3,..., п обозначены стационарные характерные состояния рабочего тела, а изменения его параметров, отвечающие происходящим в установке процессам, изображены линиями 1-2 и т.д.). Хладагент изотермически сжимается в компрессоре K1 от давления р1 додавления р2(процесс 1-2), при этом теплота сжатия q0 отдается в окружающую среду. Затем происходит адиабатич. расширение рабочего тела вдетандере (процесс 2-3, S = const), где за счет совершения работы lд хладагентом его т-ра понижается до Тx=Т3. В теплообменнике ТО рабочее тело нагревается (процесс 3-4) до т-ры Т4 путем подвода к нему теплоты qxот охлаждаемого тела (процесс 4'-3') и адиабатически сжимается (процесс 4-1) в компрессоре К2 до начальных параметров (точка 1). Процесс в ТО характеризуется отсутствием гидравлич. потерь, а также равенством т-р охлаждаемого и рабочего тел во всех сечениях аппарата. Т-ра охлаждаемого тела уменьшается, а затрачиваемая работа lц = lK1 + lK2 - lд = q0 - qx, где lK1 и lK2 - работы изотермич. и адиабатич. сжатия хладагента в компрессорах.
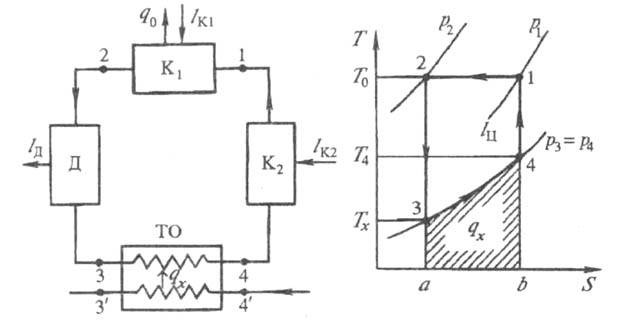
Рис. 2. Идеальный цикл охлаждения.
В тепловых расчетах холодильных циклов удобно использовать связь между изменением энтальпии di хладагента и изменениями его теплоты и рабочих параметров, выражаемую ур-нием: di = dq + Vdp. Отсюда для наиб.распространенного на практике изобарного охлаждения имеем: qx = i4 - i3 и lц = T0(S1 - S2) - (i4 - i3), гдe i3 и i4 - энтальпии рабочего тела. На рис. 2 работе lц эквивалентна площадь 12341, кол-ву отведенной теплоты q0 - площадь 12ab1, кол-ву подведенной к хладагенту или отведенной от охлаждаемого тела теплоты qx - площадь аb43а (здесь и далее заштрихована). В общем случае обратимый процесс 3-4 м. б. не только изобарным, тогда
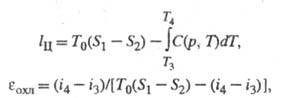
где С - теплоемкость хладагента.

Рис. 3. Идеальный цикл термостатирования.
Этот цикл принимается в качестве идеального для воздушных холодильных, а также криогенных газовых и рефрижераторных установок (см. ниже).
7.Пары. Параметры состояний
Пар — газообразное состояние вещества в условиях, когда газовая фаза может находиться в равновесии с жидкой или твёрдой фазами того же вещества. Процесс возникновения пара из жидкой (твёрдой) фазы называется «парообразованием». Обратный процесс называется конденсация. При низких давлениях и высоких температурах свойства пара приближаются к свойствам идеального газа. В разговорной речи под словом «пар» почти всегда понимают водяной пар. Пары́ прочих веществ оговариваются в явном виде. Не следует путать оптически однородный и гомогенный пар с туманом — гетерогенной системой, сильно рассеивающей свет.
Различают следующие виды состояний пара химически чистых веществ: Ненасыщенный пар — пар, не достигший термодинамического равновесия со своей жидкостью. При данной температуре давление ненасыщенного пара всегда меньше давления насыщенного пара. При наличии над поверхностью жидкости ненасыщенного пара процесс парообразования преобладает над процессом конденсации, и потому жидкости в сосуде с течением времени становится все меньше и меньше.
У разных жидкостей динамическое равновесие с паром наступает при различной плотности пара. Причина этого заключается в различии сил межмолекулярного взаимодействия. В жидкостях, у которых силы межмолекулярного притяжения велики, например у ртути, только наиболее быстрые молекулы, число которых незначительно, могут вылетать из жидкости. Поэтому для таких жидкостей уже при небольшой плотности пара наступает состояние равновесия. У летучих жидкостей с малой силой притяжения молекул, например у эфира, при той же температуре может вылететь за пределы жидкости множество молекул. Поэтому и равновесное состояние наступает только при значительной плотности пара.
Водяной пар — газообразное состояние воды. Не имеет цвета, вкуса и запаха. Содержится в тропосфере.
Образуется молекулами воды при её испарении. При поступлении водяного пара в воздух он, как и все другие газы, создаёт определённое давление, называемое парциальным.[1] Оно выражается в единицах давления — паскалях. Водяной пар может переходить непосредственно в твёрдую фазу — в кристаллы льда. Количество водяного пара в граммах, содержащегося в 1 кубическом метре, называют абсолютной влажностью воздуха.
Так как теплоёмкость пара, вернее теплота его конденсации достаточно велика, он часто используется в качестве эффективного теплоносителя. Как примеры использования можно привести паровое отопление, промышленное использование пара, например, парогенераторы.
Процессы преобразования энергии в различных тепловых машинах осуществляется с помощью вещества, называемого рабочим телом. В качестве рабочих тел могут выступать вещества в жидком, газообразном и твердом состояниях. Они являются «посредниками» в процессе обмена энергией между системой и окружающей средой. Так, например, нагреваемый газ расширяется и совершает механическую работу. В результате происходит преобразование тепловой энергии в механическую.
Рабочее тело характеризуют различные параметры состояния – давление, объем, температура, внутренняя энергия, энтальпия, т.д. В качестве основныхпараметров состояния принимают: удельный объём, абсолютное давление и абсолютную температуру.
Удельным объёмом называется объём единицы массы вещества:
![]() , м3/кг.
, м3/кг.
Масса единицы объёма, т.е. величина обратная удельному объему, называется плотностью:
![]() , кг/м3. Очевидно соотношение:
, кг/м3. Очевидно соотношение: ![]() .
.
Абсолютным давлением называется давление газа, обусловленное совокупностью ударов беспорядочно движущихся молекул о стенки сосуда, в котором заключен газ, и представляет собой нормальную силу F, действующую на единицу площади А поверхности стенки:
![]() , кг/м2 =
Па.
, кг/м2 =
Па.
В системе СИ давление измеряется в паскалях (Па).
Для измерения давления используют приборы: атмосферного – барометры, выше атмосферного – манометры, ниже атмосферного – вакуумметры. Барометр – единственный прибор, измеряющий абсолютное давление атмосферы (ратм). Давление, которое регистрирует манометр или вакуумметр, называют избыточным (ризб). Оно не является параметром состояния рабочего тела, а лишь показывает на сколько давление в сосуде выше или ниже атмосферного. Действительное давление (р) в сосуде (абсолютное) является параметром состояния и равно сумме:
![]() .
.
Величина, характеризующая степень нагретости тела, называется температурой.Степень нагретости тел связана со среднеквадратичной скоростью движения молекул выражением:
![]() ,
где m =
масса молекулы,k –
постоянная Больцмана,Т –
абсолютная температура.
,
где m =
масса молекулы,k –
постоянная Больцмана,Т –
абсолютная температура.
Абсолютная температура
измеряется в
кельвинах (К) и всегда положительна. Абсолютный
нуль – это температура, при
которой прекращается тепловое
движение молекул, т.е. начало
отсчета температуры по шкале Кельвина.
Температура по шкале Кельвина связана с температурой по
шкале Цельсия соотношением:![]() .
.
8.Паровые таблицы и диаграммы
Цикл Ренкина
Теоретическим циклом современной паросиловой установки является цикл Ренкина.
Пароводяная смесь образовавшаяся в результате передачи тепловой энергии воде в активной зоне поступает в Барабан – сепаратор где происходит разделение пара и воды. Пар направляется в паровую турбину, где расширяясь адиабатно, совершает работу. Из турбины отработавший пар направляется в конденсатор. Там происходит отдача теплоты охлаждающей воде, проходящей через конденсатор. Вследствие этого пар полностью конденсируется. Полученный конденсат непрерывно засасывается насосом из конденсатора, сжимается и направляется вновь в барабан сепаратор.
Конденсатор играет двоякую роль в установке: Во-первых, он имеет паровое и водяное пространство, разделенные поверхностью, через которую происходит теплообмен между отработавшим паром и охлаждающей водой. Поэтому конденсат пара может быть использован в качестве идеальной воды, не содержащей растворенных солей. Во-вторых, в конденсаторе вследствие резкого уменьшения удельного объема пара при его превращении в капельножидкое состояние наступает вакуум, который будучи поддерживаемым в течение всего времени работы установки, позволяет пару расширяться в турбине еще на одну атмосферу (Рк около 0,04 - 0,06 бар) и совершать за счет этого дополнительную работу.
Рисунок 6. Цикл Ренкина в T-S диаграмме.

Синяя линия в Т-S диаграмме воды является разделительной, при энтропии и температуре соответствующим точкам лежащим на диаграмме выше этой линии существует только пар, ниже паро–водяная смесь.
Влажный пар в конденсаторе полностью конденсируется по изобаре p2=const (линия 2 - 3). Затем вода сжимается насосом от давления P2 до давления P1, этот адиабатный процесс изображен в T-S-диаграмме вертикальным отрезком 3-5.
Длина отрезка 3-5 в T-S-диаграмме весьма мала, так как в области жидкости, изобары (линии постоянного давления) в T-S-диаграмме проходят очень близко друг от друга. Благодаря этому при изоэптропном (при постоянной энтропии) сжатии воды, температура воды возрастает менее чем на 2 - 3 °С, и можно с хорошей степенью приближения считать, что в области жидкости изобары воды практически совпадают с левой пограничной кривой (синяя линия); поэтому зачастую при изображении цикла Ренкина в Т-S-диаграмме изобары в области жидкости изображают сливающимися с левой пограничной кривой. Малая величина отрезка адиабаты 3-5 свидетельствует о малой работе, затрачиваемой насосом на сжатие воды. Малая величина работы сжатия по сравнению с величиной работы, производимой водяным паром в процессе расширения 1-2, является важным преимуществом цикла Ренкина.
Из насоса вода под давлением P2 поступает в барабан сепаратор, а затем в реактор, где к ней в изобарно (процессе 5-4 P1=const) подводится тепло. Вначале вода в реакторе нагревается до кипения (участок 5-4 изобары P1=const) а затем, по достижении температуры кипения, происходит процесс парообразования (участок 4-1 изобары P1=const). Пароводяная смесь поступает в барабан сепаратор где происходит разделение воды и пара. Насыщенный пар, из барабана сепаратора поступает в турбину. Процесс расширения в турбине изображается адиабатой 1-2 (Этот процесс относится к классическому циклу Ренкина в реальной установке процесс расширения пара в турбине несколько отличается от классического). Отработанный влажный пар поступает в конденсатор, и цикл замыкается.
С точки зрения термического к. п. д. цикл Ренкина представляете менее выгодным, чем цикл Карно, изображенный выше (рисунок 5) поскольку степень заполнения цикла (равно как и средняя температур подвода тепла) для цикла Ренкина оказывается меньше, чем в случае цикла Карно. Однако с учетом реальных условий осуществления экономичность цикла Ренкина выше экономичности соответствующего цикла Карно во влажном паре.
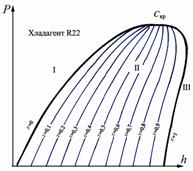
Ось ординат представляет собой логарифмическую шкалу, на которой нанесено значение давления в барах. В центре диаграммы расположена подковообразная линия, верхняя точка которой является критической и обозначена Скр. Эта линия разделяет плоскость диаграммы на 3 области. В области І (рис. 2.11) хладагент находится в жидком состоянии, в области ІІ – в парожидкостном (двухфазное состояние), в области III ‑ в состоянии перегретого пара.
В области ІІ проходят кривые x (кривые сухости), отмеченные показателем процентного содержания пара в смеси. Линия x = 0,1 соответствует состоянию газа с 10% содержанием пара и 90-процентным содержанием жидкости. Кривые x = 0 и x = 1 являются пограничными линиями. Линия х = 0 – это линия жидкого хладагента, а линия х = 1 – это линия пара. Обратим внимание на характер кривой постоянных значений температуры (рис. 2.12). В области І изотерма вертикальна, в области ІІ ‑ горизонтальна, а в области ІІІ – сначала криволинейна, а затем стремится стать вертикальной.
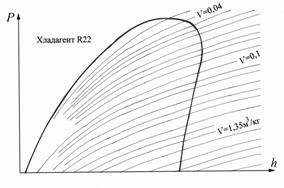
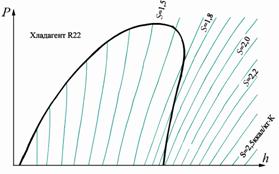
На диаграмме также изображены линии постоянного удельного объема (рис. 2.13) и линии постоянной энтропии (рис. 2.14). Для точного определения параметров термодинамического процесса пользуются lg P-h диаграммами [3], или выпускаемыми заводами-изготовителями хладагента. Как правило, эти диаграммы выполнены в крупном масштабе и очень точно, что позволяет использовать их для расчетов. Кроме того, имеются таблицы состояния хладагента при различных температурах, а также таблицы удельного объема, энтальпии и энтропии хладагента в различных состояниях (на линии насыщения, перегретого пара)
|
|
Рис. 2.11. Линии постоянной сухости на lg P-h диаграмме |
Рис. 2.12. Линии постоянной температуры (изотермы) на lg P-h диаграмме |
|
|
Рис. 2.13. Линии постоянного удельного объема на lg P-h диаграмме |
Рис. 2.14. Линии постоянной энтропии на lg P-h диаграмме |
Степень сухости - это параметр, показывающий массовую долю насыщенного пара в смеси воды и водяного пара. Значение
 соответствует
воде в момент кипения (насыщения).
Значение
соответствует
воде в момент кипения (насыщения).
Значение  ,
показывает, что в смеси присутствует
только пар. При нанесении соответствующих
точек в координатах
,
показывает, что в смеси присутствует
только пар. При нанесении соответствующих
точек в координатах  ,
взятых из таблиц насыщения справочников
свойств воды и водяного пара, при их
соединении получаются кривые,
соответствующие определённым степеням
сухости. В таком случае, линия
является
нижней пограничной кривой, а
-
верхней пограничной кривой. Область,
заключённая между этими кривыми,
является областью влажного пара. Область
ниже кривой
,
которая стягивается практически в
прямую линию (не показана), соответствует
воде. Область выше кривой
-
соответствует состоянию перегретого
пара.
,
взятых из таблиц насыщения справочников
свойств воды и водяного пара, при их
соединении получаются кривые,
соответствующие определённым степеням
сухости. В таком случае, линия
является
нижней пограничной кривой, а
-
верхней пограничной кривой. Область,
заключённая между этими кривыми,
является областью влажного пара. Область
ниже кривой
,
которая стягивается практически в
прямую линию (не показана), соответствует
воде. Область выше кривой
-
соответствует состоянию перегретого
пара.
10.Способы распространения теплоты
Формы распространения теплоты |
В природе существуют три способа передачи теплоты - излучение, конвекция, теплопроводность и два способа теплообмена между более нагретыми и менее нагретыми телами - лучистый и конвективный. Излучение - теплообмен между телами, находящимися на расстоянии друг от друга, посредством лучистой энергии, носителем которой являются электромагнитные волны (например, инфракрасное отопление). Интенсивность лучистого теплообмена между двумя телами зависит от их формы, взаимного расположения, температуры и степени черноты. Наибольшей излучающей способностью при данной температуре обладают тела, называемые абсолютно Черными. Лучистый поток от тел с меньшей излучательной способностью, чем у абсолютно черного тела (серые тела), в соответствии с законом Стефана—Больцмана, определяется формулой Фл = С0εS (T/100)4, где С0 - коэффициент излучения абсолютно черного тела, равный 4,9 ккал/(м2·ч·ºС)4; ε - степень черноты серого тела (для шероховатой стали ε = 0,944 - 0,97); S — площадь излучающей поверхности, м2. Конвекция - передача теплоты перемещением и перемешиванием частиц между собой. Различают свободную (естественную) и вынужденную (искусственную) конвекцию. Примером естественной конвекции является нагрев воздуха в квартире от радиаторов отопления, при котором часть теплоты передается излучением, а часть конвекцией воздуху, который перемещается вблизи радиатора. Нагретый воздух поднимается в верхнюю зону помещения, а более тяжелый холодный воздух постоянно перемещается к нижней части помещения. Теплопроводность - передача теплоты внутри тела от более нагретых частиц к менее нагретым. Теплопроводность материала зависит от его химического состава, пористости, влажности, температуры и давления (для жидкостей и газов). Коэффициент теплопроводности λ - количество теплоты, передаваемое в единицу времени через единицу поверхности на единицу длины (пути) теплового потока при разности температуры 1 °С. Высокой теплопроводностью характеризуются металлы, особенно серебро, медь, алюминий. Коэффициент теплопроводности стали и чугуна составляет 40-50 ккал/(м·ч·°С). Плохо проводят теплоту изоляционные материалы, некоторые жидкости (масла, жиры), воздух, газы. Очень низкой теплопроводностью обладает накипь, которая откладывается на внутренних поверхностях котлов, и сажа, которая образуется при неполном сгорании топлива и накапливается на наружных сторонах поверхностей нагрева. Количество теплоты, передаваемое через разделительную стенку, определяется формулой Q = KH Δt, где K - коэффициент теплопередачи, ккал/(м2·ч·°С); H - площадь поверхности теплообмена, м2; Δt - средний температурный напор (разность температур) между греющей и нагреваемой средой, °С. Коэффициент теплопередачи определяют по формуле: K = 1/(1/α1 + δст/λст + 1/α2), где α1 и α2 - коэффициент теплоотдачи от греющей среды к поверхности разделительной стенки и от внутренней поверхности стенки к нагреваемой среде, ккал/(м2·ч·°С); δст - толщина стенки, м; λст - коэффициент теплопроводности стенки, ккал/(м·ч·°С). Коэффициенты теплоотдачи α1 и α2 предетавляют собой сумму коэффициентов теплоотдачи конвекцией αк и излучением αл. Они зависят от режима движения потока, плотности перемещаемой среды, размеров и формы каналов, взаимного направления потоков и других условий. Примерные значения коэффициентов теплоотдачи, ккал/(м2·ч·°С): от газов к стенке α1= 20-50; от стенки к водяному пару α2 = 500-3000, к некипящей воде α2 = 5000-15 000, а к кипящей воде еще выше. Слагаемые знаменателя приведенной формулы называются частными термическими сопротивлениями. Коэффициент линейного расширения α - величина, показывающая, на какую долю первоначальной длины l0 тело удлинится при нагревании его на 1 °С. Так, для железа α = 0,000012, для меди α = 0,000017. Зная первоначальную длину конструкции (трубы) l0 и коэффициент линейного расширения или сжатия при охлаждении, можно определить длину l при любой температуре t: l = l0 (1± αt). |
11.Закон Фурье. Коэффициент теплопроводности

 Рис.
4.11
Рис.
4.11 Рис.
4.12
Рис.
4.12 Рис.
4.13
Рис.
4.13