
4. Сравните кислотность (исходя из стабильности анионов) следующий групп
соединений:
- н-пропиловый спирт, этиленгликоль
- фенол, п-нитрофенол, п-аминофенол
- этанол, этантиол, фенол
- уксусная, щавелевая, муравьиная кислоты
- фенол, п-гидроксибензойная кислота, п-дигидроксибензол
- аммиак, этиламин, ацетамид
- этанол, уксусная кислота, фенол
Напишите уравнения солеобразования.
Решение
CH3CH2CH2OH и HOCH2CH2OH
В результате электроноакцепторного эффекта (–I) второй гидроксильной группы этиленгликоль является относительно более сильной кислотой, чем 1-пропанол. Образование моноалканолята этиленгликоля частично происходит уже в растворе щелочи.
![]()
2CH3CH2CH2OH+ 2Na = 2CH3CH2CH2ONa + H2
фенол, п-нитрофенол, п-аминофенол
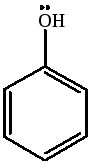
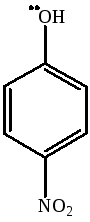
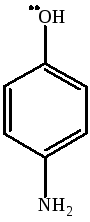
Наиболее сильной кислотой является п-нитрофенол, за счет сильного –I-эффекта нитрогруппы, затем идет фенол и п-аминофенол
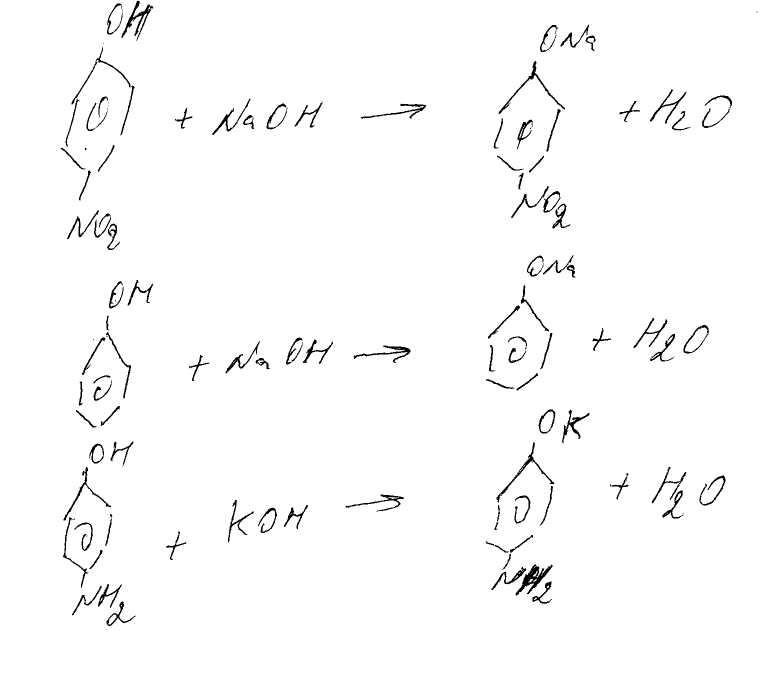
CH3CH2OH CH3CH2SH C6H5OH
Если сравнивать рКа, то наиболее кислым является фенол (рКа=9,98), затем идет этантиол (рКа=10,6) и последний этанол

уксусная, щавелевая, муравьиная кислоты
Самая сильная щавелевая кислота, затем муравьиная и уксусная. Введение алкильных групп уменьшает кислотность, что обусловлено электронодонорным действием алкильных групп.
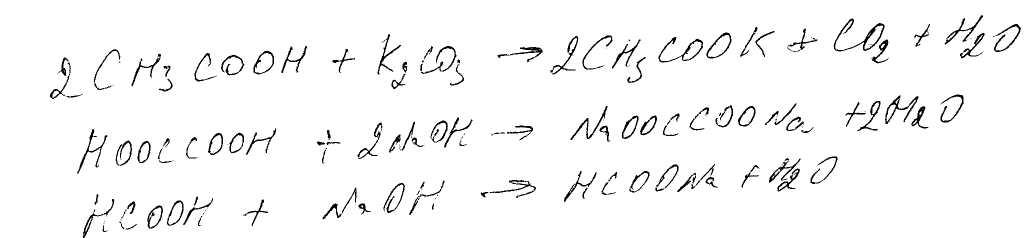
фенол, п-гидроксибензойная кислота, п-дигидроксибензол
Кислее п-гидроксибензойная кислота, затем фенол и п-дигидроксибензол. Из-за +M-эффекта второй гидроксильной группы устойчивость аниона падает.

аммиак, этиламин, ацетамид
Наиболее кислым является ацетамид, затем аммиак и этиламин. Этиламин и аммиак являются очень слабыми NH-кислотами, поэтому только взаимодействие с металлорганическими соединениями ведет к ионизации связи.
![]()
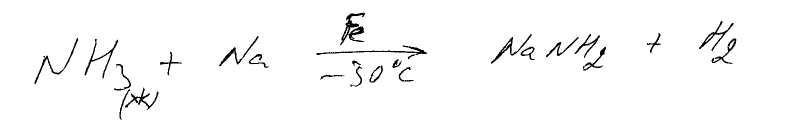
Амиды являются слабыми NH-кислотами. Повышенная кислотность амидов по сравнению с аминами объясняется сильным влиянием карбонильной группы (эффект сопряжения, делокализация отрицательного заряда в анионе):
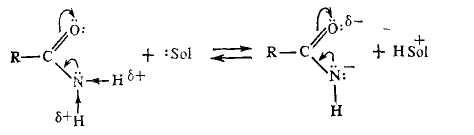
этанол, уксусная кислота, фенол
слабая кислота уксусная, затем идет фенол и этанол, как очень слабая кислота. (примеры реакций солеобразования выше)
