
3. Напишите уравнения реакций гидратации этилена, пропена; бутена-1; 2-метилбутена-1. Опишите механизм и объясните роль катализатора. Объясните действие правила Марковникова.
Решение.
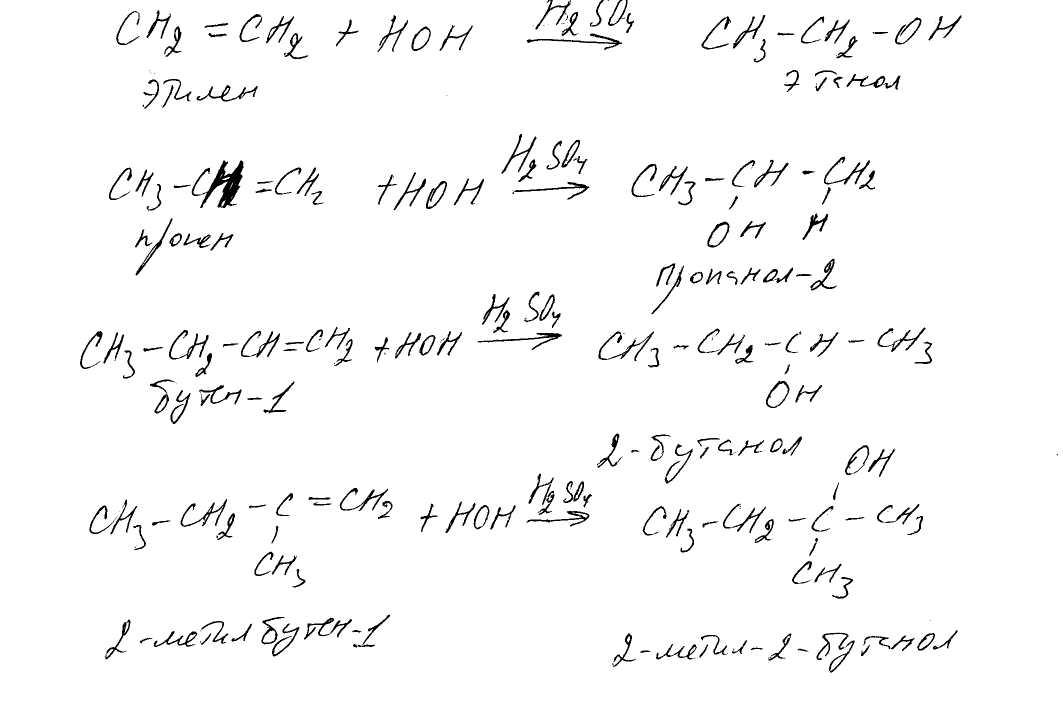
При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. В качестве электрофильного агента в этом случае выступает протон.
Стадия протонирования алкена определяет скорость реакции. Эта стадия, как и весь процесс гидратации, обратима; при этом взаимодействие образующегося карбокатиона с водой происходит быстрее, чем его депротонирование и получение алкена.
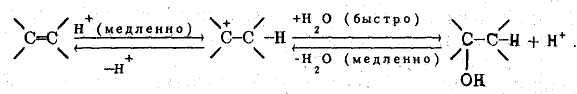
Установлено также, что комплекс «алкен-протон» в гидратации не участвует.
Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Реакция идет по правилу Марковникова.

Правило Марковникова: при присоединении молекул типа НХ к несимметричным алкенам водород присоединяется к более гидрогенюированному атому углерода двойной связи.
Изучая присоединение галогеноводородов к алкенам, В. В. Марковников нашел, что при этом протон присоединяется к наиболее гидрогенизованному атому углерода, т. е. что реакция региоселективна. Эта закономерность, известная как правило Марковникова, может быть легко объяснено. Новая С—Н-связь формируется за счет π-электронов этиленовой связи. При образовании свободного и наиболее устойчивого карбокатиона протон присоединяется к наименее замещенному (т.е. содержащему наибольшее число Н-атомов, наиболее гидрогенизованному атому углерода). Но при присоединении галогеноводородов к алкенам свободные карбокатионы обычно не образуются, а правило Марковникова тем не менее соблюдается и для этих случаев. Это объясняется тем, что возникающий в интермедиатах частичный положительный заряд локализуется преимущественно на наиболее замещенном атоме углерода, где он более всего компенсирован.
