
Проверка знаний по всему курсу. Часть 2 (pdf)
.pdf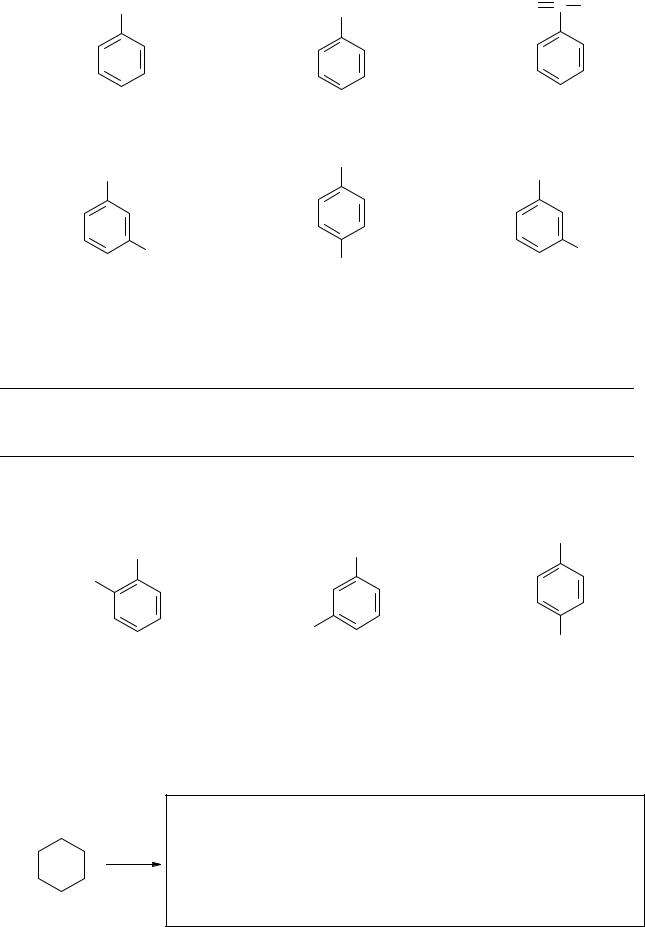
21
г) |
д) |
+ |
е) |
|
O-- |
O C R |
|
|
NH3 |
|
___________________ |
___________________ |
___________________ |
ж) |
з) |
OH |
и) |
|
CH3 |
COOH |
|
|
|
Cl |
NO2 |
NH2 |
|
|
|
___________________ |
___________________ |
___________________ |
4.Из задания 3 выберите соединения, имеющие дезактивирующие ориентанты.
5.Из задания 3 выберите соединения, имеющие согласованную ориентацию.
6.Расположите в порядке увеличения дипольного момента следующие соедине-
ния: |
|
|
|
а) |
б) |
в) |
Cl |
|
Cl |
Cl |
|
|
Cl |
|
|
|
|
Cl |
Cl |
|
|
|
_________________________________________________________
СПОСОБЫ ПОЛУЧЕНИЯ
1. Какие углеводороды ряда бензола могут образоваться при реакции каталитической дегидрогенизации углеводородов:
а)
kat

22
б)
C7H16 kat
в)
kat
2. Какой ароматический углеводород может образоваться при полимеризации метилацетилена?
kat CH3 C CH
CH 
3. Напишите и назовите продукты нижеприведенных реакций алкилирования. Укажите условия их протекания.
CH2 CH CH3
CH CH3
CH3
CH2 C
CH3

23
4. С помощью каких реагентов можно осуществить нижеприведенные схемы реакций Фриделя–Крафтса? Укажите условия протекания реакций.
Cl
ХИМИЧЕСКИЕ СВОЙСТВА И МЕХАНИЗМЫ РЕАКЦИЙ
1. Напишите уравнения реакций бромирования толуола (с образованием монобромзамещенных). Назовите образующиеся соединения.
t
CH3
+ Br2
Fe (или Al)

24
2. Напишите продукты реакций окисления.
CH3
CH(CH3)2
CH(CH3)2 KMnO4, t
CH3
C(CH3)3
3. Напишите для бензола уравнения реакций (с образованием однозамещенных производных). Укажите условия каждой реакции. Назовите образующиеся соединения.
O |
|
CH3C Cl |
H2SO4 |
|
Cl2 |
|
HNO3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

25
4. Напишите, как будут преимущественно протекать реакции бромирования.
OH
Br
CH3
NO2
+ Br2 (FeBr3)
NH2
Cl
OCH3
COOH
5. В каком из трех изомеров ксилола метильные группы проявляют согласованное влияние на реакцию замещения? Напишите для этого изомера реакции нитрования. Назовите образующиеся продукты.

26
6. Знаками больше/меньше (<>) укажите какое из нижеприведенных соединений будет легче вступать в реакцию нитрования (HNO3, H2SO4).
а) |
|
O |
б) |
OH |
|
|
C |
NO2 |
|
|
|
CH3 |
|
|
в) |
CH3 |
CH3 |
г) |
CH3 |
CH3
7. Напишите продукты реакций нафталина (с образованием однозамещенных производных). Укажите условия каждой реакции. Назовите образующиеся соединения.
CrO3 |
|
H2SO4 |
|
|
|
|
H2 |
|
Br2 |
|
|
|
|
|
|
|
|
8. Предложите способ получения из бензола м-нитробензойной кислоты.

27
1. Приведите механизм реакции алкилирования толуола хлористым этилом по Фриделю–Крафтсу. Укажите лимитирующую стадию.
КОМПЛЕКСНЫЕ ЗАДАЧИ
1. Используя метан, в качестве единственного источника органических соединений получите м-нитробромбензол.

28
2. Ароматический углеводород состава С9Н8 обесцвечивает раствор брома, присоединяя две молекулы брома, а при окислении образует бензойную кислоту; с аммиачным раствором оксида серебра (I) дает характерный осадок. Напишите формулу и название углеводорода, а также схемы реакций.
3. Некоторые изомерные углеводороды состава С10Н10 ведут себя при реакциях так же, как описано в задании 2. Напишите формулу одного из углеводородов, отвечающих этому условию, а также схемы соответствующих реакций.
29
ОСОБЕННОСТИ СТРОЕНИЯ, РЕАКЦИОННОЙ СПОСОБНОСТИ И МЕТОДЫ СИНТЕЗА ГАЛОГЕНПРОИЗВОДНЫХ И ГИДРОКСИЛСОДЕРЖАЩИХ УГЛЕВОДОРОДОВ
ПРОГРАММА
Галогенопроизводные. Классификация галогенпроизводных.
Галогеналканы. Изомерия. Номенклатура. Физические свойства. Основные методы синтеза галогеналканов из алканов, алкенов, спиртов.
Нуклеофильное замещение у насыщенного атома углерода. Реакции нуклеофильного замещения у насыщенного атома углерода как метод создания связи угле- род-галоген, углерод-азот, углерод-кислород, углерод-углерод, углерод-сера, углеродфосфор (получение алкилгалогенидов, спиртов, тиолов, дисульфидов, простых эфиров, нитросоединений, аминов, нитрилов и др.).
Классификация механизмов реакций нуклеофильного замещения. Понятие о нуклеофильности. Основные характеристики SN1– и SN2–процессов. Энергетический профиль реакций.
Реакции SN2–типа. Кинетика, стереохимия, вальденовское обращение. Влияние природы радикала и уходящей группы субстрата, природы нуклеофильного агента и растворителя на скорость SN2–реакций. Факторы, определяющие реакционную способность нуклеофильного реагента.
Реакции SN1-типа. Кинетика, стереохимия. Зависимость SN1–процесса от природы радикала, уходящей группы и растворителя. Карбокатионы, факторы, определяющие их устойчивость. Перегруппировки карбокатионов. Методы генерирования стабильных карбокатионов. Электрофильный катализ в SN1–реакциях.
Реакции отщепления галогеноводорода (правило Зайцева). Конкуренция реакций замещения и отщепления в зависимости от природы реагента и условий реакции.
Другие галогенпроизводные. Реакции нуклеофильного замещения у галогенарилов (SN2аром). Зависимость реакционной способности от природы галогена и характера радикала. Соединения с «нормальной» (галоидный алкил, циклоалкил), пониженной (галоидвинил, галоидбензол) и повышенной (галоидные аллил и бензил) реакционной способностью.
Реакции алкилгалогенидов с металлами. Металлорганические соединения и их значение для органического синтеза. Реактив Гриньяра. Ди- и полигалогенпроизводные. Реакции гидролиза и отщепления.
Оксисоединения, их классификация (насыщенные, ненасыщенные и ароматические спирты, фенолы и нафтолы; многоатомные спирты).
Одноатомные спирты. Номенклатура. Физические свойства. Методы введения ОН-группы в органическое соединение. Ассоциация. Химические свойства спиртов. Свойства спиртов. Спирты как слабые ОН-кислоты. Спирты как основания Льюиса. Замещение гидроксильной группы в спиртах на галоген (под действием галогеноводородов, галогенидов фосфора, хлористого тионила). Механизм и стереохимия замещения, перегруппировки с гидридным перемещением. Реагенты регио- и стереоспецифического замещения (комплексы трифенилфосфина с галогенами). Дегидратация спиртов. Ретропинаколиновая перегруппировка.
Окисление первичных спиртов до альдегидов и карбоновых кислот, вторичных спиртов - до кетонов. Реагенты окисления на основе хромового ангидрида.

30
Методы получения спертов: из алкенов, карбонильных соединений, галогеналканов, сложных эфиров.
Двухатомные спирты. Номенклатура. Физические свойства. Методы синтеза. Свойства. Окислительное расщепление 1,2-диолов (йодная кислота, тетраацетат свинца). Пинаколиновая перегруппировка.
Фенолы. Номенклатура. Физические свойства. Методы получения: щелочное плавление аренсульфонатов, замещение галогена на гидроксил, гидролиз солей арендиазония. Кумольный метод получения фенола в промышленности. Свойства. Фенолы как ОН-киолоты, влияние заместителей на кислотность фенолов. Амбидентный характер фенолят-ионов. С– и О-алкилирование фенолятов. Реакции электрофильного замещения в ароматической ядре фенолов и нафтолов: галогенирование, сульфирование, нитрование, нитрозирование, алкилирование. Карбоксилирование фенолятов щелочных металлов. Конденсация фенолов с карбонильными соединениями (фенолформальдегидные смолы). Окисление фенолов.
Простые эфиры спиртов и фенолов. Номенклатура. Физические свойства. Методы получения: реакция Вильямсона, алкоксимеркурирование алкенов, межмолекулярная дегидратация спиртов. Свойства простых эфиров: образование оксониевых солей, расщепление кислотами. Гидропероксиды. Краун-эфиры. Получение и применение в синтетической практике. Циклические простые эфиры. Окись этилена. Тетрагидрофуран, диоксан, диэтиловый эфир.
ОСНОВНЫЕ ТЕРМИНЫ, ПОНЯТИЯ, ОПРЕДЕЛЕНИЯ
Дайте определение следующим понятиям:
Вальденовское обращение –
Водородная связь –
Гидролиз –
Нуклеофильное замещение –
Правило Зайцева-Гофмана –
