
- •Ароматичні вуглеводні.
- •Правила орієнтації в бензеньному ядрі.
- •З Циклогексанон nh2oh циклогексаноноксим поліамідна смола(капрон) адипінова к-та гексаметилендіамін поліамідна смола (нейлон) астосування бензену
- •Застосування толуену
- •Нафтален. Фізичні властивості.
- •Особливості будови (c10h8).
- •Хімічні властивості:
- •Отримання в техніці.
- •Антрацен.
- •Антрахінон
- •Фенантрен
Ароматичні вуглеводні.
NO2
NO2
OH
2
–
H Бензен - C6H6
Толуен - C6H5CH3
О-ксилол - C6H4(CH3)2
Стирол - C6H5(C2H3)
Нафтален - C10H8
Дифелін - C6H5-C6H5
Радикали, утворені з ароматичних вуглеводнів, носять загальну назву арили:
Феніл бензіл -о-толіл
Фізичні властивості.
Бензен і його гомологи володіють сильними специфічними запахами. Рідкі вуглеводні сильно заломлюють світло, легші за воду і малорозчинні у воді і горючі. Володіють значною токсичністю. |
Хімічні властивості.
а) Електрофільного
б) Нуклеофільного
в) Радикального
|
4
+O2 Методи отримання.
а) з кам’яновугільної смоли, коксового газу. б) Піроліз, каталітичний крекінг нафти. в) Дегідрування циклоалканів.
а) Реакція В.Фітіша:
б) Алкілування:
в) Сплавлення солей арильних кислот з лугами:
Використання.
Бензен має дуже різноманітне використання: на його основі синтезують інсектициди, барвники, ліки, вибухові речовини, поліефіри, синтетичне волокно, каучуки, пластмаси. Його також застосовують в якості розчинника для багатьох органічних речовин.
|
Реакції приєднання.
|
Правила орієнтації в бензеньному ядрі.
-OH, -OR,-OCOR, -SH, -SR, -NH2, -NHR, -NR2, -NHCOR, -N=N-CH3, -CH2R, -CR3, -F, -Cl, -Br, -J. Замісники другого роду це атомні угрупування, які здатні відтягувати, приймати електрони від бензеньного ядра (електроноакцепторні). До них відносяться: -SO3H, -NO2, -CHO, -COR, -COOH, -COOR, -CN, -CCl3, -NH3+, -NR3+.
Замісники першого роду полегшують реакцї з електрофільними реагентами (крім галогенів), при чьому вони орієнтують новий замісник в орто- і пара- положення. Замісники другого роду утруднюють реакції з електрофільними реагентами, при чьому вони орієнтують новий замісник в мета-положення. В той же час ці замісники полегшують реакції з нуклеофільними реагентами. Головні замісники по силі орієнтуючої дії в реакціях електрофільного заміщення: OH>NH2>Cl>J>Br>CH3; COOH>SO3H>NO2.
|
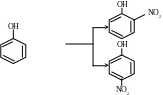
Приклади реакцій з різною орієнтуючою дією замісників.
- орто-нітрофенол
+HONO2
- пара-нітрофенол
+HONO2 30C мета-динітробензен
+NaOH -NaH
|














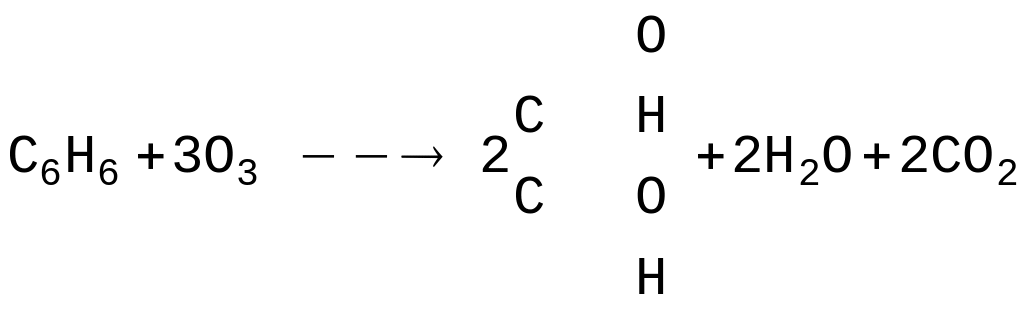
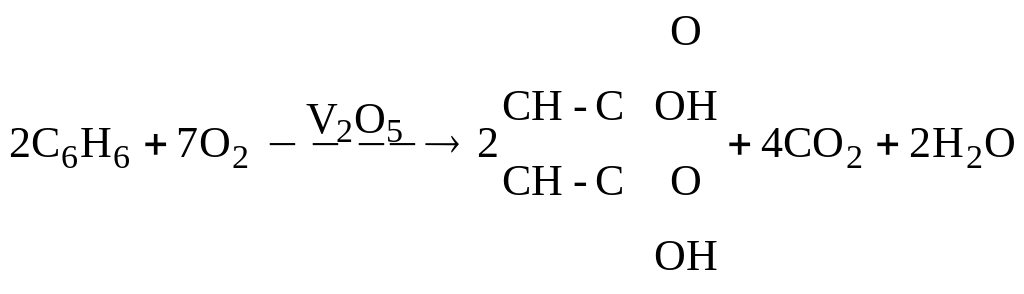
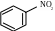






 Замісники
першого роду
це угрупування атомів, які здатні
віддавати електрони (електронодонорні).
Жо них відносяться:
Замісники
першого роду
це угрупування атомів, які здатні
віддавати електрони (електронодонорні).
Жо них відносяться: