- •1. Основные понятия термодинамики: термодинамическая система, параметры экстенсивные и интенсивные, функция состояния, ее свойства. Уравнения состояния.
- •1) Поглощенная системой теплота расходуется на увеличение внутренней энергии системы и на совершение ею работы.
- •2) Работа любого циклического процесса равна его теплоте:
- •3. Работа. Определение работы в изотермически, изохорическом, изобарическом и адиабатическом процессах. Изобразите эти процессы на диаграмме p(V).
- •4. Нулевой закон термодинамики. Эмпирическая температура.
- •6. Теплота. Определение теплоты в изотермическом, изохорическом, изобарическом процессах. Теплота циклического процесса.
- •7.Адиабатический процесс. Уравнения адиабаты работа и теплота в адиабатическом процессе.
- •8,9.Политропический процесс. Уравнения политропы. Работа и теплота в политропическом процессе.Показатель политропы. Привести график зависимости показателя политропы (n) от теплоемкости (с).
- •12. Закон Гесса и следствия из него. Дайте определения тепловому эффекту химической реакции, стандартной энтальпии образования и сгорания веществ. Термохимическое уравнение реакции.
- •16.Циклические процессы. Термодинамический кпд. Цикл Карно. Приведите цикл Карно на диаграмме p(V). Кпд цикла Карно.
- •17.Теорема Карно. Теорема Клаузиуса. Теорема Карно-Клаузиуса. Свойства цикла Карно.
- •19.Равенство Клаузиуса. Расчет энтропии в различных термодинамических процессах с идеальным газом: изохорическом, изобарическом, изотермическом, адиабатическом, политропическом.
- •24.Системы переменного состава. Химический потенциал как парциальная молярная величина экстенсивного свойства системы. Приведите выражения для приращений функций dF,dG для систем переменного состава.
- •26.Уравнения Гиббса-Дюгема. Какие важные соотношения можно получить, используя эти уравнения.
- •27. Приведите выражения для химического потенциала компонента в идеальных и реальных газовых системах. Какие факторы влияют на значение химического потенциала. Что такое летучесть компонента?
- •53. Что такое активность и коэффициент активности? Как зависит коэффициент активности от общей концентрации электролита? Сформулируйтe правило ионной силы Льюиса-Рендалла.
- •54. Дайте определение экстракции. Какие факторы влияют на процесс экстракции? Коэффициент распределения.
- •55. Экстракция. Что называется степенью извлечения r? От каких факторов зависит численное значение степени извлечения?
- •56. Экстракция. Сформулируйте закон распределения Нернста. От каких факторов зависит численное значение коэффициента распределения? Применение экстракции в фармации.
- •65. Запишите уравнение Нернста для электродного потенциала следующих систем в водных растворах:
- •75. Рассчитайте значения эдс в стандартных условиях и ΔrG298 для следующей ов-реакции и сделайте вывод о возможности ее самопроизвольного протекания в данных условиях:
- •76. Рассчитайте значения эдс в стандартных условиях и ΔrG298 для окислительно- восстановительной реакции и сделайте вывод о возможности ее самопроизвольного протекания в данных условиях:
- •97. Понятие катализа. В чем состоит ключевое отличие гомогенного катализа от гетерогенного? От каких факторов зависит скорость реакции в случае гомогенного и в случае гетерогенного катализа?
- •99. Ферментативный катализ. Теория Михаэлиса-Ментен. Основные постулаты теории Константа Михаэлиса. Экспериментальные методы определения константы Михаэлиса.
97. Понятие катализа. В чем состоит ключевое отличие гомогенного катализа от гетерогенного? От каких факторов зависит скорость реакции в случае гомогенного и в случае гетерогенного катализа?


Скорость гомогенной реакции (vгомог) определяется как изменением количества вещества в единицу времени в единице объема:
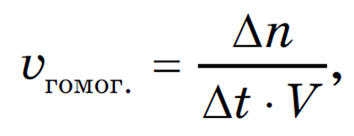
где Δn — изменение числа молей одного вещества (чаще всего исходного, но может быть и продукта реакции); Δt — интервал времени (с, мин); V — объем газа или раствора (л).
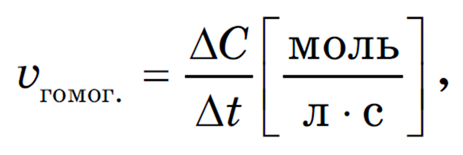

98. Приведите уравнение Михаэлиса-Ментен. Каков физический смысл константы Михаэлиса? Какова стационарная скорость ферментативного процесса (w), если константа Михаэлиса равна концентрации субстрата Km=C(S)?



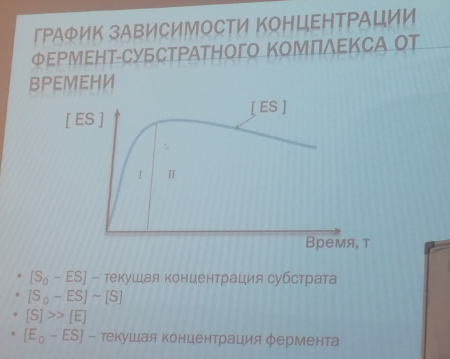






99. Ферментативный катализ. Теория Михаэлиса-Ментен. Основные постулаты теории Константа Михаэлиса. Экспериментальные методы определения константы Михаэлиса.



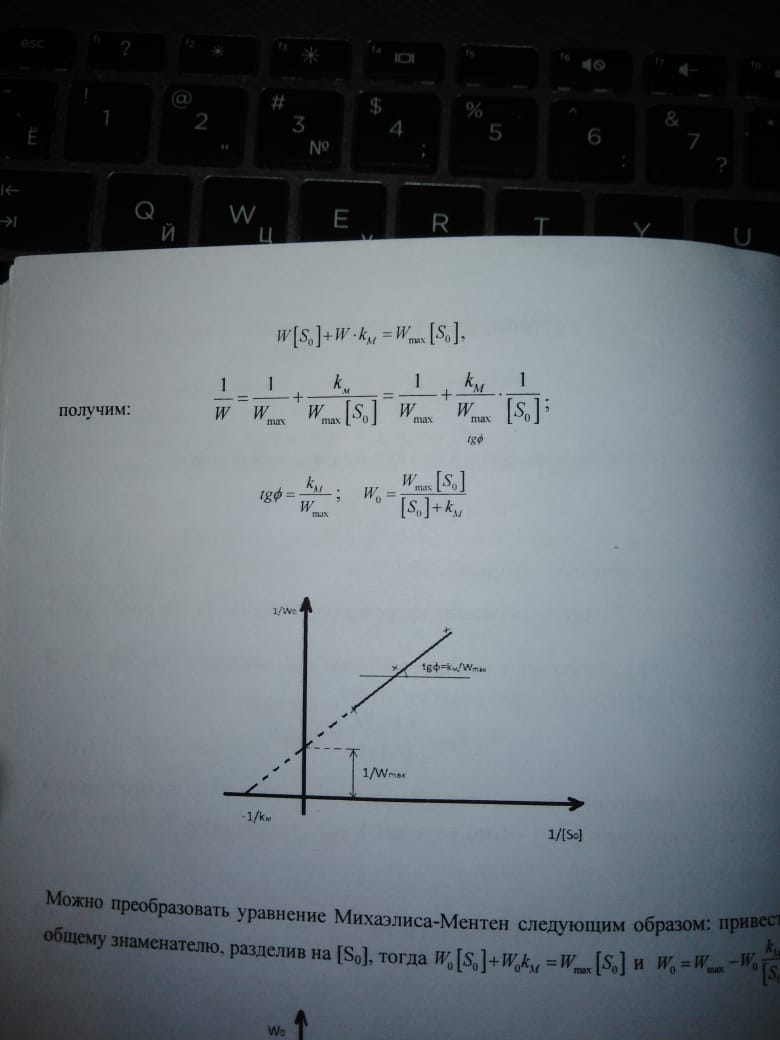


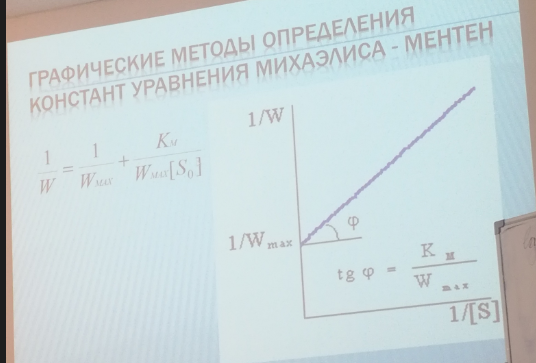
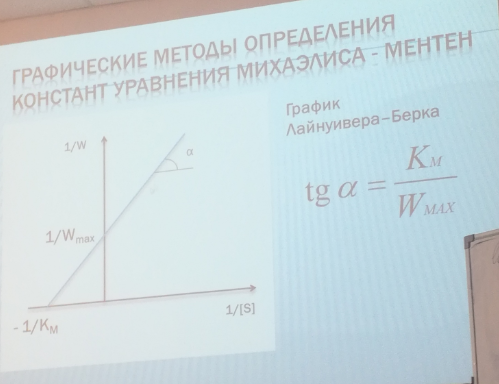

100. Гетерогенный катализ. Основные стадии каталитических гетерогенных реакций. Приведите основные теории гетерогенного катализа: мультиплетная теория Баландина, теория активных ансамблей Кобозева, электронная теория.

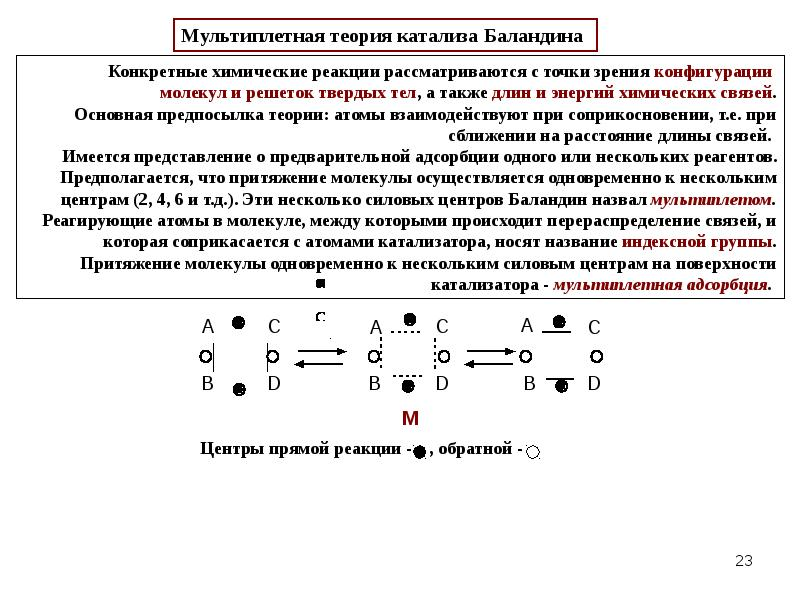
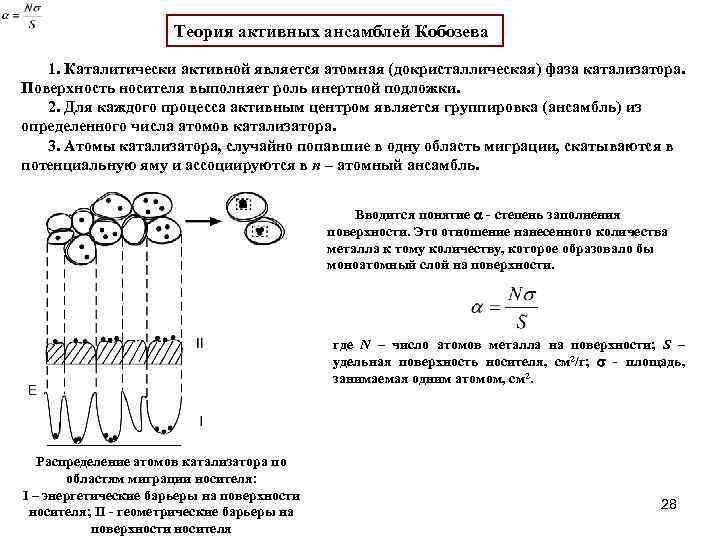


Доп. инфо:
Электронные представления в катализе начали развиваться в 30-х годах XX в. Писаржевским, Волькенштейном, Хауффе и др. Электронная теория катализа основывается на квантовомеханической зонной теории твердого тела.
Рассмотрим ионный кристалл полупроводника MR, состоящий из однозарядных катионов М+ и анионов .R-. Электропроводность такого кристалла связана с тем, что часть электронов, обладающая повышенной энергией, делокализуется и может свободно перемещаться по кристаллу. В свете элементарных химических представлений это значит, что электрон переходит от аниона к катиону с образованием в двух соседних узлах кристаллической решетки двух нейтральных атомов:
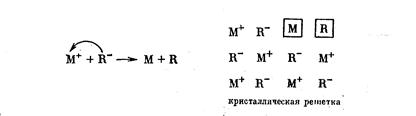
У ионов М+ и R- (например, Na+ и С1-) имеются замкнутые восьмиэлектронные оболочки и отсутствуют свободные неспаренные (валентные) электроны. У электроположительного атома имеется валентный электрон—свободная положительная валентность (n-связь). У электроотрицательного атома отсутствует один электрон в восьмиэлектронной оболочке, что равнозначно появлению эффективного положительного заряда (дырке) или отрицательной свободной валентности (р-связь). Для катализа имеет значение появление таких свободных валентностей на поверхности твердого тела:
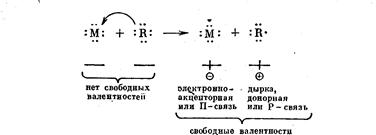
Горизонтальные отрезки на схеме изображают поверхность катализатора. Электрон может перемещаться по катионной подрешетке (электронная проводимость); дырка—по анионной подрешетке (дырочная проводимость).
В настоящее время эти элементарные представления получили уточнение в зонной теории твердого тела. В твердом теле электронные энергетические уровни атома расщепляются в энергетические полосы. При этом в полупроводниках между энергетической полосой валентных электронов атомов твердого тела (валентная зона) и энергетической полосой возбужденных электронов (зона проводимости) имеется некоторый промежуток (запрещенная зона), в котором (в случае идеального кристалла без примесей) нет энергетических уровней электронов. Чтобы перейти из валентной зоны в зону проводимости, электрону нужно иметь некоторую минимальную избыточную энергию активации, равную ширине запрещенной полосы. Переход электрона из валентной зоны в зону проводимости соответствует перескоку электрона с аниона на катион и его перемещению по катионной подрешетке (электронная, или n-проводимость). После перехода электрона в зону проводимости в валентной зоне остается дырка, которая соответствует аниону, лишенному электрона, и перемещению этой дырки по анионной подрешетке (дырочная, или р-проводимость).
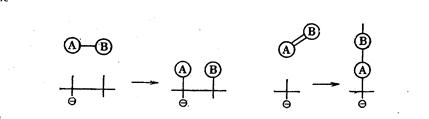
Электронная теория катализа допускает существование разных видов связи хемосорбированных частиц из газа на поверхности полупроводника: слабой одноэлектронной связи и двух видов прочной двухэлектронной связи — акцепторной и донорной, которые в свою очередь могут иметь ковалентный или ионный характер в зависимости от природы адсорбируемой частицы. Предположим, что адсорбируемая частица является одновалентным атомом: электроположительным атомом А (типа Na) или электроотрицательным атомом В (типа С1), а катализатор — полупроводниковый ионный кристалл состава MR (типа NaCl), который имеет в узлах решетки и на поверхности кристалла частицы: М+, R-, М и R. При этом будут наблюдаться следующие шесть случаев химической связи, показанные на схеме (в двух случаях — 2 и 5 — связь не образуется).
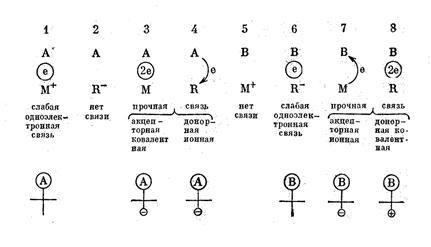
Как видно из схемы, при адсорбции атома (или радикала) на свободной валентности образуется прочная связь (случаи 3, 4 и 7, 8). При этом свободная валентность расходуется на образование химической связи, которая в предельных случаях может быть ионной или ковалентной. Такой адсорбированный атом или радикал не реакционноспособный. У адсорбированного атома или радикала в состоянии слабой связи остается свободная валентность (случай 1 и 6); он является реакционноспособным и вступает в химические реакции.
Свободные валентности (электроны и дырки) могут перемещаться (блуждать) по кристаллу. Поэтому прочная связь может переходить в слабую, а слабая в прочную. В зависимости от характера полупроводника ( n- или р - полупроводник) на нем будет протекать адсорбция преимущественно на прочной акцепторной или прочной донорной связи и соответственно будет меняться избирательность (селективность) полупроводникового катализатора. Если адсорбируются молекулы, то при адсорбции их в форме прочной связи в них обычно рвутся связи между атомами, молекула превращается в радикал и это способствует осуществлению катализа. Например, при адсорбции двухатомной молекулы АВ с одинарной связью на прочной связи происходит диссоциация молекулы на адсорбированные атомы А и В. При адсорбции молекулы с двойной связью рвется одна связь и образуется радикал. Эти процессы можно представить на схеме