
- •6.051301 “Хімічна технологія” денної і заочної форм навчання
- •6.051301 “Хімічна технологія” денної і заочної форм навчання
- •Передмова
- •Вимоги до звіту лабораторних робіт
- •Техніка безпеки в хімічній лабораторії
- •Методи визначення аміаку в газах
- •1. Теоретичні відомості
- •2. Обладнання і хімічні реактиви
- •3 Опис лабораторної установки
- •4. Послідовність виконання роботи і проведення розрахунків
- •5. Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Конверсія оксиду вуглецю (II)
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви
- •3 Опис лабораторної установки, послідовність виконання роботи і проведення розрахунків
- •Опис приладу
- •Підготовка приладу до роботи
- •Відбір проби на аналіз
- •Проведення аналізу
- •4. Техніка безпеки
- •5. Контрольні питання
- •6. Література
- •Аналітичний контроль нітрозних газів
- •1. Теоретичні відомості
- •2 Обладнання і хімічні реактиви
- •3. Опис лабораторної установки
- •4 Послідовність виконання роботи і проведення розрахунків
- •5 Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Каталітичне окиснення аміаку
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви
- •3 Опис лабораторної установки
- •4 Порядок виконання роботи і проведення розрахунків
- •5 Техніка безпеки
- •2. Обладнання та хімічні реактиви
- •3. Порядок виконання роботи
- •4 Опрацювання результатів
- •5 Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Абсорбція оксидів азоту в пінному апараті
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви:
- •3 Опис лабораторної установки
- •4. Порядок виконання роботи і проведення розрахунків
- •5 Техніка безпеки
- •6 Контрольні питання
- •7 Література
- •Аналіз азотної кислоти
- •1 Теоретичні відомості
- •2 Обладнання і хімічні реактиви:
- •3 Опис лабораторної установки
- •4. Техніка безпеки
- •5. Контрольні питання
- •6. Література
- •1 Умови виконання вимірювань
- •2 Приготування розчинів
- •3. Приготування градуювальних розчинів
Опис приладу
Газоаналізатор (рис. 2.3) складається з вимірювальної бюретки 1, водяної (повітряної) сорочки 2, напірної склянки 3, кранової системи (гребінки) 4 з трьома триходовими кранами 5, які пов'язують її з поглинальними посудинами 6, 7, 8, триходового крана 9 для відбору проб газу і регулювання роботи системи в цілому.
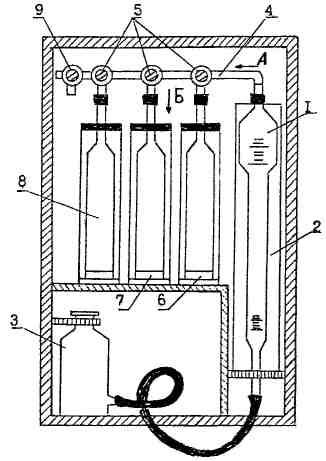
1 – вимірювальна бюретка; 2 – повітряна сорочка; 3 – напірна склянка; 4 – гребінка; 5, 9 – триходові крани; 6, 7, 8 – поглинальні посудини.
Рисунок 2.3 – Газоаналізатор
Вимірювальна бюретка 1 призначається для виміру об'єму, взятого на аналіз газу і для подальшого визначення зміни об'єму газу після поглинання.
Вміст вимірювальної бюретки 100 см3. Верхня розширена частина (50 см3) має поділки через 10 см3 і ціну поділки 1 см3, нижня подовжена циліндрична (50 см3) частина має поділки через 2 см3 і ціну 0,2 см3.
Для зручності користування шкала бюретки має подвійну цифрову шкалу з правого боку вгорі – нуль шкали, знизу 100 см3, з ліва знизу – нуль шкали, вгорі – 100 см3.
Це дозволяє робити відлік з правого боку об'єму забраної проби газової суміші в см3, а з лівого об'єму поглинених газів у см3 або об'ємних процентах.
Призначення водяної сорочки 2 – виключення різких коливань температури у вимірювальній сорочці, що впливають на точність.
Напірна склянка з ємністю не менше 300 см3 заповнена на 3/4 об'єму затвірною рідиною і з'єднана з нижньою частиною вимірювальної бюретки 1 гумовою трубкою, призначеною для всмоктування газу у вимірювальну бюретку з наступним поданням його у поглинальну посудину.
Кранова система (гребінка) 4 являє собою розподільний пристрій, що складається з товстостінної капілярної трубки з трьома кранами 5. Крани з'єднані з поглинальними посудинами 6, 7, і 8 за допомогою товстостінних гумових трубок. Одним кінцем гребінка 4 з'єднана з вимірювальною бюреткою 1, а іншим – через триходовий кран 9 з атмосферою та джерелом газу, що направляється на аналіз (до досліду – з газометра вихідного газу, після досліду – з газометра з конвертованим газом.
Триходові крани 5 і 9 призначені для зміни напряму газових потоків у приладі і зєднання останнього з джерелом газу і атмосферою. Залежно від положення триходового крана мають місце 4 варіанти руху газових потоків. Наступне положення відрізняється від попереднього поворотом на 900 за годинниковою стрілкою. Усі три крани 5 (для яких направлення А гребінка, а направлення Б – поглинальна посудина) мають два робочі положення: 1 – коли крани разом з гребінкою утворюють наскрізний канал для проходу газу у вимірювальну бюретку або з неї; 2 – коли виконується аналіз газу на вміст якогось з компонентів, вимірювальна бюретка і відповідна поглинальна посудина являють собою ізольовану від зовнішнього середовища систему з двох сполучених посудин.
Через кран 9 крізь трубку А проводиться забір аналізоваого газу, крізь трубку В – викид газу в атмосферу, крізь трубку Б кран 9 сполучається з поглинальною системою в цілому. Відповідно до цього кран 9 має три робочі положення: 1 – набір газу у вимірювальну бюретку; 2 – викид газу в атмосферу; 3 – ізоляція поглинальної системи від зовнішнього середовища.
Кожна з поглинальних посудин 6, 7 і 8 складається з подвійних посудин, що знаходяться одна в одній. Внутрішня посудина призначена для прийому газу протягом часу поглинання. Для збільшення поверхні зіткнення газу з поглиначем вона заповнена тонкостінними скляними трубками.
Зовнішня посудина служить для прийому поглинального розчину за час заповнення внутрішньої посудини газом.
Поглинальну посудину 6 для поглинання СО2 наповнюють розчином КОН.
Оксид вуглецю (IV), реагуючи з КОН, утворює карбонат калію:
2 КОН + СО2 К2СО3 + Н2О.
Поглинальна посудина 7 призначена для поглинання кисню і наповнюється розчином пірогалолу (1, 2, 3 – триоксибензолу). У лужному середовищі пірогалол утворює пірогалят калію:
С6Н3(ОН)3 + 3 КОН С6Н3(ОК)3 + 3 Н2О.
Останній, поглинаючи кисень і відщеплюючи воду, переходить у гексаоксидифенолят калію:
4 С6Н3(ОК)3 + О2 2 (ОК)3С6Н2 – Н2С6(ОК)3 + 2 Н2О.
Поглинальна посудина 8 служить для поглинання СО і наповнюється аміачним розчином однохлористої міді.
СО, реагуючи з СН2Сl2, утворює спочатку комплексну, що легко розкладається:
Сu2Сl2 + 2СО Сu2Сl2 2СО,
що далі взаємодіє з аміаком та відновлюється до вільної міді:
Cu2Cl2∙2CO + 4NH3 + 2H2O 2Cu + (NH4)2C2O4 + 2NH4Cl.
