
- •1. Основное кинетическое уравнение массопередачи. Коэффициент массопередачи и движущая сила процесса.
- •2. Движущая сила моссообменного процесса при нелинейной равновесной зависимости. Число единиц переноса и его физический смысл.
- •3. Выражение для средней движущей силы и числа единиц переноса при линейной равновесной зависимости.
- •4. Модифицированные уравнения массопередачи. Число единиц переноса. Высота эквивалентная единице переноса.
- •5. Материальный баланс массообменного процесса. Рабочая линия массообменного процесса.
- •6. Массообмен в системах без твердой фазы. Молекулярная и конвективная диффузия.
- •7. Дифференциальные уравнения молекулярной и конвективной диффузии. Числа подобия диффузионных процессов, их физический смысл.
- •8. Молекулярная диффузия. Первый закон Фика. Коэффициент диффузии и его физический смысл.
- •9. Уравнение Щукарева. Коэффициент массоотдачи и его физический смысл. Сопоставление с коэффициентом массопередачи.
- •10. Выражения коэффициента массопередачи через коэффициенты массоотдачи.
- •11. Равновесие в системах газ-жидкость. Закон Генри. Уравнение равновесной зависимости. Влияние давления и температуры на абсорбцию.
- •12. Равновесие в процессах пар-жидкость для идеальных смесей. Закон Рауля. Диаграммы t-X,y и y-X.
- •13.Принципиальная схема противоточной абсорбции и графическое изображение процесса.
- •14.Принципиальная схема абсорбции с рециркуляцией жидкости и графическое изображение процесса.
- •15. Схема ректификационной установки непрерывного действия. Материальный баланс ректификационной колонны. Флегмовое число.
- •16.Уравнение рабочих линий процесса ректификации для непрерывно действующей ректификационной колонны. Минимальное и оптимальное флегмовое число.
- •17.Изображение рабочих линий ректификации в диаграмме y-X.
- •18.Влияние флегмового числа на размеры ректификационной колонны и расход тепла при ректификации. Оптимальное флегмовое число.
- •19.Схема периодически действующей ректификационной установки. Рабочие линии процессов с переменным и постоянным флегмовым числом.
- •20.Схема периодически действующей ректификационной установки. Изображение процесса в y-X диаграмме при постоянном составе дистиллята.
- •21.Тепловой баланс процесса ректификации.
- •22.Построение кинетической кривой и определение реального числа тарелок.
- •23. Порядок расчета ректификационной тарельчатой колонны.
- •27.Непрерывная противоточная экстракция .Материальный баланс.Графическое изображение процесса.
- •28. Ступенчатая противоточная экстракция. Принципиальная схема. Графическое изображение процесса.
- •29. Многократная экстракция с противотоком растворителя.
- •30. Массопередача в системах с твердой фазой. Массопроводность. Дифференциальные уравнения массопроводности.
- •Процесс сушки. Технические способы проведения процесса. Виды связи влаги с материалом.
- •32.Основные способы сушки. Материальный баланс конвективной сушки.
- •33.Диаграмма состояния влажного воздух (диаграмма Рамзина).
- •34.Изображение в диаграмме н-х процессов изменения параметров влажного воздуха: температура точки росы, охлаждение, нагревание, смешение.
- •36. Тепловой баланс воздушной сушки. Уравнение рабочей линии процесса сушки.
- •37. Параметры, влияющие на процесс сушки. Способы интенсификации сушки.
- •38. Сушка с многократным промежуточным подогревом воздуха. Принципиальная схема. Изображение в н-х диаграмме.
- •39. Сушка с частичным возвратом отобранного воздуха. Принципиальная схема. Изображение в н-х диаграмме.
- •40. Сушка с замкнутой циркуляцией сушильного агента. Принципиальная схема. Изображение в н-х диаграмме.
- •41. Процесс адсорбции. Динамическая и статическая активность адсорбентов. Условия, влияющие на проведение процесса адсорбции.
- •42. Физическая сущность процесса адсорбции. Адсорбенты. Условия, способствующие протеканию процесса адсорбции.
- •43. Ионообменные процессы – основные закономерности, область применения. Регенерация ионитов.
- •44. Кристаллизация. Основные способы проведения кристаллизация. Равновесие в процессах кристаллизации.
- •45. Мембранные процессы. Классификация мембранных процессов в зависимости от их механизма. Область применения.
- •46. Влияние различных параметров на селективность и проницаемость мембран.
- •47. Материальный и тепловой баланс изогидрической кристаллизации
- •48. Материальный и тепловой баланс кристаллизации с удалением части растворителя (это изотермическая кристаллизация).
14.Принципиальная схема абсорбции с рециркуляцией жидкости и графическое изображение процесса.
Абсорбция – поглощение газов или паров из газовых или паровых смесей жидкими поглотителями, называемыми абсорбентами. Процесс абсорбции обратим, обратный ему – десорбция. Ж→Г,П
Два вида: 1) физическая абсорбция (растворение газа не сопровождается химической реакцией); 2) хемосорбция (абсорбируемый компонент вступает в хим. реакцию в жидкой фазе.)
В химической технике используют следующие принципиальные схемы абсорбционных процессов: прямоточные, противоточные, одноступенчатые с рециркуляцией и многоступенчатые с рециркуляцией.
Схемы с рециркуляцией предусматривают многократный возврат в аппарат либо жидкости, либо газа. Схема с рециркуляцией жидкости показана на рис. 12.3.,а.Газ проходит через аппарат снизу вверх, и концентрация распределяемого вещества в нем изменяется от Yн до Yк. Поглощающая жидкость подводится к верхней части аппарата при концентрации распределяемого вещества Хн, затем смешивается с выходящей из аппарата жидкостью, в результате чего концентрация повышается до Хс. Рабочая линия представляется на диаграмме отрезком прямой; крайние точки его имеют координаты Хн,Хк и Yк,Хс соответственно. Значение Хс легко найти из уравнения материального баланса.
Обозначим отношение количества поглощающей жидкости на входе в аппарат к количеству свежей поглощающей жидкости через n. Тогда
G(Yн-Yк) = L(Xк-Xн) = Ln(Xк-Xс)
Xc=[Xк(n-1)+Xн]/n
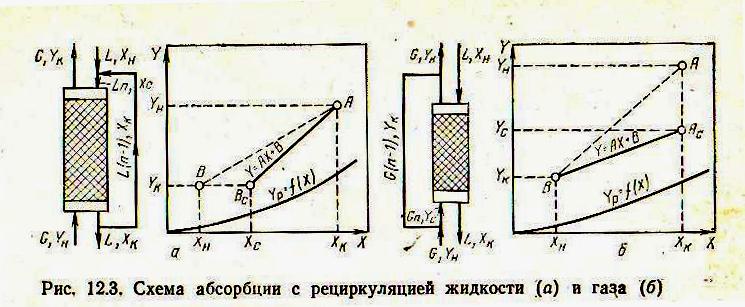
С рециркуляцией жидкого компонента: лимитирующая стадия – растворение компонента (т.е.βх - низкое). L увеличивается → Re↑ → Nuд↑ → βх↑. Процесс абсорбции идет с выделением тепла, поэтому его необходимо проводить при пониженных температурах (использовать холодильник). → βх вновь ↑.
С рециркуляцией газовой фазы: лимитирующая стадия – в газовой фазе. Жидкость хорошо растворяет компонент газовой фазы. βy – низкий. Увеличиваем G → Re↑ → Nuд↑ → βy↑. Процесс все равно идет с выделением тепла. Теплоемкость газа незначительна.
15. Схема ректификационной установки непрерывного действия. Материальный баланс ректификационной колонны. Флегмовое число.
Ректификация – разделение жидких однородных смесей на составляющие вещества или группы составляющих веществ в результате противоточного взаимодействия паровой смеси и жидкой смеси.
Непрерывно действующие ректификационные установки в зависимости от назначения работают по различным схемам. Далее будут рассмотрены: 1) установки для ректификации исходной смеси на две составляющие части в аппарате, обеспечивающем как укрепление, так и исчерпывание летучего компонента;2) установки для экстрактивной и азеотропной ректификации; 3) установки для ректификации многокомпонентных смесей.
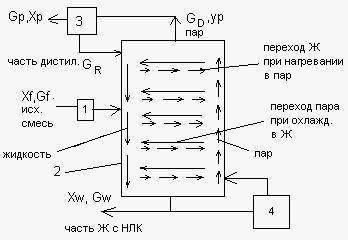 Установка для разделения исходной
смеси на две составляющие части приведена
на рис. Исходная смесь поступает в
подогреватель 1, где ее температура
повышается за счет тепла греющего
водяного пара до температуры кипения.
Нагретая смесь поступает в питающую
секцию ректификационной колонны 2 ,
присоединяясь к орошению, которое
обеспечивается концентрацией паров в
дефлегматоре 3. Необходимое для проведения
ректификации многокомпонентное испарение
жидкости осуществляется в кипятильнике
4. В дефлегматоре 3 происходит полная
конденсация паров. Из делителя потока
часть дистиллята отвечающая флегме,
возвращается в колонну, а остальная
часть удаляется. Менее летучая часть
исходной смеси непрерывно отбирается
из нижней части ректификационного
аппарата.
Установка для разделения исходной
смеси на две составляющие части приведена
на рис. Исходная смесь поступает в
подогреватель 1, где ее температура
повышается за счет тепла греющего
водяного пара до температуры кипения.
Нагретая смесь поступает в питающую
секцию ректификационной колонны 2 ,
присоединяясь к орошению, которое
обеспечивается концентрацией паров в
дефлегматоре 3. Необходимое для проведения
ректификации многокомпонентное испарение
жидкости осуществляется в кипятильнике
4. В дефлегматоре 3 происходит полная
конденсация паров. Из делителя потока
часть дистиллята отвечающая флегме,
возвращается в колонну, а остальная
часть удаляется. Менее летучая часть
исходной смеси непрерывно отбирается
из нижней части ректификационного
аппарата.
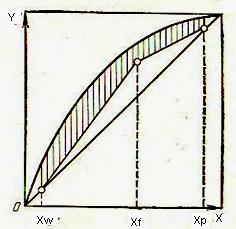
В рассмотренной схеме не учитывается возможность рационального использования тепла. Практически тепло отходящих потоков можно использовать для нагревания входящих, и в частности, нагревать исходную смесь за счет тепла жидкости, удаляющейся из нижней части колонны. Зависимость между рабочим и равновесными концентрациями показаны на рисунке 12.21; они позволяют находить движущую силу процесса для любой рабочей концентрации.
Материальный баланс
Gw – количество кубовой жидкости(содержит НЛК)
Gp-Дистилят (Содержит ЛЛК)
Gr - флегма
Х – массовые % или массовые доли
Gf=Gp+Gw
Gfхf=Gpxp+Gwxw
Gf/Gp=F - сколько исходной смеси(кг) надо направить в колонну, чтобы получить 1 кг дистиллята
Gw/Gp=W – сколько кг кубовой жидкости необходимо отвести из колонны, чтобы получить 1кг дистиллята.
Gd=Gp+GR
Gd/Gp=D – какле кол-во пара необходимо отвести из верхней части колонны, чтобы получить 1кг дистиллята.
Gd/Gp=D=1+GR/Gp
GR/Gp=R - флегмовое число, это то количество флегмы, которое необходимо возвратить в колонну, чтобы получить 1 кг дистиллята
D= 1+R
