
Экспериментальная часть
Высококремнеземный цеолит с силикатным модулем 40 синтезировали в гидротермальных условиях из щелочных алюмокремнегелей с использованием в качестве структурообразующей добавки гексаметилендиамина (ГМДА). Источником кремния служило жидкое стекло состава: 29 % SiO2, 9 % Na2O, 62 % H2O, алюминия – 9-водный азотнокислый алюминий.
Получение жидкого стекла
Жидкое стекло готовили растворением 429 г кремневой кислоты в 771,4 г 18 % раствора едкого натра(139 г NaOH в 632 г H2O). Полученную смесь помещали в автоклав емкостью 1 л и нагревали до 150-170 оС в атмосфере аргона при давлении 20-25 атм. в течение 3 ч при постоянном перемешивании. Затем автоклав охлаждали до 70-90 оС также при постоянном перемешивании. Полученное жидкое стекло выливали в подготовленную емкость и остужали до комнатной температуры.
Состав жидкого стекла: 29 % SiO2, 9 % Na2O, 62 % H2O.
Синтез алюмосиликата (М=40) с жидким стеклом
Находим количество моль SiO2:
М SiO2=60, 29:60=0,483 моль SiO2
2) Находим количество моль Al2O3:
У
нас
![]() =40;
=40;
![]() =40;
Al2O3=0,012
моль
=40;
Al2O3=0,012
моль
У нас 9-водный азотнокислый алюминий.
Al2O3 - Al(NO3)3*9H2O; М Al(NO3)3*9H2O=375
1 моль - 2 моль
0,012*2*375=9 г Al(NO3)3*9H2O
3) Определяем количество органической добавки:
![]() =0,85,
МNa2O=62
=0,85,
МNa2O=62
Na2O - 2 Na
62 - 2*23 x=6,68 г
9 - x
Находим количество моль Na: 6,68/23=0,29 моль Na
![]() =0,85;
R=0,05;
R=гексаметилендиамин(ГМДА);
МR=116
=0,85;
R=0,05;
R=гексаметилендиамин(ГМДА);
МR=116
m(ГМДА)= 116*0,05=5,8 г
ИТОГО: 100 г жидкого стекла
5,8 г ГМДА в 50 мл H2O
9 г Al(NO3)3*9H2O в 50 мл H2O
0,25 г «затравки»
К жидкому стеклу при перемешивании добавляем «затравку» и по каплям через капельную воронку сначала раствор ГМДА, затем раствор соли алюминия и для создания определенной pH среды (pH ≈10,5) 0,1 н HNO3.
Полученную реакционную смесь загружаем в стальной автоклав емкостью 0,5 л, помещаем в сушильный шкаф, в котором выставлена температура 175 оС, и в стационарном режиме выдерживаем автоклав в течение 5 суток. При этом в автоклаве создается избыточное давление 10-15 атм.
После окончания кристаллизации твердую фазу отделяли от жидкой фильтрованием, промывали дистиллированной водой до рН промывных вод 9, сушили в атмосфере воздуха при 110 оС в течение 24 ч и прокаливали для удаления ГМДА при 550 оС в течение 8 ч.
Для перевода в активную Н-форму полученный образец обрабатывали 25%-ным водным раствором NH4Cl при 90 оС в течение 2 ч при расходе 10 г раствора на 1 г цеолита. После удаления катионов натрия цеолиты в NH4-форме сушили при 110 оС и прокаливали в атмосфере воздуха при 540 оС в течение 6 ч для получения Н-формы ВКЦ.
Обсуждение результатов
Контроль за качеством полученного образца осуществляли с помощью метода ИК-спектроскопии. ИК-спектр исследуемого цеолита снимали на ИК-фурье спектрометре Nicolet 5700 в области 2000-400 см–1 в таблетках с KBr (1,2 мг цеолита на 300 мг KBr) на воздухе.
ИК-спектр полученного цеолита представлен на рис. 2. Данные ИК-спектроскопии цеолита указывают на то, что синтезированный образец имеет характерные для высококремнеземных цеолитов полосы поглощения. Так, полоса поглощения в области 550-560 см-1, относящаяся к колебаниям по внешним связям тетраэдров Al, SiO4 каркаса, обусловлена присутствием сдвоенных 4-х, 5-ти и 6-ти членных колец и определяет структуру цеолита. Наличие данной полосы поглощения в ИК-спектре цеолита указывает на его принадлежность к семейству пентасила. Отношение интенсивностей полос поглощения 550/450 см-1 позволяет судить о чистоте синтезированного образца и степени его кристалличности. Для полученного образца это отношение больше 0,8 (60/73=0,82), что говорит о достаточно высокой степени кристалличности. Отсутствие полосы поглощения при 960 см-1 так же подтверждает высокую степень кристалличности образца и указывает на отсутствие в их составе примеси аморфной фазы.
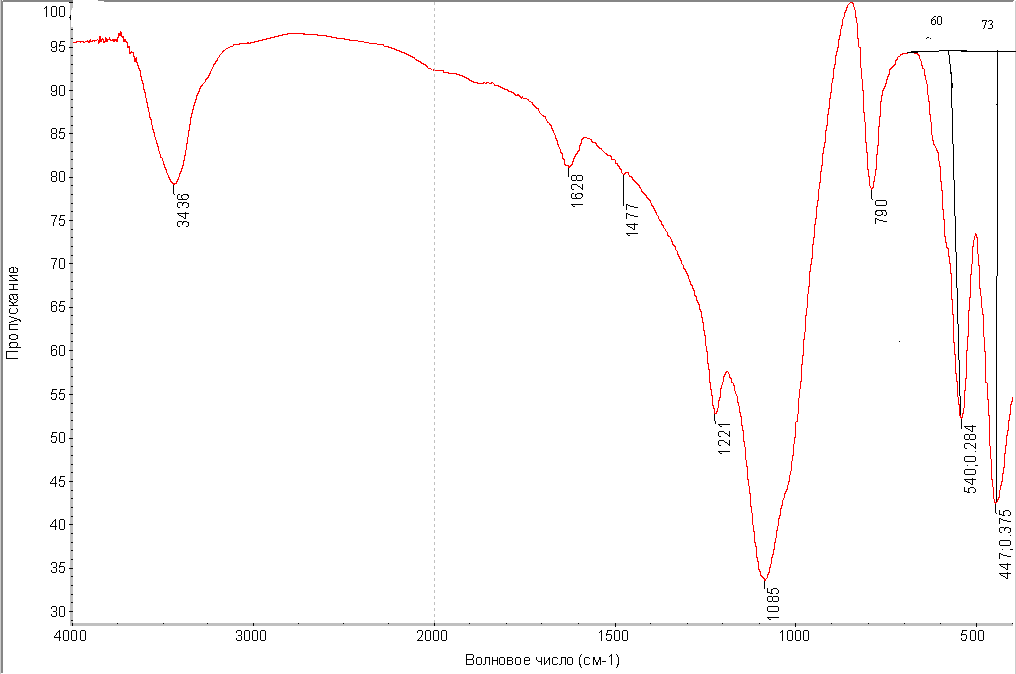
Рисунок 2. ИК-спектр алюмосиликатного катализатора.
Другой способ определения степени кристалличности полученного катализатора заключается в определении оптической плотности. На рисунке 3 представлен график взаимосвязи оптической плотности и степени кристалличности.

Рисунок 3. Зависимость степени кристалличности от оптической плотности.
Оптическая плотность полученного образца составляет 0,757. По графику определяем, что степень кристалличности по данному методу составляет 97 %.
Алюмосиликатные катализаторы в Na-форме не активны в процессе ароматизации низших алканов. Для перевода в активную Н-форму полученный образец обрабатывали 25%-ным водным раствором NH4Cl при 90 оС в течение 2 ч при расходе 10 г раствора на 1 г цеолита.
Выход катализатора составил 27 г. Для декатионирования требуется 270 г 25% р-ра NH4Cl:
100 г - 25 г NH4Cl х=270*25:100=67,5 г NH4Cl
270 г - х г
270 г -67,5 г=202,5 г H2O
Растворяем 67,5 г NH4Cl в 202,5 г H2O и заливаем полученным раствором цеолит. Полученную смесь ставим на водяную баню при 90 оС и непрерывно перемешиваем при этой температуре в течение 2 часов. После окончания декатионирования твердую фазу отделяли от жидкой фильтрованием, промывали дистиллированной водой. После удаления катионов натрия цеолиты в NH4-форме сушили при 110 оС и прокаливали в атмосфере воздуха при 540 оС в течение 6 ч для получения Н-формы ВКЦ.
ВЫВОДЫ
Методом гидротермального синтеза с использованием в качестве структурообразователя ГМДА получен алюмосиликатный цеолитный катализатор.
Полученный образец алюмосиликатного катализатора обладает высокой степенью кристалличности и не содержит примесей аморфной фазы.
Н-форма синтезированного катализатора будет использована в качестве катализатора ароматизации пропана.
