
- •Билет №1
- •1. Круговые процессы. Обратимые и необратимые процессы. Цикл Карно.
- •2. Постоянный электрический ток. Закон Ома в дифференциальной форме.
- •Билет №2
- •Угловая скорость, угловое ускорение.
- •Энтропия. Іі начало термодинамики
- •3. Определить напряженность поля в точке, указанной на рисунке. Билет №3
- •Механический принцип относительности. Преобразования координат Галилея.
- •Потенциал электрического поля. Связь потенциала с напряженностью
- •Какой объем занимают 10 г водорода при давлении 750 мм. Рт. Столба и температуре 200с.
- •Билет №4
- •Нормальное и тангенциальное ускорение.
- •Распределение молекул по скоростям. Распределение Максвелла, и его экспериментальная проверка
- •Билет №5
- •Элементы кинематики материальной точки. Скорость и ускорение как производные радиус-вектора по времени.
- •Ток, его характеристики и условия существования. Плотность тока. Закон Ома.
- •Билет №6
- •Закон сохранения момента импульса.
- •Уравнение и изотермы Ван-дер-Ваальса. Внутренняя энергия реального газа.
- •Билет №7
- •Инерциальные системы отсчета. Законы Ньютона.
- •II закон Ньютона справедлив только для инерциальных систем отсчета!
- •Если на материальную точку действует одновременно несколько сил, то каждая из них сообщает материальной точке ускорение согласно второму закону Ньютона, как будто других сил не было.
- •Энтропия. Іі начало термодинамики.
- •Билет №8
- •Работа газа. І начало термодинамики.
- •Проводники в электрическом поле. Распределение зарядов в проводнике.
- •Билет №9
- •Кинетическая энергия вращающегося тела.
- •Электроемкость. Конденсаторы.
- •Билет №10
- •1.Применение I начала термодинамики к адиабатическому процессу.
- •2. Электрическое поле. Напряженность поля. Расчет полей методом суперпозиции.
- •Билет №11
- •Второе начало термодинамики. Энтропия.
- •Явление электромагнитной индукции. Закон Фарадея.
- •Билет №12
- •Теплоемкость идеального газа. Уравнение Майера.
- •Закон Био-Савара-Лапласа.
- •Билет №13
- •Цикл Карно. Тепловые и холодильные машины.
- •Магнитное поле бесконечного прямолинейного проводника с током. Магнитное поле кругового тока.
- •Билет №14
- •Cилы инерции. Импульс. Закон сохранения импульса.
- •Работа при перемещении проводника с током в магнитном поле
- •Билет №15
- •Кинетическая энергия вращающегося тела.
- •Ферромагнетики. Доменная структура.
- •Билет №16
- •Внутренняя энергия идеального газа.
- •Билет №17
- •Адиабатический процесс. Цикл Карно.
- •Магнитное поле в магнетиках. Намагниченность. Магнитная восприимчивость.
- •Билет №18
- •Основное уравнение молекулярно-кинетической теории газов.
- •Поток вектора напряженности электрического поля. Теорема Остроградского - Гаусса.
- •Билет №19
- •Движение материальной точки по окружности. Угловая скорость, угловое ускорение.
- •Самоиндукция. Индуктивность. Взаимоиндукция
- •Билет №20
- •Момент силы. Момент инерции. Момент импульса. Закон сохранения момента импульса.
- •Изопроцессы. Уравнение состояния идеального газа
- •Билет №21
- •Степени свободы молекул. Распределение энергии по степеням свободы молекул
- •Правила Кирхгофа
- •Билет №22
- •Импульс. Закон сохранения импульса.
- •Явление взаимоиндукции. Трансформаторы.
- •Билет №23
- •Основной закон динамики вращательного движения.
- •Напряженность электрического поля. Принцип суперпозиции по лей.
- •Билет №24
- •Изопроцессы. Уравнение состояния идеального газа.
- •3. Определить напряженность в точках, указанных на рисунке:
Билет №16
Внутренняя энергия идеального газа.
В теории идеального газа потенциальная энергия взаимодействия молекул считается равной нулю. Поэтому внутренняя энергия идеального газа определяется кинетической энергией движения всех его молекул. Средняя энергия движения одной молекулы равна
![]()
Так
как в одном киломоле содержится ![]() молекул,
то внутренняя энергия одного киломоля
газа будет
молекул,
то внутренняя энергия одного киломоля
газа будет
![]() Учитывая,
что
Учитывая,
что ![]() ,
получим
,
получим
![]()
Для
любой массы m газа, т.е. для любого числа
киломолей ![]() внутренняя
энергия
внутренняя
энергия
![]()
Из этого выражения следует, что внутренняя энергия является однозначной функцией состояния и, следовательно, при совершении системой любого процесса, в результате которого система возвращается в исходное состояние, полное изменение внутренней энергии равно нулю. Математически это записывается в виде тождества
![]()
Закон Ома в дифференциальной форме.
Закон Ома в интегральной форме для однородного участка цепи (не содержащего ЭДС)
Для однородного линейного проводника выразим R через ρ:
ρ – удельное объемное сопротивление; [ρ] = [Ом·м].
Найдем связь между и в бесконечно малом объеме проводника – закон Ома в дифференциальной форме.
В изотропном проводнике (в данном случае с постоянным сопротивлением) носители зарядов движутся в направлении действия силы, т.е. вектор плотности тока и вектор напряженности поля коллинеарны (рис. 7.6).
Рис. 7.6
Исходя из закона Ома, имеем:
А мы знаем, что или . Отсюда можно записать
это запись закона Ома в дифференциальной форме.
Здесь – удельная электропроводность.
Размерность σ – [ ].
Плотность тока можно выразить через заряд электрона е, количество зарядов n и дрейфовую скорость :
.
Обозначим , тогда ;
Теперь, если удельную электропроводность σ выразить через е, n и b: то вновь получим выражение закона Ома в дифференциальной форме:
.
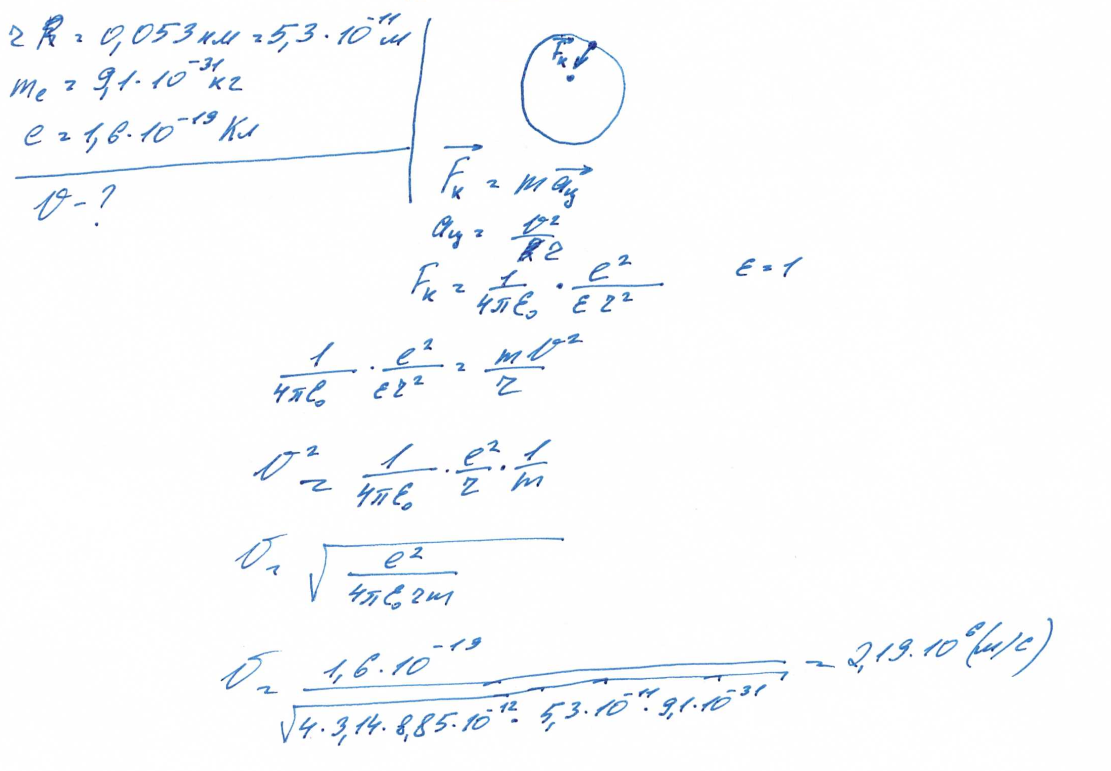
В элементарной теории атома водорода принимают, что электрон обращается вокруг ядра по круговой орбите. Определить скорость электрона, если радиус вращения r = 0,053 нм. (me = 9,1 10-31кг, е = 1,6 10-19Кл).
Билет №17
Адиабатический процесс. Цикл Карно.
Адиабатический процесс - это процесс, при котором отсутствует теплообмен с окружающей средой, следовательно, dQ = 0. К адиабатическим процессам можно отнести все быстро протекающие процессы. Например, процесс распространения звука в среде. Скорость распространения звука настолько велика, что процесс обмена энергией между звуковой волной и средой произойти не успевает и т.д. и т.п.
Из I начала термодинамики получают, что dA = –dU, т.к. dQ = 0, т.е. внешняя работа совершается за счет изменения внутренней энергии системы. Для произвольной массы газа имеем:
Если продифференцировать уравнение Менделеева-Клапейрона, то получим
Исключив T, получим
Интегрирую обе части от P1 до P2 и от V1 до V2, получим
Т.к. состояния 1 и 2 выбраны произвольно, то можно записать, что
PV = const.
Полученный результат есть уравнение адиабатического процесса, или уравнение Пуассона. Перейдя к переменным T и V или к переменным P и T, используя уравнение Менделеева-Клапейрона, получим
TV –1 = const; T P 1– = const.
Эти формулы тоже выражают уравнение Пуассона, только в других параметрах.
Для одноатомных газов i = 3, = 1,67; для двухатомных газов i = 5, = 1,4.
Значение , вычисленное по формуле, хорошо подтверждается экспериментом.
Диаграмма адиабатического процесса изображается гиперболой.
Вычислим работу, совершаемую газом в адиабатическом процессе. Если газ адиабатически расширяется от V1 до V2, то его температура уменьшается от T1 до T2.
Произведя некоторые преобразования, можно перейти к виду
Работа, совершаемая газом при адиабатическом расширении, меньше, чем при изотермическом. Это можно объяснить тем, что при адиабатическом расширении происходит охлаждение газа, тогда как при изотермическом – температура поддерживается постоянно за счет притока извне эквивалентного количества теплоты.
Рассмотренные процессы имеют общую особенность – они проходят при постоянной теплоемкости; в первых двух процессах они соответственно равны CV и CP. При изотермическом процессе dt = 0, теплоемкость равна . В адиабатическом процессе dQ = 0, следовательно, теплоемкость тоже равна нулю.
Процесс, при котором теплоемкость остается постоянной, называется политропным.
Исходя из I начала термодинамики, при условии, что теплоемкость постоянна, выводится уравнение политропы:
Очевидно, что при C = 0 n = , получаем уравнение адиабаты. При C = n = 1, получаем уравнение изотермы. При C = CP n = 0, получаем уравнение изобары. При C = CV n = , получаем уравнение изохоры. Таким образом, все процессы являются частным образом от изотропного процесса.
Анализируя работу тепловых двигателей, французский инженер С. Карно в 1824г. пришел к выводу, что наивыгоднейшим круговым процессом является обратимый круговой процесс, состоящий из двух изотермических и двух адиабатических процессов, т.к. он характеризуется наибольшим коэффициентом полезного действия. Такой цикл получил название цикла Карно. В прямом цикле Карно рабочее тело изотермически, а затем адиабатически расширяется, после чего снова изотермически (при более низкой температуре) и потом адиабатически сжимается. Т.е. цикл Карно ограничен двумя изотермами и двумя адиабатами.
При изотермическом расширении от нагревателя отбирается тепло (на участке 1-2 рис. 9.11). Вследствие этого температура газа поддерживается неизменной. Соответственно, параметры точки 2 будут равны . На участке 2-3 происходит адиабатное расширение. Внутренняя энергия газа уменьшается и его температура падает до Т2. Параметры точки 3 - . На участке 3-4 газ изотермически сжимается. Параметры точки 4 - . Выделяющееся при этом тепло отбирается холодильником. Участок 4-1 -адиабатическое сжатие до исходного состояния, соответствующего точке 1. Таким образом, завершен цикл “1-2-3-4-1 и в итоге нагреватель отдал газу теплоту , а холодильник отобрал Разность определяет полезную работу газа за один цикл, так как согласно I началу термодинамики , но для кругового процесса и, следовательно .
Отношение полезной работы к затраченной энергии нагревателя определяет коэффициент полезного действия (к.п.д.) тепловой машины:
Эта формула справедлива для любого обратимого и необратимого процесса.
Определим коэффициент полезного действия цикла Карно для обратимого процесса. Теплота подводится на участке 1-2 и отводится на участке 3-4. Для изотермического процесса внутренняя энергия Q=const и все подводимое тепло расходуется на работу .
Тогда или Для изотермического процесса работа С учетом последних выражений
Покажем, что
Так как процессы на участках 2-3 и 1-4 адиабатические, для определения связи между и и и используем уравнение Пуассона в виде
Следовательно, и Разделим эти уравнения и получим Тогда выражение для к.п.д. (9.24) примет вид
Эта формула справедлива только для обратимого цикла Карно.
Теоремы Карно.
1 Все обратимые машины, работающие по циклу Карно, имеют, е зависимо от природы рабочего тела, одинаковый КПД при условии если у них общий нагреватель и холодильник.
2 Если две тепловые машины имеют общий нагреватель и холодильник и одна обратимая, а другая необратимая, то КПД обратимой больше необратимой
