
- •2. Современные представления о строении белка. Методы определения строения белка.
- •3. Уровни структурной организации белка и их связь с его биологическими функциями.
- •4. Современные классификации белков: классификация по строению белка. Общая характеристика простых белков. Их роль.
- •5. Аминокислоты. Общая характеристика, классификация, представители. Хроматографический метод определения аминокислот.
- •6. Денатурация и деструкция белковых молекул. Какие факторы способны вызвать денатурацию белков? Значение денатурации белков в медицине? Ренатурация.
- •7. Азотистый баланс организма и его регуляция. Суточная потребность в белках. Их биологическая ценность.
- •8. Охарактеризуйте функции белков в организме.Что такое полноценные белки? Патологии белкового питания.
- •9. Переваривание белков в пищеварительном тракте. Характеристика ферментов.
- •10. Переваривание белков в желудке. Характеристика ферментов. Особенности переваривания белков в желудке у детей.
- •11.Образование соляной кислоты в желудке. Роль соляной кислоты в переваривании белков.
- •12. Переваривание белков в кишечнике.
- •13. Роль соляной кислоты, кислотность желудочного сока и его изменение при патологическом состоянии.
- •14. Современные представления о механизме всасывания аминокислот.
- •15. Внутриклеточный обмен белков. Катепсины, их локализация, мех-м действия, регуляция активности.
- •16. Процессы гниения белков в толстом кишечнике и мех-м обезвреживания токсических продуктов.
- •17. Общие пути обмена аминокислот. Дезаминирование, трансаминирование. Значение работ а.А.Браунштейна для определения путей превращения аминокислот.
- •18. Общие пути обмена аминокислот. Декарбоксилирование. Биогенные амины, роль, распад.
- •19. Образование и обезвреживание аммиака в организме.
- •20.Глутамин и аспаргин; химическая природа, образование, роль.
- •21. Современные представления про уреогенез. Нормальное содержание мочевины в крови и моче, и ее изменение при острой почечной недостаточности.
- •22.Орнитиновый цикл синтеза мочевины, его роль и связи с другими метаболическими путями.
- •23. Креатин. Биологическая роль. Обмен.
- •24. Специфический обмен циклических аминокислот, характеристика путей и образующихся веществ.
- •25. Специфический обмен серосодержащих аминокислот, характеристика путей и образующихся веществ.
- •26. Специфический обмен аминокислот. Гликогенные и кетогенные аминокислоты. Привести примеры.
- •27. Современные представления о биосинтезе белка и его регуляции.
15. Внутриклеточный обмен белков. Катепсины, их локализация, мех-м действия, регуляция активности.
16. Процессы гниения белков в толстом кишечнике и мех-м обезвреживания токсических продуктов.
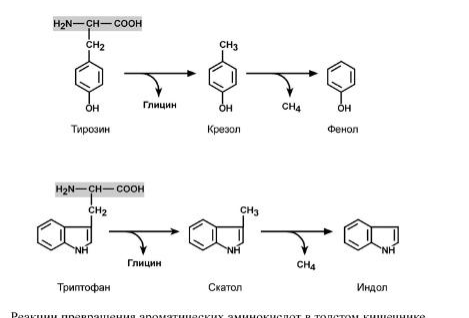
При ухудшении всасывания аминокислот, при избытке белковой пищи, при нарушении деятельности пищеварительных желез недопереваренные фрагменты белков достигают толстого кишечника, где подвергаются воздействию кишечной микрофлоры. Этот процесс получил название гниение белков в кишечнике. При этом образуются продукты разложения аминокислот, представляющие собой кактоксины (кадаверин, путресцин, крезол, фенол, скатол, индол, пиперидин, пирролидин, сероводород и метилмеркаптан (СН3SН)), так инейромедиаторы (серотонин, гистамин, октопамин, тирамин).
Гниение белков также активируется при снижении перистальтики кишечника (запоры).
17. Общие пути обмена аминокислот. Дезаминирование, трансаминирование. Значение работ а.А.Браунштейна для определения путей превращения аминокислот.
Общие пути превращения аминокислот включают реакции дезаминирования, трансаминирования, декарбоксилирования, биосинтеза и рацемизации. Реакции рацемизации характерны только для микроорганизмов, физиологическая роль которой заключается в синтезе D-изомеров аминокислот для построения клеточной оболочки.
Дезаминирование ( отщепление аминогруппы) – существует четыре типа реакций, катализируемых своими ферментами:
Восстановительное дезаминорование ( +2H+)
Гидролитическое дезаминированиие (+H2О)
Внутримолекулярное дезаминирование
Окислительное дезаминирование (+1/2 О2)
Во всех случаях NH2- группа аминокислоты высвобождается в виде аммиака. Помимо аммиака продуктами дезаминирования являются жирные кислоты, окикислоты и кетокислоты. Для животных тканей, растений и большинства микроорганизмов преобладающим типом реакций является окислительное дезаминирование аминокислот, за исключением гистидина, который подвергается внутримолекулярному дезаминированию.
Кроме перечисленных четырех типов реакций и катализирующих их ферментов в животных тканях и печени человека открыты также три специфических фермента (серин- и треониндегидратазы и цистатионин-γ- лиаза), катализирующих неокислительное дезаминирование серина, треонина и цистеина. Они требуют присутствия пиридоксаль-фосфата в качестве кофермента. Конечными продуктами реакции являются пируват и α- кетобутират, аммиак и сероводород.Трансаминирование – реакции межмолекулярного переноса аминогруппы (NH2) от аминокислоты на α-кетокислоту без промежуточного образования аммиака (глутамат+ пируват =α-кетоглутарат + аланин). Впервые эти реакции были открыты в 1937г. А.Е. Браунштейном и М.Г. Крицман. Реакции трансаминирования являются обратимыми и универсальными для всех живых организмов, они протекают при участии специфических ферментов – аминотрансфераз (трансамниназ). Теоретически реакции возможны между любой амино- и кетокислотой, но наиболее интенсивно они протекают, если один из партнеров представлен дикарбоновой амино- или кетокислотой. В переносе амниогруппы активное участие принимает кофермет трансминаз – пиридоксальфосфат (производное витамина В6). Для реакций трансаминирования характерен общий механизм. Ферменты реакции катализируют перенос аминогруппы не на α -кетокислоту, а на кофермент; образовавшееся промежуточное соединение (шиффово основание) подвергается внутримолекулярным превращениям, приводящим к освобождению α-кетокислоты и пиридоксамнофосфата. Последний на втолрой стадии реагирует с любой другой α-кетокислотой, что через те же стадии приводит к синтезу новой аминокислоты и пиридоксальфосфата.Декарбоксилирование - отщепление карбоксильной группы в виде СО2, образующиеся продукты реакции называются биогенными аминами, они оказывают сильное фармакологическое действие на множество функций. Эти реакции являются необратимыми, они катализируютя специфическими ферментами – декарбоксилазами аминокмлот- которые в качестве кофермента содержат пиридоксальфосфат ( кроме гистидиндекарбоксилазы и аденозилдекарбоксилазы – содержат остаток пировиноградной кислоты в качестве кофермента). В живых организмах открыты четыре типа декарбоксилирования аминокислот.
α-декарбоксилирование – характерно для тканей животных: от аминокислот отщепляется соседняя от α-углеродного атома карбоксильная группа.
ω-декарбоксилирование- свойственно микроорганизмам декарбоксилирование, связанное с реакцией трансаминирования. Образуется альдегид и новая аминокислота, соответствующая исходной кетокислоте.
Декарбоксилирование, связанное с реакцией конденсацией двух молекул.
