
- •Лекция 24 карбонильные соединения
- •Насыщенные альдегиды и кетоны
- •Способы получения альдегидов и кетонов
- •2. Гидроформилирование алкенов (оксосинтез)
- •4. Термическое разложение Са- и Ва-солей карбоновых кислот
- •6. Окисление алканов кислородом воздуха:
- •7. Окисление алкенов сильными окислителями:
- •8. Реакция Кучерова:
- •Физические свойства альдегидов и кетонов
- •Химические свойства альдегидов и кетонов
- •Реакции нуклеофильного присоединения к карбонильной группе
- •2. Присоединение спиртов.
- •Основной катализ
- •Лекция 25 карбонильные соединения
- •Реакции с участием α-водородного атома
- •2. Галогенирование альдегидов и кетонов
- •Окислительно–восстановительные реакции
- •Отдельные представители
- •Ненасыщенные альдегиды и кетоны
- •Химические свойства
- •Конденсация формальдегида с ацетоном:
- •Химические свойства
- •Лекция 26 карбонильные соединения
- •1. Классификация и номенклатура.
- •Способы получения.
- •Каталитическое окисление боковой цепи:
- •Гидролиз геминальных дигалогенпроизводных:
- •Введение карбонильной группы в ароматическое ядро
- •Физические свойства
- •Химические свойства
- •Отдельные представители
- •Часть 4
- •Химические свойства хинонов
Лекция 24 карбонильные соединения
Схема лекции.
1. Классификация и номенклатура.
2. Способы получения альдегидов и кетонов.
3. Физические свойства альдегидов и кетонов.
4. Химические свойства альдегидов и кетонов.
4.1. Строение карбонильной группы.
4.2. Реакции нуклеофильного присоединения к карбонильной группе.
Насыщенные альдегиды и кетоны
Альдегиды и кетоны относятся к карбонильным соединениям (содержат группу >С=О) и имеют общую формулу
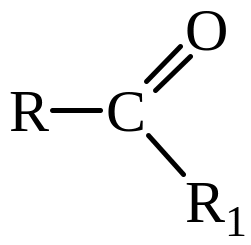
для альдегидов R1=Н, R=Alk, для кетонов R=R1=Alk
Изомерия альдегидов связана со строением радикалов. Альдегиды называют или по названию тех кислот, в которые они превращаются при окислении (тривиальная номенклатура) или, выбрав за основу самую длинную цепь углеродных атомов, включающую альдегидную группу, прибавляют к ее названию окончание -аль (номенклатура IUPAC).
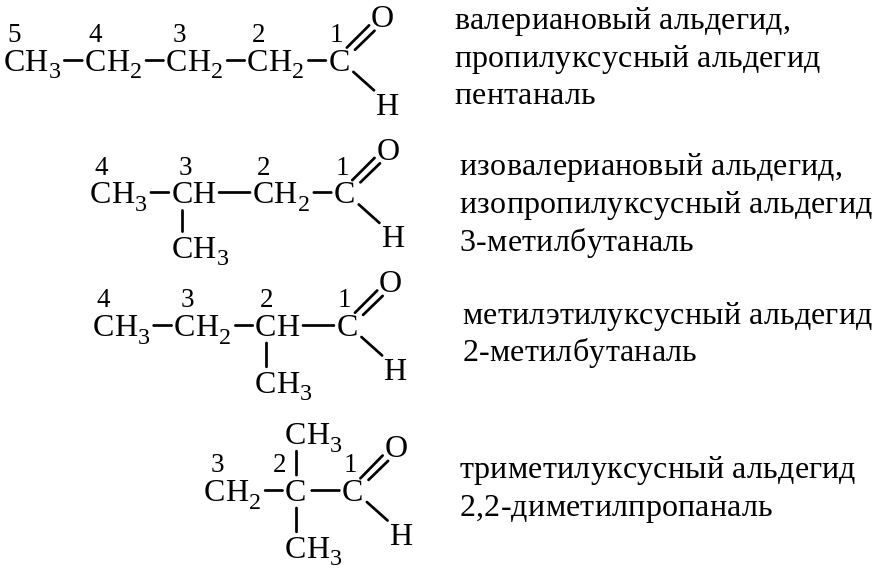
Когда альдегидная группа младшая она обозначается префиксом – оксо.
Изомерия кетонов связана со строением радикалов и с положением карбонильной группы в углеродной цепи. Кетоны называют по заместительной номенклатуре ИЮПАК аналогично альдегидам, но прибавляют окончание -он. Кетоны называют также по радикально-функциональной номенклатуре ИЮПАК. Кроме того, широко используются исторически сформировавшиеся (тривиальные) названия:

Способы получения альдегидов и кетонов
Альдегиды и кетоны могут быть получены окислением алкенов (кислородом в присутствии солей палладия и озоном), спиртов и гидратацией алкинов.
Промышленное значение имеет метод гидроформилирования алкенов (оксосинтез).
1. Из спиртов. Дегидрированием спиртов получают многие альдегиды и кетоны, но в настоящее время процесс сохранил свое значение только для получения формальдегида (катализатор Cu):
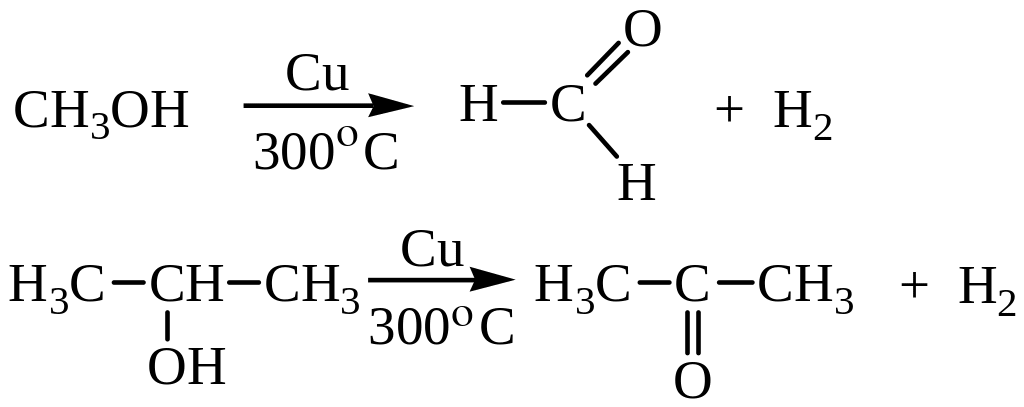
Промышленным способом получения является окисление спиртов. В качестве окислителей применяют K2Cr2O7/разб. H2SO4, Cr2O3/разб. H2SO4. Окислением первичных спиртов получают альдегиды, вторичных – кетоны.
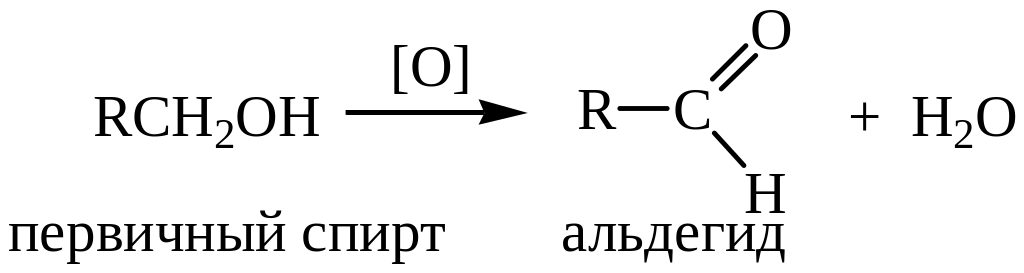
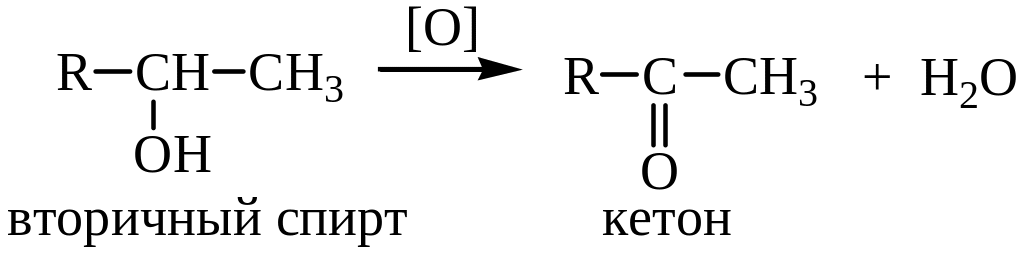
2. Гидроформилирование алкенов (оксосинтез)
Реакция открыта Реленом в 1938 г. (100-200оС, 100-250 атм СО, катализатор - ThO2+mgo на кизельгуре). Процесс (оксосинтез) катализируется дикобальтоктакарбонилом [Co(CО)4]2.
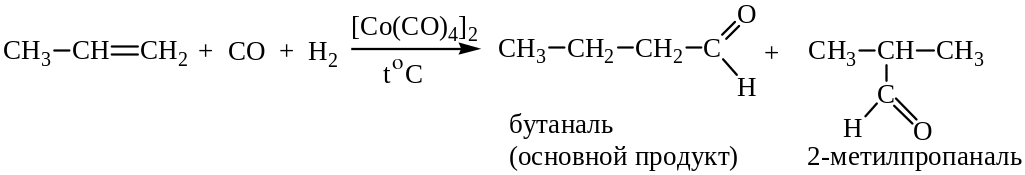
Практическое значение имеют пропионовый, н- и изомасляный альдегиды, получаемые гидроформилированием этилена и пропилена.
3. Восстановление карбоновых кислот и их производных. Прямое восстановление карбоновых кислот для получения альдегидов не применимо, так как альдегиды восстанавливаются легче, чем соответствующие кислоты. Альдегиды можно получать восстановлением хлорангидридов карбоновых кислот (реакция Розенмунда):
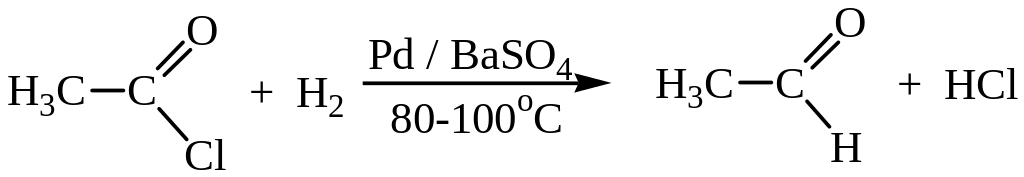
Активность катализатора снижается добавкой контактных ядов, например тетраметилтиомочевины (ТМТМ).
Одним из лучших методов восстановления хлорангидридов кислот является восстановление три-трет-бутоксиалюмогидридом лития при -78°С. Специфический восстановитель и низкая температура исключают дальнейшее восстановление альдегида до спирта.
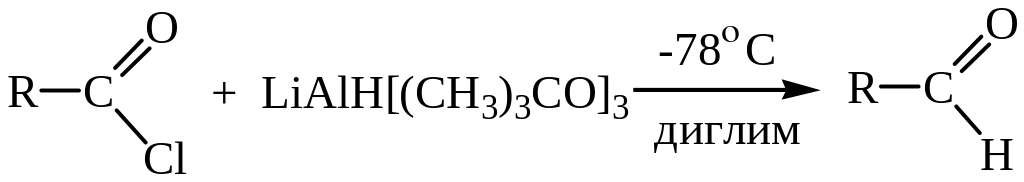
Восстановитель получают при взаимодействии 1 моля галогенидов лития с 3 молями трет-бутилового спирта.
