
МиНистерсво здравоохранения и социального развития рф
Кафедра педиатрии
Учебно-методическое пособие
для студентов педиатрических факультетов, интернов, ординаторов и врачей педиатров.
ПЕРИНАТАЛЬНАЯ И НЕОНАТАЛЬНАЯ НЕФРОЛОГИЯ:
ДИАГНОСТИКА, ОСОБЕННОСТИ ТЕЧЕНИЯ И ЛЕЧЕНИЕ ПОРАЖЕНИЙ ПОЧЕК
У НОВОРОЖДЕННЫХ ДЕТЕЙ
Введение
Поражения органов мочевой системы /ОМС/ у детей не только распространены (в среднем 29 : 1000), но и имеют тенденцию к росту, причем нередко в раннем возрасте. Ухудшение экологического фона, токсико-аллергическое воздействие лекарственных препаратов ведут к поражению в первую очередь почек, которые являются элиминирующим органом. Подавляющее большинство заболеваний почек в старшем возрасте, а иногда и у взрослых, представляют собой пролонгированную патологию плода и новорожденного. Нарастание нефропатий у новорожденных детей связывают также с увеличением частоты врожденных и наследственно-обусловленных форм, возрастанием заболеваемости матерей и перинатальной патологии, расширением реанимационной помощи новорожденным и направленным исследованием данной проблемы. Последние эпидемиологические исследования указывают, что частота заболеваний ОМС среди детского населения колеблется от 5,4 до 34,2 %, причем она значительно варьирует среди различных групп детей и максимальна /до 74 %/ у детей, родившихся в семьях с нефропатиями. Особенностью заболеваний почек у новорожденных и грудных детей является своеобразный фон - морфологическая незрелость почечной ткани и недифференцированность нефронов в функциональном отношении, а также наличие у них дисфункции иммуногенеза, дисбактериоза и своеобразия течения перинатального периода. У новорожденных детей стали чаще встречаться латентные формы нефропатий, поздно диагностируемые и рано приводящие к развитию хронических заболеваний почек и даже к формированию хронической почечной недостаточности (ХПН) уже в младенчестве. Отсутствие, нередко, заметных клинических признаков нефропатий у новорожденных вследствие их неспецифичности, требует поиска новых информативных диагностических тестов, указывающих на развитие патологического процесса в почечной ткани. Последствия поражения почек в раннем детском возрасте настолько значимы, что своевременное их выявление является проблемой не только медицинского, но и социального характера.
Своеобразие течения многих заболеваний, в частности, почек, у детей неонатального периода связано с морфологической и функциональной незавершенностью всех органов и систем ребенка к моменту рождения. Особенности организма новорожденного способствуют быстрому прогрессированию воспалительного процесса с развитием некротических и склеротических изменений в ткани почки. Однако, по мнению большинства исследователей, при этом у них наблюдается и высокая пластичность, позволяющая при ранней диагностике и своевременном вмешательстве предотвратить неблагоприятные последствия, если они не определяются генетическими факторами.
Факторы риска развития нефропатий у новорожденных детей
Основными патогенетическими механизмами развития заболеваний почек у детей перинатального периода являются гипоксия и массивная инфекция. Повреждающее воздействие на ОМС у новорожденных детей оказывают также синдром ДВС, гипербилирубинемия, метаболический ацидоз, шок, токсическое влияние лекарственных препаратов. Высокая вероятность дебюта нефропатий у новорожденных определяется наличием у них признаков морфо-функциональной незрелости почек, дисфункции иммуногенеза, дисбактериоза, своеобразия течения перинатального периода, генетических факторов, неадекватной терапией соматических заболеваний. У каждого ребенка перинатального периода, перенесшего реанимационные мероприятия, возможно развитие патологии ОМС.
Наши исследования подтверждают неблагоприятное влияние осложненного течения беременности и родов, а также соматических заболеваний у матери и родственников на возникновение нефропатий у новорожденных. Однако, отягощенный акушерский анамнез является фактором риска и других патологических состояний. У новорожденных детей в постреанимационном периоде заболевания ОМС редко бывают изолированными. Яркая их клиническая картина возникает обычно только вследствие грубых пороков развития почек. На первый план выступают симптомы поражения ЦНС, явления дыхательной и сердечно-сосудистой недостаточности. Учитывая вышеизложенное необходима настороженность педиатров в плане возможности развития у новорожденных, особенно перенесших реанимационные мероприятия, почечной патологии, и в связи с этим обязательного проведения нефрологического обследования с использованием новых скрининг-тестов.
Диагностика заболеваний почек у новорожденных детей
Диагностика заболеваний почек у новорожденных в настоящее время должна основываться на данных изучения семейного анамнеза, учета особенностей течения беременности и послеродового периода, комплексного объективного обследования и лабораторно-биохимического контроля.
Врожденные и наследственные нефропатии, как правило, выявляются случайно, нередко на фоне тяжелой соматической патологии и имеют латентное и торпидное течение. А такие нозологические формы, как инфекция мочевой системы, токсические нефропатии, острая почечная недостаточность и другие, в развитии которых велика роль экзогенных факторов, в дебюте имеют определенную клинику.
Ранней и дифференциальной диагностике поражения почек у новорожденных способствуют:
тщательный сбор анамнеза (наличие нефропатий у родственников, отягощенное течение беременности и родов);
проведение антенатальной эхографии почек, начиная с 20 недели гестации;
осмотр, во время которого обращают внимание на отечность или пастозность тканей новорожденного, увеличение размеров живота с наличием синдрома «пальпирующейся опухоли» (пальпируемые почки), задержку мочеиспускания, дизурические явления;
результаты клинических и биохимических анализов крови и мочи (мочевой синдром любой степени выраженности в виде протеинурии, лейкоцитурии, эритроцитурии, цилиндрурии, бактериурии, наличие солевого осадка, изменение реакции мочи с кислого на щелочной или нейтральный; рост флоры в посеве мочи: условно-патогенной более 100000 м. тел в 1 мл или любое количество патогенной; воспалительная реакция крови в виде лейкоцитоза и нейтрофилеза со сдвигом влево, ускорение СОЭ; азотемия по данным биохимического анализа крови, изменение уровней калия, натрия, кальция и фосфора; протеинурия, глюкозурия, оксалурия, уратурия, кальцийурия и изменение экскреции титруемых кислот и аммиака по результатам биохимического анализа мочи; снижение антикристаллообразующей способности мочи);
проведение УЗИ почек, где обращается внимание на положение и размеры почек, структуру паренхимы, ширину чашечно-лоханочного комплекса, наличие эхо-негативных дорожек;
дополнительное нефрологическое обследование для уточнения характера патологии ОМС включает: цистографию (для диагностики пузырно-мочеточникового рефлюкса, стеноза уретры, клапана задней уретры), внутривенную урографию (для определения аномалии формы и количества почек, диагностики нефроптоза, мочекаменной болезни и нарушения функционального состояния почек), радиоизотопное исследование почек (возможно определение изолированно гломерулярной и тубулярной функции отдельно правой и левой почек), допплерографию (изучение почечного кровотока), а так же исследование ферментурии и уровня Б-2-МГ в крови и моче.
По результатам многолетнего наблюдения за детьми, поступающими в неонатальный центр (отделение реанимации), а затем переводимых в отделение патологии новорожденных с различными соматическими заболеваниями, более чем у трети (34%) пациентов выявляется, по результатам обследования, нефрологическая патология.
Показанием к обязательному проведению УЗИ почек у новорожденных детей является наличие:
1) отягощенной наследственности в плане почечной патологии;
2) отечного синдрома любого генеза;
3) пальпируемого образования в брюшной полости;
4) мочевого синдрома любой степени выраженности;
5) азотемии;
6) множественных (более 6) стигм дисэмбриогенеза.
Методы ультразвуковой диагностики позволяют провести морфологическую оценку почек у детей различных возрастных групп, в том числе и у новорожденных. Однако ряд состояний имеют неспецифические и схожие морфологические проявления. Только комплексная оценка, включающая анализ клинического материала и результаты других методов исследования, позволяют поставить точный диагноз.
В качестве скрининг-теста для исключения тяжелой нефрологической патологии (гидронефроза, поликистоза почек, мультикистоза и др.) рекомендуется всем новорожденным, перенесшим реанимационные мероприятия, проведение УЗИ почек на первом месяце жизни, начиная с 3-5 суток, остальным детям – в первые 6 месяцев жизни в поликлинических условиях.
Одну из важнейших сторон перинатальной нефрологии составляет стремление к ранней диагностике с тем, чтобы предпринять адекватные меры лечения. В этом отношении мы настоятельно рекомендуем шире использовать при обследовании детей неонатального периода современные микрометоды - исследование ферментурии и уровня бета-2-микроглобулина в крови и моче у новорожденных детей.
Определение активности различных ферментов мочи перспективно для диагностики преимущественно заболеваний почек, так как основным источником ферментурии являются клетки нефротелия, влияние же других причин крайне незначительно. При повреждении различных структур канальцев и клубочков почек увеливается проницаемость клеточных мембран и разрушаются клетки, что в свою очередь индуцирует экскрецию разных ферментов или их групп из клеток в мочу. Определение активности ферментов в моче позволяет оценить степень повреждения структурно-функциональных элементов нефрона, уточнить преимущественную локализацию процесса и судить о прогнозе заболевания.
Щелочная фосфатаза (ЩФ) в почках практически полностью находится в корковом слое и прочно фиксирована на матриксе мембран “щетинистой” каемки нефротелия. Активность ЩФ в моче возрастает при поражении проксимальных извитых канальцев почек.
Y-глутамилтрансфераза (Y-ГТ) обнаруживается преимущественно в клетках проксимальных извитых канальцев и в нисходящей части петли Генле. Увеличение активности Y-ГТ в моче выявлено на ранних стадиях повреждения почек. Для пациентов, резистентных к проводимой терапии, характерна медленная нормализация активности Y-ГТ в моче в процессе лечения.
Арилсульфатаза-А (АС-А) относится к лизосомальным гидролазам, ее основным источником являются дистальные канальцы. Сульфатазная активность мочи может быть использована для оценки глубины повреждения почечной ткани.
В-глюкуронидаза (В-ГЛ) также является лизосомальным ферментом, преимущественно отражает функцию дистальных канальцев.
Лактатдегидрогеназа (ЛДГ) находится в цитоплазме клеток. В корковом веществе почек преобладают изоферменты ЛДГ1 и ЛДГ2 , в мозговом слое и сосочках – ЛДГ4 и ЛДГ5. Повышение активности только цитоплазматических ферментов указывает на легкое и обратимое повреждение клеток.
Холинэстераза (ХЭ) - единственный фермент, отражающий поражение клубочкового аппарата.
Для правильной интерпретации показателей ферментурии у детей с различной патологией, особенно почечной, нами были обследованы 42 практически здоровых ребенка в возрасте от 7 суток до 1 года и разработаны нормативы. Активность ферментов в моче определяли кинетическими и колориметрическими методами при 37°С с использованием анализатора скорости реакции “Spectronic-710” (США). Для оценки ферментурии исследовали только свежесобранную мочу (утренняя порция - с 6 до 9 часов).
Активность энзимов выражали в международных единицах. За одну международную единицу активности фермента (Е) принимают количество энзима, которое при оптимальном рН и субстратной концентрации вызывает превращение 1 мкмоль субстрата за 1 минуту при 30°С. Наиболее оптимальным является соотнесение активности ферментов на 1 мг выделенного с мочой креатинина (мЕ/мг креатинина), что позволяет при использовании разовой порции мочи нивелировать колебания суточного диуреза. Результаты представлены в табл. 1.
Таблица 1.
Активность ферментов в моче (мЕ/мг креатинина) у практически здоровых новорожденных и грудных детей (М±м)
|
Возраст Ферменты |
7-10 суток |
1-2 месяца |
6-7 месяцев |
Старше 1 года* |
|
Y-ГТ |
57,472±1,173 |
46,182±2,769 |
34,462±2,591 |
до 40 |
|
ЩФ |
17,089±1,407 |
13,482±2,290 |
8,769±0,642 |
до 10 |
|
ЛДГО |
34,828±1,905 |
26,346±4,581 |
28,308±3,169 |
до 42 |
|
ЛДГ1,2 |
14,594±1,536 |
12,091±2,002 |
18,615±2,209 |
до 35 |
|
ХЭ |
7,55±0,611 |
6,818±0,749 |
6,462±0,595 |
до 10 |
|
В-ГЛ |
0,58±0,088 |
0,39±0,074 |
0,194±0,016 |
До 0,23 |
|
АС-А |
0,968±0,088 |
0,463±0,051 |
0,334±0,027 |
До 0,42 |
*собственные данные, совпадающие с данными литературы
Выявлена зависимость ферментурии от возраста. При комплексной оценке активности в моче ферментов, имеющих различную внутрипочечную локализацию, обнаружено, что эти показатели у новорожденных в 1,5-2 раза выше, чем у детей старше года. Вероятно, это объясняется морфофункциональной незрелостью почек, преимущественно тубулярного отдела, у новорожденных. Со второго полугодия жизни активность ферментов в моче соответствует таковой у детей старше года. Активность ХЭ у здоровых детей практически не претерпевала изменений в возрастном аспекте, что свидетельствует о более быстром созревании гломерулярного отдела нефрона по сравнению с тубулярным.
В последние годы возросло внимание исследователей к бета-2-микроглобулину (Б-2-МГ) и его значению в патологии детского возраста. Б-2-МГ - низкомолекулярный белок, представляет собой легкую цепь HLA - комплекса и является его постоянной субъединицей. Основной путь выведения и метаболизма Б-2-МГ осуществляется через почки. Он полностью фильтруется через базальную мембрану гломерул и на 99,9 % реабсорбируется клетками проксимальных канальцев посредством пиноцитоза. Повышение уровня Б-2-МГ в крови отражает либо увеличение его синтеза, либо снижение скорости гломерулярной фильтрации (СКФ). Для определения СКФ лучше использовать сывороточный уровень Б-2-МГ, чем креатинина, так как первый показатель стабилен в течение дня и не зависит от характера принимаемой пищи. Повышение уровня Б-2-МГ в моче наблюдается только при тубулярных дисфункциях - нарушении реабсорбции и катаболизма проксимальными канальцами почек. Оценка уровня Б-2-МГ в сыворотке крови и моче у новорожденных детей может быть использована в целях дифференциальной диагностики почек (особенно пиелонефрита и инфекции мочевыводящих путей), уточнения преимущественного места поражения нефрона, в качестве объективного критерия степени функциональных нарушений, частично - для характеристики иммунологического статуса. Данные о содержании Б-2-МГ в крови и моче у детей малочисленны и противоречивы. Это послужило основанием для изучения уровня Б-2-МГ у новорожденных и детей раннего возраста с почечной патологией.
Нами обследованы 152 здоровых ребенка в возрасте 1 суток жизни до 3 лет (контральная группа). Содержание Б-2-МГ в сыворотке крови и моче исследовали методом радиоиммунологического анализа in vitro с использованием Б-2-МГ, меченного 125I. Применяли наборы реактивов ИБОХ АН Республики Беларусь. Результаты представлены в табл. 2.
Таблица 2.
Уровень Б-2-МГ в сыворотке крови и моче у практически здоровых новорожденных и детей раннего возраста
|
Возраст |
Число детей (n) |
Б-2-МГ в крови (мг/л) М±м |
Б-2-МГ в моче (мг/л) М±м |
|
1-2 сут. |
18 |
7,055±0,123 |
1,494±0,827 |
|
3-5 сут. |
20 |
8,233±0,508 |
1,847±0,284 |
|
8-10 сут. |
18 |
7,612±0,505 |
1,354±0,242 |
|
11-15 сут. |
12 |
6,823±0,544 |
1,181±0,233 |
|
16-30 сут. |
13 |
5,762±0,275 |
0,504±0,093 |
|
2-3 мес. |
18 |
4,942±0,441 |
0,305±0,052 |
|
4-6 мес. |
16 |
4,047±0.338 |
0,144±0,014 |
|
7-12 мес. |
21 |
3,505±0,171 |
0,109±0,013 |
|
2-3 г. |
16 |
3,446±0,146 |
0,099±0,012 |
Половых различий в концентрации Б-2-МГ не выявлено, но установлена четкая зависимость от возраста детей. Более высокий уровень Б-2-МГ в сыворотке крови обнаружен у новорожденных и детей первого месяца жизни (6,0 - 8,0 мг/л), далее он заметно снижается и после 1 года приближается к показателям у детей старшего возраста (по данным литературы - от 0,8 до 3,0 мг/л). Наиболее высокий уровень Б-2-МГ в моче наблюдается у новорожденных, особенно в первые 7-10 дней жизни. У грудных детей он постепенно снижается, на 2-м и 3-м годах жизни достигаем минимальной отметки (0,1 мг/л), хотя остается в 2-3 раза выше, чем у детей старшего возраста и у взрослых (по данным литературы - до 0,05 мг/л), что объясняется незрелостью канальцевого аппарата почек.
В связи с ухудшением экологических условий, а также улучшением реанимационных мероприятий в неонатальном периоде, приводящим к выхаживанием детей с очень низкой и экстремально низкой массой тела, отмечается нарастание дисметаболических нефропатий, нередко приводящих к развитию мочекаменной болезни даже у детей раннего возраста. Своевременная диагностика обменных нарушений у детей, предупреждение разития камнеобразования, а также профилактика осложнений является одной из важнейших задач детской нефрологии. С этой целью рекомендуется использование не только биохимического анализа мочи и определение антикристаллообразующей способности мочи, но и исследование мочи с помощью Литос-системы.
Литос-система разработана на основе метода клиновидной дегидратации, предложенного С.Н. Шатохиной и В.Н. Шабалиным. Литос-система позволяет: 1) выявлять процесс камнеобразования в органах мочевой системы; 2) определять степень активности и устойчивости процесс камнеобразования; 3) устанавливать состав камнеобразующих солей мочи. Литос-система разрешена Минздравом РФ для применения в клинической практике (Приказ №17 МЗ РФ от 21 января 1997 г.). Специальное обучение и обследование проводится на базе лаборатории кристаллографических методов исследования при Российском НИИ геронтологии Минздрава России. Диагностика основана на принципах теории самоорганизации сложных систем и состоит в выявлении структурных особенностей капли мочи при переходе ее из жидкого состояния в твердое с помощью метода клиновидной дегидратации биологической жидкости. В норме, при добавлении белка к моче, образуется краевая белковая зона, хорошо наблюдаемая визуально в виде прозрачного периферического кольца дегидратированной капли. Отсутствие краевой аморфной зоны указывает на наличие процесса камнеобразования в органах мочевой системы обследуемого (рис. 1).
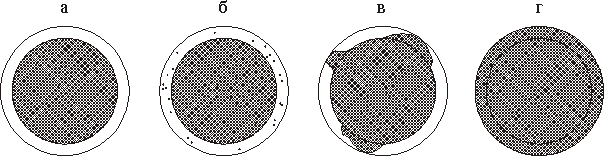
Рис. 1. Вид дегидратированных капель мочи в смеси с белковым Литос-реагентом при отсутствии (а) и различной степени активности камнеобразования в органах мочевой системы: б - слабой; в - умеренной; г - высокой (схема).
Таким образом, необходимо активное выявление нефропатий у новорожденных детей с применением современных неинвазивных информативных диагностических тестов для осуществления ранней диагностики и своевременного проведения реабилитационных мероприятий.
Структура нефропатий у новорожденных детей
Наиболее часто в неонатальном периоде встречаются инфекционно-воспалительные заболевания ОМС, несколько реже – гипоксические нефропатии, острая почечная недостаточность (ОПН), токсико-аллергические состояния и интерстициальный нефрит, а также у них возможно развитие врожденных и наследственных заболеваний почек (гидронефроз, пузырно-мочеточниковый рефлюкс, поликистоз почек, мультикистоз, микрокистоз почек и др.), инфарктов почек, дисметаболических нефропатий и мочекаменной болезни (МКБ).
При анализе историй болезни и осмотре более 2 тысяч новорожденных детей, перенесших реанимационные мероприятия, находившихся в неонатальном центре и отделении патологии новорожденных ДГКБ №13 им. Н.Ф. Филатова, нефропатии были выявлены у 1/3 детей (34,2%). Установлена структура и частота встречаемости различных нозологических форм заболеваний ОМС у детей неонатального периода. Результаты представлены в табл. 3.
Таблица 3.
Структура и частота встречаемости заболеваний органов мочевой системы у новорожденных детей
|
п/п |
Клинический диагноз |
Частота в % |
|
1. |
Инфекция мочевой системы (/ИМС) |
37,3 |
|
2. |
Гипоксическая нефропатия (ГНП) |
32 |
|
3. |
Острая почечная недостаточность (ОПН) |
16 |
|
4. |
Интерстициальный нефрит (ИН) |
6 |
|
5. |
Дисметаболические нефропатии (ДН) |
4 |
|
6. |
Инфаркты почек (ИП) |
3,5 |
|
7. |
Прочие |
1,2 |
