
- •Расчётные задачи химической термодинамики
- •Глава 1.
- •Если использовать средние значения теплоемкости и плотностив заданном температурном интервале, то объемная плотность аккумулированной энергии равна:
- •Задача 1.3.4
- •Задача 1.3.6
- •Задача 1.38
- •1.4 Задачи
- •Глава 2. Тепловые эффекты физико-химических процессов.
- •2.1. Цели изучения
- •2.2. Основные закономерности.
- •Для реакций с участием идеальных газов
- •2.3. Основные задачи
- •Отметим, что рассматриваемая реакция протекает наряду с реакциями
- •Задача 2.3.4.
- •Глава 3.
- •В некоторых случаях можно воспользоваться значениями средних
- •3.3. Основные задачи.
- •Задача 3.3.2
- •Задача 3.3 Определите возможность протекания процесса
- •Решение
- •Задача. 3.3.4
- •Задача 3.3.5
- •Решение
- •Решение
- •Решение уравнения с помощью эвм - секунды, но почти с той же
- •Задача 3.3.8
- •Согласно [1], логарифм константы равновесия реакции образования
- •Исходя из этих соображений, проследим влияние давления на вели-
- •Выразим связь между константой равновесия и равновесным соста-
- •Задача 3.3.13
- •3.4. Многовариантные задачи.
Задача 3.3 Определите возможность протекания процесса
Al2O3 (тв) + 3SO3(газ) → Al2(SO4)3(тв)
В закрытой системе при стандартных условиях и температуре 298 К.
Решение
Критерием возможности протекания процесса в закрытой системе при постоянном давлении является (3.29) условие
![]()
По условию задачи обсуждается возможность проведения этого процесса при стандартных условиях, т.е парциальное давление SO3 P(SO3)=1.
Тогда должно выполнятся условие
![]()
Значение
![]() может быть рассчитано согласно закону
Гесса по данным об энергиях Гиббса
образования
может быть рассчитано согласно закону
Гесса по данным об энергиях Гиббса
образования![]() компонентов
реакции [1]:
компонентов
реакции [1]:
Al2O3 (тв) + 3SO3(газ) → Al2(SO4)3(тв)

Следовательно, условие (3.29) соблюдается и в исследуемых условиях возможно протекание рассматриваемого процесса.
Задача. 3.3.4
В закрытой системе при стандартных условиях и 298 К для реакции
Al2O3 (тв) + 3SO3(газ) → Al2(SO4)3(тв)
![]() .
Возможен ли этот процесс при той же
температуре в изолированной системе?
.
Возможен ли этот процесс при той же
температуре в изолированной системе?
Решение.
Критерием возможности самопроизвольного протекания процесса в изолированной системе является условие (3.2)
![]() ,
,
то есть в изолированной системе самопроизвольно протекают процессы, идущие с ростом энтропии.
В исследуемом процессе (задача 3.3.1)
![]()
Следовательно, в изолированной системе процесс не возможен.
Задача 3.3.5
Определите температурный интервал, в котором в закрытой системе при стандартных условиях возможно самопроизвольное протекание процесса
Al2O3 (тв) + 3SO3(газ) → Al2(SO4)3(тв)
Решение
Критерием возможности самопроизвольного протекания процесса в закрытой системе при P,T = const является условие (3.29)
![]() или
(3.17)
или
(3.17)
![]()
где
![]() и
и![]() рассчитываются
согласно (2.10)
рассчитываются
согласно (2.10)
![]()
и (3.9)
![]()
а
![]() согласно
(2.9)
согласно
(2.9)
![]()
Значения
![]() и
коэффициенты∆a,
∆b
и ∆с’
в (2.9) рассчитываются согласно закону
Гесса.(Расчет для исследуемой реакции
приведен в задаче 3.3.2)
и
коэффициенты∆a,
∆b
и ∆с’
в (2.9) рассчитываются согласно закону
Гесса.(Расчет для исследуемой реакции
приведен в задаче 3.3.2)
Тогда после подстановки
![]()
и
![]()
в (3.17) получим, согласно (3.29), что самопроизвольный процесс возможен при температурах когда,
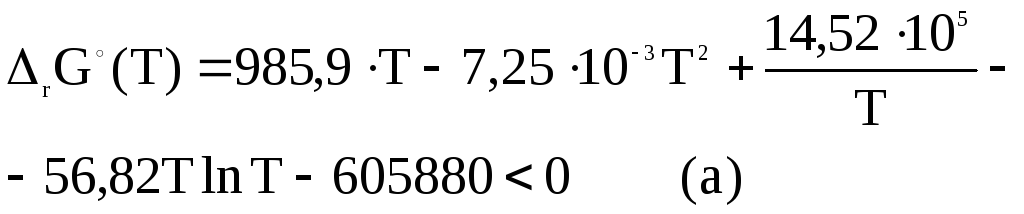
Таким образом задача свелась к решению неравенства.
Напомним,
что полученная зависимость адекватно
описывает изменения
![]() с
температурой в области температур 298 –
1100 К, поскольку в этой области (см. задачу
3.3.2) адекватны зависимости Ср(Т) для всех
компонентов реакции).
с
температурой в области температур 298 –
1100 К, поскольку в этой области (см. задачу
3.3.2) адекватны зависимости Ср(Т) для всех
компонентов реакции).
Если
пренебречь изменением
![]() и
и![]() с увеличением температуры, как отмечается
в некоторых пособиях [5], то вместо
неравенства (а) можно использовать
с увеличением температуры, как отмечается
в некоторых пособиях [5], то вместо
неравенства (а) можно использовать
![]()
и![]() ли
для исследуемой реакции
ли
для исследуемой реакции
Разумеется неравенство (б) решается мгновенно:
![]() если
298
T<994,
если
298
T<994,
но используя неравенство (б) мы не знаем, какую ошибку, или какую погрешность допускаем при определении температурного интервала.
Разумеется, решение неравенства (а) сопряжено с некоторыми вычислительными трудностями, которые удается избежать, если у Вас под рукой ПЭВМ. А если нет?
Отступление второе, в котором напоминается об одном достаточно простом методе решения нелинейных уравнений.
Гарантированную сходимость и простую программную реализацию решения уравнений F(x)=0 дает метод деления отрезка пополам [7].
Вернёмся
к рассматриваемой задаче и проведём
описанную процедуру для решения уравнения
(а), помня ,что если имеется корень
уравнения, т.е. некоторое значение
![]() для которой
для которой![]() ,то
он должен находиться в температурном
интервале 298–1100 К (весьма возможна
ситуация, тогда при любом значении
температуры
,то
он должен находиться в температурном
интервале 298–1100 К (весьма возможна
ситуация, тогда при любом значении
температуры![]() )
и рассчитаем
)
и рассчитаем![]() на концах температурного интервала:
на концах температурного интервала:
![]()
![]()
Вывод:
значит
![]() на концах температурного интервала
имеет разные знаки , следовательно, и
при некоторой
на концах температурного интервала
имеет разные знаки , следовательно, и
при некоторой
![]()
![]() ;
;
Можем уменьшить рассматриваемый интервал, учтя приближенное значение
![]()
![]()
![]()
![]()
![]()
![]()
и,
если задана точность определения
температурного интервала
![]() ,
то можно остановить расчёт: значение
,
то можно остановить расчёт: значение![]() находится
между
находится
между![]() и
и![]() ,
что отличается от приближенного значения
944К на 100К .
,
что отличается от приближенного значения
944К на 100К .
Задача 3.3.6.
Исследуйте возможность самопроизвольного процесса
![]()
при T=1050K
