
- •Сборы. Лекарственные и весовые соотношения ингредиентов в них
- •Условные термины обозначения растворимости
- •Структурно-логическая схема технологии и контроля качества концентрированных растворов
- •Количество стабилизатора на 1,0 г гидрофобного вещества
- •Способы приготовления первичных масляных эмульсий
- •Структурно-логическая схема технологии и контроля качества водных вытяжек из растительного лекарственного сырья
- •Классификация мазевых основ
- •Количество лекарственных веществ и основы, необходимое для приготовления 30 суппозиториев методом выливания в формы емкостью 2 см3
- •Вспомогательные вещества, используемые для приготовления пилюльной массы
- •Перечень лекарственных веществ, к которым предъявляются дополнительные требования
- •Влияние относительной влажности воздуха на отсыревание порошков
- •Влияние некоторых факторов на расплавление и отсыревание смесей лекарственных веществ
- •Вощеных капсулах
- •Совместимость солей алкалоидов и азотистых оснований с бензоатами, салицилатами, бромидами и йодидами (а. А. Фелсберг, в. А. Шидловска)
- •Несовместимости витаминов
- •Несовместимость витаминов с некоторыми лекарственными веществами
Перечень лекарственных веществ, к которым предъявляются дополнительные требования
Препарат |
Требования |
Глюкоза Гексаметилентетрамин Желатин медицинский Кофеин-бензоат натрия Магния сульфат Мезатон Метиленовый синий Мочевина Натрия бензоат Натрия гидрокарбонат Натрия цитрат Тиамина бромид Тиамина хлорид Фетанол Эуфиллин |
Должна быть свободна от пирогенных веществ Отсутствие аминов, солей аммония, параформа 10 %-ный раствор должен быть апирогенен и не превышать эталон мутности ¹ 3
Отсутствие органических примесей проверяется по реакции с концентрированной кислотой серной; 20 %-ный раствор дол-жен быть прозрачен и бесцветен при нагревании на водяной бане в течение 30 минут
Отсутствие примесей марганца Для инъекций используется препарат не позже 2 месяцев после его приготовления 1 % раствор должен иметь рН не ниже 3,9
Для инъекций требуется препарат специальной очистки, стерильный и лиофилизированный («мочевина для инъекций»). К каждой упаковке мочевины прилагается флакон с раствором глюкозы 10 %-ной. Раствор мочевины для внутривенных вли-ваний в концентрации 30 % готовится непосредственно перед введением на 10 %-ном растворе глюкозы. При хранении раствор мочевины разлагается и может вызвать гемолиз
Примесей солей железа должно быть не более 0,0075 % 5 %-ный раствор должен быть прозрачен и бесцветен до и после стерилизации
Раствор для инъекций 10 %-ный имеет рН 7,8—8,3 (у раствора натрия гидроцитрата 5 % рН 4,7—5,0) 6 %-ный раствор должен быть прозрачен и бесцветен
Содержание препарата должно быть не менее 99 %
Для инъекций должен использоваться не позже 6 месяцев после приготовления (срок годности — 3 года) 10 %-ный раствор должен быть прозрачным; содержание этилендиамина должно быть 18—22, теофиллина 75—82 % |
-
Стерилизационное оборудование для воздушной стерилизации
Тип
Техническая характеристика
Шкаф сушильный электрический круглый АВ-151
Диапазон регулируемой температуры от 40 до 200 °С. Размеры рабочей камеры: диаметр 358, глубина 270 мм.
Шкаф сушильно-стерили-зационный ШСС-80П
Диапазон регулируемых температур от 50 до 200 °С. Размеры рабочей камеры 400×430×500 мм
Шкаф сушильно-стерили-зационный ШСС-250П
Диапазон автоматически поддерживаемой температуры в рабочей камере от 50 до 200°С. Объем рабочей камеры 250 дм3.
Шкаф сушильно-стерили-зационный проходной ШСС-250ПР
Диапазон автоматически регулируемых температур от 50 до 200 °С. Размеры рабочей камеры 800×630×500 мм.
Шкаф сушильно-стерили-зационный ШСС-500П
Диапазон автоматически поддерживаемых температур от 50 до 200°С. Размеры рабочей камеры 1000х8000х630 мм.
Шкаф сушильно-стерили-зационный проходной ШСС-500ПР
Диапазон автоматически поддерживаемых температур от 50 до 200°С. Размеры рабочей камеры 1000х8000х630 мм.
Шкаф сушильно-стерили-зационный ШСС-1000П
Диапазон автоматически регулируемых температур от 50 до 200 °С. Размеры рабочей камеры 1500×830×800 мм.
Шкаф сушильно-стерили-зационный проходной ШСС-1000ПР
Диапазон температур от 50 до 200 °С. камеры 1500×830×800 мм.
СТРУКТУРНО-ЛОГИЧЕСКАЯ СХЕМА ТЕХНОЛОГИИ И КОНТРОЛЯ КАЧЕСТВА РАСТВОРОВ ДЛЯ ИНЪЕКЦИЙ
Подготовка этикеток
и сигнатур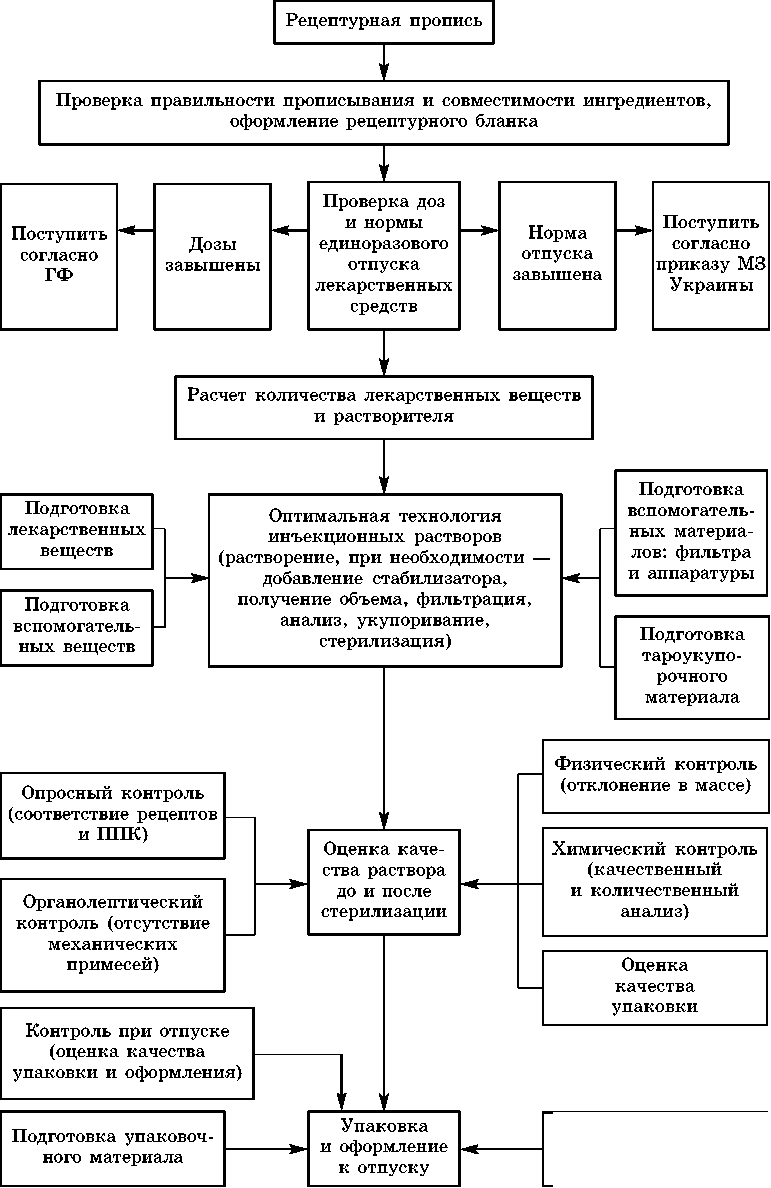
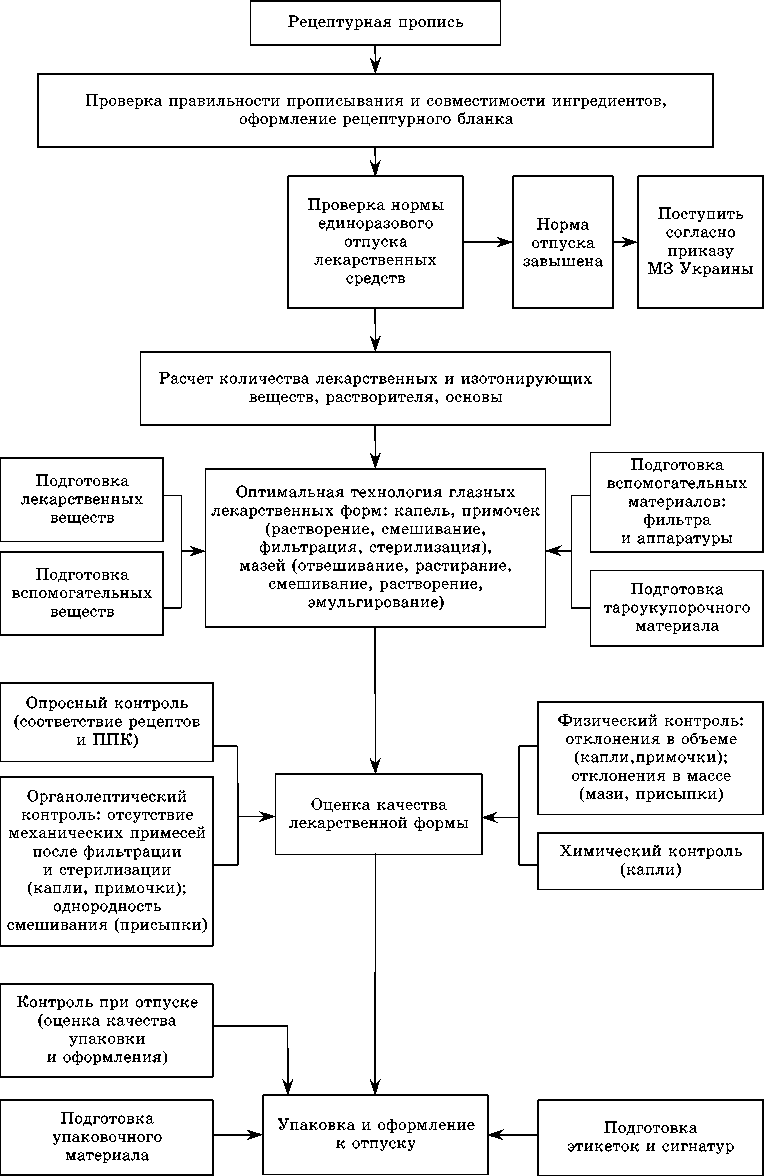
СТРУКТУРНО-ЛОГИЧЕСКАЯ СХЕМА ТЕХНОЛОГИИ И КОНТРОЛЯ КАЧЕСТВА ГЛАЗНЫХ ЛЕКАРСТВЕННЫХ ФОРМ
Зависимость между массой и единицами действия некоторых антибиотиков
Лекарственное вещество |
Единицы действия (ЕД), млн |
Масса, г |
Ампициллин |
1 |
0,580 |
Бензилпенициллина натриевая соль |
1 |
0,600 |
Бензилпенициллина новокаиновая соль |
1 |
0,900 |
Бициллин |
1 |
0,760 |
Гликоциллин |
1 |
1,000 |
Дигидрострептомицина пантотенат |
1 |
2,120 |
Дигидрострептомицина сульфат |
1 |
1,820 |
Канамицин |
1 |
1,230 |
Леворин |
1 |
0,100 |
Линкомицина гидрохлорид |
1 |
1,000 |
Метициллин |
1 |
0,676 |
Мономицин |
1 |
1,000 |
Морфоциклин |
1 |
1,000 |
Неомицина сульфат |
1 |
1,564 |
Новобиоцин |
1 |
1,000 |
Окситетрациклина гидрохлорид |
1 |
1,000 |
Олеандомицина основа |
1 |
1,000 |
Олеандомицина фосфат |
1 |
1,100 |
Олететрин |
1 |
1,000 |
Полимиксин |
1 |
0,125 |
Стрептомицина основа |
1 |
1,000 |
Стрептомицина сульфат |
1 |
1,250 |
Феноксиметилпенициллин |
1 |
0,650 |
Фторимицин |
1 |
1,300 |
Хлортетрациклин |
1 |
1,000 |
Циклосерин Д |
– |
1,000 |
Эритромицин |
1 |
1,110 |
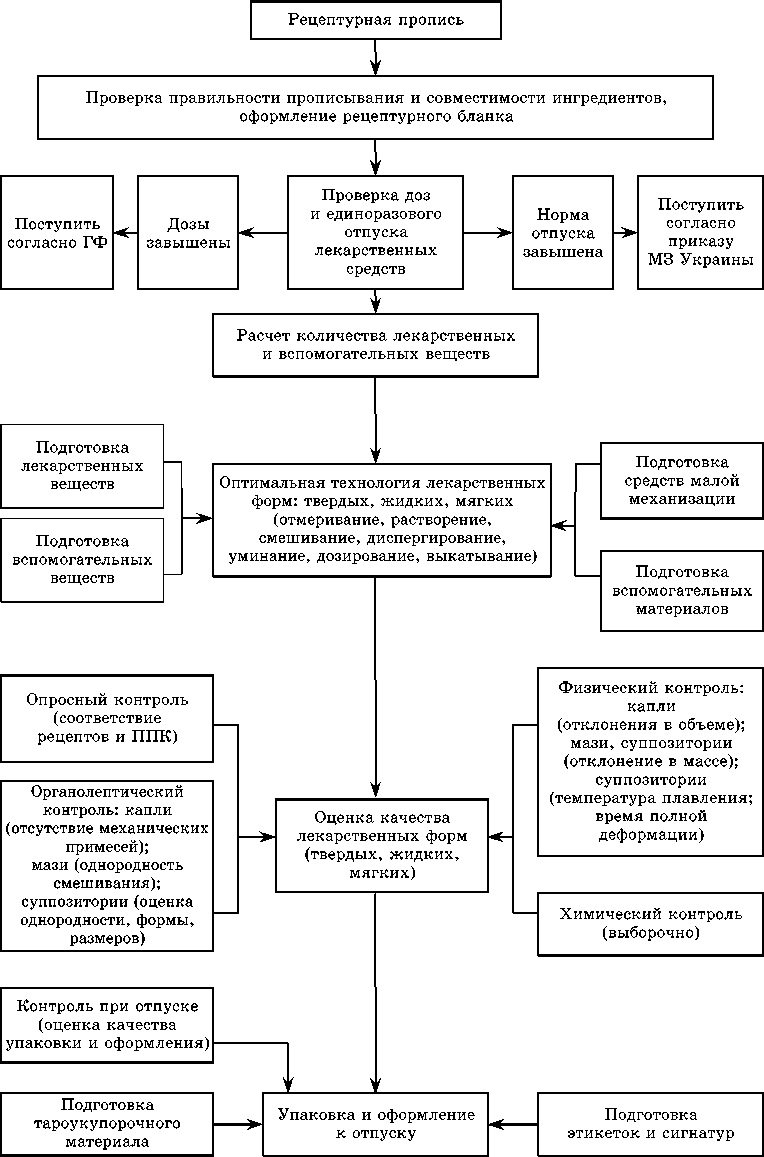
СТРУКТУРНО-ЛОГИЧЕСКАЯ СХЕМА ТЕХНОЛОГИИ И КОНТРОЛЯ КАЧЕСТВА ЛЕКАРСТВЕННЫХ ФОРМ С АНТИБИОТИКАМИ
Сроки годности и условия стерилизации растворов
внутреннего употребления для новорожденных детей
(во флаконах и бутылках, герметично укупоренных
резиновыми пробками под обкатку)
№ п/ п 1 |
Наименование раствора и концентрация |
Срок годности в сутках при температуре не выш е 25 °С |
Х ранение |
Условия стерилизации |
Примечание |
|
|
|
|
|
температура, °С |
время, мин |
|
|
2 |
3 |
4 |
5 |
6 |
7 |
1 |
Вода очищенная |
30 |
|
120 |
8 |
|
2 |
Растворы глюкозы 5, 10, 25 % -ные |
30 |
|
120 |
8 |
Готовя т без стабилизатора |
3 |
Раствор глюкозы 5 % -ны й 100 мл кислоты аскорбиновой 1,0 г |
5 |
В за-щ ищ ен-ном от света месте |
100 |
30 |
Готовят на свежепро-кипяченной воде очи-щенной. При фасовке флаконы заполняются доверху |
4 |
Раствор глюкозы 10 или 20 % -ны й 100 мл кислоты глютаминовой 1,0 г |
30 |
В за-щ ищ ен-ном от света месте |
120 |
8 |
|
5 |
Раствор дибазола 0,01 % -ны й |
30 |
|
120 |
8 |
|
6 |
Раствор димедрола 0,02 % -ны й |
30 |
В за-щ ищ ен-ном от света месте |
120 |
8 |
Раствор следует использовать только в концентрации 0,02% и фа-совке по 10 м л. В усло-ви я х родильного дом а следует воздержаться от применения растворов димедрола , учитывая его выраженное седативное действие, угнетающее влияние на Ц НС и возможность интоксикации |
7 |
Раствор калия ацетата 0 ,5 % -ный |
30 |
|
120 |
8 |
|
8 |
Раствор калия йодида 0,5 % -ный |
30 |
В за-щ ищен-ном от света месте |
120 |
8 |
Фасовка раствора не должна превышать 20 мл |
9 |
Раствор кальция лактата 3 или 5 % -ный |
30 |
|
120 |
8 |
Готовят с учетом фактического содержания влаги в препарате |
10 |
Раствор кальция глюконата 1— 3 или 5 % -ный |
7 |
|
120 |
8 |
Растворяют в горя чей воде |
11 |
Раствор кальция хлорида 3 % -ны й |
30 |
|
120 |
8 |
Д л я приготовления растворов целесообразно использовать 10—5% концентрат |
12 |
Раствор кислоты аскорбиновой 1 % -ный |
5 |
В за-щ ищ ен-ном от света месте |
100 |
30 |
Готовят на свежей прокипя ченной воде очищенной. При фасовке флаконов заполняют доверху |
573
Окончание табл. 39
12 3 |
4 |
5 |
6 |
7 |
||
13 |
Раствор кислоты никотиновой 0,05 % -ный |
30 |
В защищенном от света месте |
120 |
8 |
|
14 |
Раствор кислоты хлористоводородной 1 % -ный |
30 |
|
120 |
8 |
При приготовлении используют разбавленную кислоту хлористо-водород-ную (8,2—8,4 % ) ГФ Х, ст. 18, принимая ее за 100 % |
15 |
Раствор натрия хлорида 0,9 % -ный |
30 |
|
120 |
8 |
|
16 |
Раствор натрия бромида 1 % -ный |
30 |
В защищенном от света месте |
120 |
8 |
|
17 |
Раствор пиридок-сина гидрохлорида 0,2 % -ный |
30 |
|
120 |
8 |
|
18 |
Раствор эуфиллина 0,05 или 0,5 % -ный |
15 |
|
120 |
8 |
|
