
- •Прикладна електрохімія Методичні вказівки до виконання лабораторних робіт
- •Лабораторна робота 1. Хімічне нікелювання поверхні діелектриків
- •Лабораторна робота 2. Вилучення іонів нікелю з відпрацьованого розчину хімічного нікелювання
- •Лабораторна робота 3. Електрохімічне осадження міді
- •Лабораторна робота 4. Електрохімічне вилучення міді
- •Методика виконання роботи
- •Лабораторна робота 5. Електрохімічне осадження нікелю.
- •Лабораторна робота 6. Електрохімічне анодування алюмінію
- •Лабораторна робота 7. Електрохімічне цинкування.
- •Лабораторна робота 8. Дослідження деяких параметрів вторинних хімічних джерел струму
Лабораторна робота 6. Електрохімічне анодування алюмінію
Мета роботи – ознайомитись з електрохімічним анодування алюмінію.
Завдання роботи – провести процес анодування, визначити кількість електрики, що пройшла через зразок, зміни ваги зразка, дослідити деякі фізико-хімічні властивості оксидної плівки та її здатність до забарвлення.
Короткий огляд теоретичних основ процесу
Анодна обробка металів (анодування) застосовується для нарощування на їх поверхні товстої оксидної плівки, яка краще захищає метал від корозії, поліпшує його зовнішній вигляд, або механічні якості.
Своєрідним древнім способом оксидування без застосування електрохімічних методів був процес «вороніння» сталі. Гарячі деталі занурювали у рослинне (льняне) масло. Операції повторювали декілька раз і поверхні металу нарощувався достатньо товстий оксидний шар чорного кольору (що і дало таку назву), який краще захищав сталь від корозії.
Серед електрохімічних методів анодування найбільш розповсюдженим є анодування алюмінію та сплавів. Його мета – нарощування на поверхні металу захисної оксидно-гідроксидної плівки. Плівка пориста, що дозволяє стійку пропитку пігментами з метою забарвлення металевого виробу.
Для анодування деталь занурюють у слабку (для отримання тонкої щільної і мало пористої плівки, яка непридатна для забарвлення), або сильну (для отримання товстої пористої плівки, що придатна для фарбування) кислоту.
Н а
алюмінієвому аноді йдуть електрохімічні
процеси розчинення алюмінію
а
алюмінієвому аноді йдуть електрохімічні
процеси розчинення алюмінію
![]() та утворення кисню внаслідок розкладання
води
та утворення кисню внаслідок розкладання
води
![]() .
Утворені йони кисню рухаються у напрямку
поверхні аноду, де розряджаються і
утворюють газ кисень
.
Утворені йони кисню рухаються у напрямку
поверхні аноду, де розряджаються і
утворюють газ кисень
![]() .
Однак, на цьому шляху вони можуть
зустрітися з щойно утвореними йонами
алюмінію та утворити молекулу алюміній
оксиду
.
Однак, на цьому шляху вони можуть
зустрітися з щойно утвореними йонами
алюмінію та утворити молекулу алюміній
оксиду
![]() .
Таким чином на поверхні електроду
розростається оксидний шар. З іншого
боку, зовнішній край оксидного шару
хімічно розчиняється у кислоті
.
Таким чином на поверхні електроду
розростається оксидний шар. З іншого
боку, зовнішній край оксидного шару
хімічно розчиняється у кислоті
![]() .
.
Рисунок 1. Схема розростання оксидної анодної плівки.
Отже, в результаті оксидна плівка ніби то проростає всередину металу, а її товщина визначається балансом процесів утворення оксиду на границі плівки з металом та його розчинення на границі плівки з розчином. Більша частина плівки внаслідок нерівномірного утворення/розчинення стає пронизаною глибокими порами. Схематично анодна плівка виглядає як на Рисунку 1.
Складається вона з відносно тонкого глибинного щільного шару без пор та ширшого пористого шару.
Після закінчення анодування
пори можна «закрити» пропарювання
анодованої деталі. При цьому у порах
утворюється гідроксид-оксид алюмінію
![]() ,
який “забиває» пору. З іншого боку,
свіжу анодовану деталь можна обробити
біхроматом. При цьому поверхня набуває
жовтого кольору, а пори закриваються
за рахунок утворення хромату-оксиду
алюмінію
,
який “забиває» пору. З іншого боку,
свіжу анодовану деталь можна обробити
біхроматом. При цьому поверхня набуває
жовтого кольору, а пори закриваються
за рахунок утворення хромату-оксиду
алюмінію
![]() .
Нарешті, анодовану деталь можна занурити
у розчин органічного, або неорганічного
барвника, молекули якого теж заходять
у пори і забарвлюють поверхню.
.
Нарешті, анодовану деталь можна занурити
у розчин органічного, або неорганічного
барвника, молекули якого теж заходять
у пори і забарвлюють поверхню.
Утворені оксидні плівки на алюмінії ефективно захищають його від корозії, вони добре зчеплені з металом та досить стійкі до механічних впливів. разом з тим, гнучкість їх мала (а алюміній – досить пластичний метал), тому при згинанні анодованого виробу у оксидній плівці утворюються тріщини, які погіршують ізолюючий ефект плівки.
МЕТОДИКА ВИКОНАННЯ РОБОТИ
Для проведення анодування підготувати електроліт, що містить 200 г/л сульфатної кислоти і 5 зразків алюмінію.
Знежирити всі зразки шляхом занурення на 5-10 хв у розчин, що містить 30 г/л Na3PO4 . 12H2O; 30 г/л Na2CO3 і 30 г/л Na2SiO3 при температурі 60-70 0С. Після цього промити зразки проточною водою.
Протравити зразки шляхом занурення на 2 хв у нагрітий до 60-80 0С розчин NaOH 50-150 г/л. Після цього промити зразки проточною водою.
Освітлити зразки шляхом занурення на 30 сек у розчин з концентрацією HNO3 350-400 г/л при кімнатній температурі. Після цього промити зразки проточною водою, висушити і зважити, записавши результат у таблицю.
З
 ібрати
електричну схему для оксидування
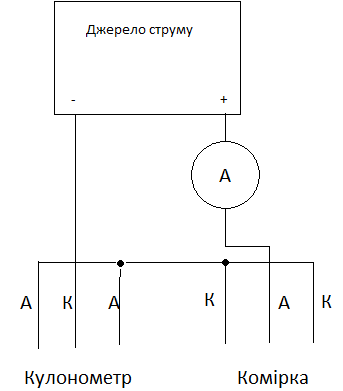
алюмінію (Рис. 2).
ібрати
електричну схему для оксидування
алюмінію (Рис. 2).
Рисунок. 2. Схема електричних з’єднань для анодування алюмінію.
Вивчити зміну ваги електроду залежно від кількості електрики, що пройшла через електрод. Для цього провести оксидування 5 зразків при густині струму 1,5 А/дм2 пропустивши через зразки кількість електрики 5, 10, 20, 30, 40 А-хв/дм2.
Після закінчення електролізу кожен алюмінієвий електрод промити, висушити і зважити, , записавши результат у Таблицю 1.
Розрахувати зміну ваги кожного електроду і побудувати графік залежності питомої зміни ваги (г/см2) від кількості електрики, що пройшла через електрод.
Дослідити можливість фарбування анодованого алюмінію. Для цього слід обрати один, або декілька зразків, отриманих у попередньому досліді та занурити його (їх) у розчин K4[Fe(CN)6] з концентрацією солі 10 г/л на 10-15 хв при кімнатній температурі. Потім сполоснути холодною водою протягом 30 сек. і занурити у розчин FeCl3 з концентрацією солі 100 г/л при кімнатній температурі на 5-10 хв. Далі зразок (зразки) знов промити холодною водою. Анодована поверхня повинна стійко забарвитись у інтенсивно синій колір.
Всі зразки разом із заповненим протоколом виконання роботи представити під час її здачі викладачу.
Таблиця 1
Результати виконання анодування алюмінію
№ зразка |
Площа, см2 |
Вага до обробки, г |
Вага після обробки, г |
Питома зміна ваги, г/см2 |
Результат забарвлення |
1 |
|
|
|
|
|
2 |
|
|
|
|
|
3 |
|
|
|
|
|
4 |
|
|
|
|
|
5 |
|
|
|
|
|
ОРІЄНТОВНИЙ ПЕРЕЛІК ПИТАНЬ ДЛЯ ЗДАЧІ РОБОТИ
Хімічні процеси, що супроводжують електрохімічне анодування.
Сфера застосування, мета, переваги й недоліки електрохімічно анодованих виробів.
Роль кожного реагенту у технології анодування алюмінію.
Описати основні етапи технологічного процесу анодування алюмінію.
Негативний вплив технологій електрохімічного анодування на довкілля і можливості його зменшення.
