Стоки и источники точечных дефектов
Из вышесказанного ясно, что концентрация точечных дефектов не является величиной постоянной, а меняется самопроизвольно в зависимости от внешних параметров (температуры).
Основным источником вакансий являются свободные поверхности кристалла, пустоты и трещины внутри него, а также границы зерен в поликристаллических образцах (так как границы зерен представляют собой чрезвычайно дефектную структуру с нарушенной кристаллической решеткой).
Вакансии могут образовывать в процессе пластической деформации при взаимодействии дислокаций: аннигиляции краевых дислокаций разного знака или движении дислокаций с порогами.
Также точечные дефекты могут образовываться при ядерном облучении металлов: атомы выбиваются из узлов структуры, в результате чего образуется френкелевская пара – межузельный атом и вакансия.
Стоками точечных дефектов являются те же места, что служили их источником – свободная поверхность, пустоты, трещины, границы зерен, дислокации. Возможна аннигиляция вакансии и межузельного атома, но это маловероятно из-за малой концентрации межузельных атомов.
Миграция вакансий
Атомы, совершающие колебательное движение, непрерывно обмениваются энергией. Из-за хаотичности теплового движения энергия неравномерно распределена между атомами, в какой-то момент атом может получить от соседей такой избыток энергии, что может занять соседнее положение, если оно совбодно, что равносильно перемещение -миграции вакансий.
Для перехода из положения с минимальной энергией (узла кристаллической структуры) в другое положение с минимальной энергией (вакантного узла кристаллической структуры) атом должен пройти через состояние с повышенной энергией – преодолеть энергетический барьер. На модели твердых сфер: атом должен протиснуться между соседними шарами, раздвинув их.
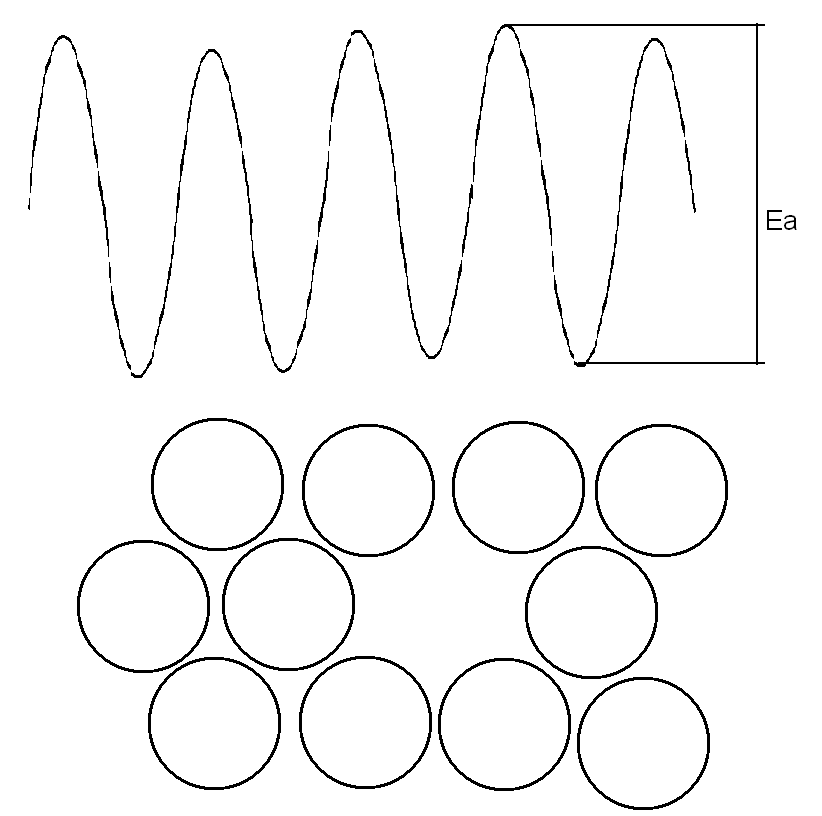
В реальности атомы должны преодолевать потенциальный барьер; происхождение которого связано, главным образом, с квантовыми силами отталкивания, сильно увеличивающимися при сближении атомов.Для того чтобы осуществить такой переход атом должен обладать некоторым избытком энергии, который он может получить от соседей в процессе теплового движения, и который он потеряет протискиваясь в соседнее положение и раздвигая соседей. Энергия, необходимая для такого перескока, называется энергией активации. Она обычно значительно больше средней энергии теплового движения (kT). Вероятность такого события очень мала и задается формулой Больцмана:
P = C =
Частота перескоков атома из своего положения в вакантное – подвижность вакансий -пропорционально вероятности, что атом обладает необходимой энергией Еа и частоте колебаний (можно сказать частоте попыток перескока).
Энергия активации миграции примерно в полтора-два раза ниже энергии образования вакансии. В случае, когда вакансионный механизм диффузии является основным, коэффициент самодиффузии пропорционален концентрации и подвижности вакансий, а энергия активации самодиффузии равна Еv + Em.
Поведение вакансий при закалке и отжиге
С понижением температуры (при равновесном охлаждении) снижается равновесная концентрация вакансий, вакансии мигрируют и исчезают в разного рода стоках. При быстром охлаждении – закалке – эти процессы не успевают произойти, и фиксируется избыточная концентрация вакансий (равновесная для более высокой температуры). В период закалки существует тенденция образования комплексов вакансий – ди-, тривакансий и более. Часть вакансий при миграции захватывается атомами примесей. Но если металл, пересыщенный вакансиями, нагреть, то благодаря увеличению подвижности атомов и, следственно, вакансий, весь их неравновесный избыток должен исчезнуть в стоках. Возможна также аннигиляция вакансий при встрече их с межузельными атомами. Если принять, что число стоков постоянно, а сами стоки имеют неограниченную емкость, то зависимость концентрации вакансий от времени отжига, (т.е. скорость изменения концентрации вакансий) подчиняется уравнению химической реакции первого порядка:
![]() , где С – концентрация реагента,
К – константа скорости реакции.
, где С – концентрация реагента,
К – константа скорости реакции.
закон действующих масс - скорость химической реакции в каждый момент времени пропорциональна концентрациям реагентов, возведённым в некоторые степени равные порядку реакции.
В нашем случае:
-dn/dt=Kn
Где n – число вакансий, К – константа скорости «реакции», зависит от коэффициента самодиффузии и геометрии стока.
Преобразование приведенного уравнения дает:
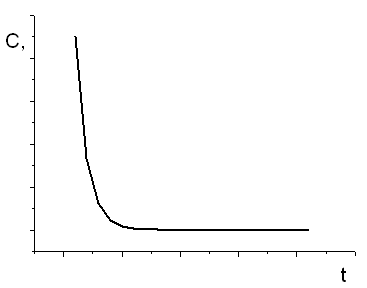
С= С0 exp(-Kt)
следовательно, концентрация вакансий экспоненциально уменьшается при увеличении времени отжига.