
- •1. Промышленное производство полиэтилена
- •2. Полиэтилен высокого давления (низкой плотности)
- •2.1. Особенности полимеризации этилена в газовой фазе
- •2.2. Производство полиэтилена высокого давления в трубчатом реакторе
- •2.3. Свойства и применение полиэтилена высокого давления
- •3. Полиэтилен низкого давления (высокой плотности)
- •3.1 Особенности полимеризации этилена на комплексных металлорганических катализаторах
- •3.2. Производство полиэтилена низкого давления (высокой плотности) в жидкой фазе
- •3.3. Производство полиэтилена низкого давления (высокой плотности) в газовой фазе
- •4. Полиэтилен среднего давления (высокой плотности)
- •4.1. Особенности получения и свойства полиэтилена среднего давления
- •Свойства конструкционных материалов на основе полиэтилена
- •4.2. Производство полиэтилена среднего давления в жидкой фазе
- •5. Сверхвысокомолекулярный полиэтилен
- •5.1. Особенности получения сверхвысокомолекулярного полиэтилена
- •Влияние строение алюминийорганического соединения на степень восстановления титана и молекулярную массу полиэтилена низкого давления
- •5.2. Свойства сверхвысокомолекулярного полиэтилена
- •Основные структурные характеристики свмпэ и пэнд
- •Основные свойства свмпэ и пэнд
- •6. Линейный полиэтилен высокого давления
- •Технологии производства линейного полиэтилена
5.1. Особенности получения сверхвысокомолекулярного полиэтилена
Сверхвысокомолекулярным полиэтиленом (СВМПЭ) называют разновидность полиэтилена низкого давления (ПЭНД) со средней молекулярной массой 1000000 – 10000000. В англоязычной литературе принят термин ultra high molecular weight polyethylene (UHMWPE), также встречаются термины high-modulus polyethylene (HMPE) и high-performance polyethylene (HPPE). Этот материал обладает высокими механическими и физическими свойствами, благодаря которым нашел широкое применение в промышленности. Наиболее примечательны его химическая инертность, смазывающие способности, высокая ударная вязкость и абразивная устойчивость.
Для увеличения молекулярной массы полиэтилена при использовании классических катализаторов Циглера – Натта необходимо обеспечить условия формирования каталитического комплекса, при которых титан находится в наименьшей степени окисления. В первую очередь это достигается применением в качестве алкилирующего компонента системы сильного восстанавливающего агента. В табл. 2 показано, как строение алюминийорганического соединения влияет на степень восстановления титана и молекулярную массу полиэтилена низкого давления [2].
Таблица 2
Влияние строение алюминийорганического соединения на степень восстановления титана и молекулярную массу полиэтилена низкого давления
Алюминийорганическое соединение |
Степень восстановления титана, % |
Молекулярная масса |
Al(C2H5)2H |
96 – 98 |
440000 – 500000 |
Al(C2H5)3 |
83 – 85 |
350000 – 430000 |
Al(C4H9)3 |
76 – 78 |
250000 – 300000 |
Al(C8H17)3 |
58 – 60 |
140000 – 180000 |
Al(C2H5)2Cl |
48 – 50 |
130000 – 135000 |
При использовании каталитической системы TiCl3 – алкилалюминий образуется значительно более высокомолекулярный полиэтилен низкого давления, чем при использовании TiCl4, однако активность первой каталитической системы ниже. Поэтому для синтеза СВМПЭ, как правило, используется смесь алкилалюминия с четыреххлористым титаном. Повышению молекулярной массы полиэтилена в этом случае способствует увеличение мольного соотношения алюминийорганическое соединение – TiCl4. Для синтеза СВМПЭ могут быть использованы любые алюминийорганические соединения, однако такой слабый восстановитель, как Al(C2H5)2Cl, должен быть взят в большом избытке, чтобы обеспечить нужную степень восстановления титана. Это приводит к повышенному расходу алюминийорганического соединения, что делает каталитические системы со слабовосстанавливающими агентами не технологичными.
Применение в качестве алюминийорганических соединений таких сильных восстановителей, как диалкилалюминийгидрид или триалкилюминий, обеспечивающих степень восстановления Ti до 80 – 98 %, позволяет при высокой интенсивности процесса синтезировать СВМПЭ с молекулярной массой более 1000000. При этом мольное соотношение алюминийорганическое соединение – TiCl4 должно составлять от 2/1 до 3/1. Также к росту содержания титана с пониженной степенью окисления приводит увеличение длительности взаимодействия компонентов каталитического комплекса и температуры их взаимодействия. Таким образом, при получении СВМПЭ в присутствии каталитической системы на основе алюминийорганического соединения и четырёххлористого титана регулирование молекулярной массы начинается уже на стадии формирования каталитического комплекса.
Способствует повышению молекулярной массы СВМПЭ использование диалкилалюминийгидридов, в которых имеется некоторое количество алкоксигрупп, поскольку наличие кислородосодержащих лигандов в активных центрах снижает скорость обрыва растущих макроцепей.
В более узких пределах можно регулировать молекулярную массу СВМПЭ на стадии полимеризации, меняя температуру реакционной среды. Вследствие того, что энергия активации ограничения цепей превышает энергию активации их роста, с понижением температуры молекулярная масса полимера растет. Однако существенное снижение температуры в реакторе приводит к затруднениям с теплосъемом и уменьшению выхода полимера, поэтому для конкретной аппаратурно-технологической схемы получения СВМПЭ температурный интервал полимеризации имеет ограничения.
Помимо систем алюминийорганическое соединение – TiCl4, при получении СВМПЭ используются различные соединения переходных металлов IV – VIII групп в гомогенном, гетерогенном и нанесенном на носитель виде.
В настоящее время широко исследуется и применяется большое количество каталитических систем, не с одним центром полимеризации, как в традиционно используемых катализаторах Циглера – Натта, хромовых и ванадиевых катализаторах, а имеющих несколько центров полимеризации. К таким каталитическим системам относят металлценовые катализаторы, которые представляют систему из трех компонентов: металлорганического комплекса, сокатализатора и носителя. Последний отсутствует при проведении полимеризации в растворе, а металлорганический комплекс составляет всего 1 – 2 % от массы катализатора.
Обычно сокатализаторами являются оксиды алюминия и фторированные органоборатные смеси. Активность таких катализаторов в 2 – 5 раз превышает активность классических катализаторов Циглера –Натта.
Рассмотрим механизм полимеризации на металлоценовом катализаторе на примере цирконоценовой каталитической системы.
Простейший представитель цирконоценов представляет из себя соединение Zr4+ с двумя циклопентадиенил-анионами:

(бис-(η6-циклопентадиенил)дихлорид циркония).
Одно из достоинств металлоценовых катализаторов состоит в возможности получения полимеров регулярного строения. В этом случае используют несимметричные цирконоценовые комплексы с инденильным лигандом:

П
ри полимеризации этилена стереорегулярность строения не может проявиться, поэтому используют более дешевый тип каталитической системы. Связь Zr–Cl в таких соединениях очень неустойчива, и для замены ее более стабильной связью Zr–СH3 используют сокатализатор метилалюмоксан: – [Al – O]n – .CH3
В результате атомы хлора в цирконоценовом соединении заменяются на метильные группы:

Далее происходит элеминирование одной CH3-группы и образование нестабильного комплекса, в котором цирконий стабилизирован слабой α-агостической связью с атомами водорода оставшейся метильной группы:

Образование π-комплекса с двойной связью мономера и последующие перегруппировки можно представить схемой:


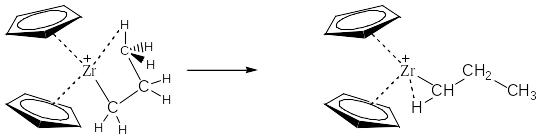
и далее по аналогичному механизму:

Особенно важно то, что на металлоценовых катализаторах можно получать полиэтилен с узким молекулярно-массовым распределением при высокой скорости процесса. Скорость полимеризации может быть увеличена путем повышения соотношения метилалюмоксан / металлоцен в каталитической системе. Молекулярная масса может контролироваться изменением температуры проведения реакции.
