
- •Лабораторная работа №1
- •Галогенопроизводные алифатических углеводородов Опыт 1. Получение хлорэтана
- •Опыт 2. Щелочной гидролиз алкилгалогенидов (реакции нуклеофилыюго замещения)
- •Опыт 3. Свойства хлороформа
- •Опыт 5. Реакции окисления этилового спирта
- •Опыт 6. Получение простого диэтилового эфира
- •Опыт 7. Получение глицерата и гликолята меди
- •Фенолы Осторожно! Фенолы вызывают ожоги кожи. Опыт 8. Образование и разложение фенолятов
- •Опыт 9. Взаимодействие фенола с бромной водой
- •Опыт 10. Окисление фенола
- •Опыт 11. Реакция фенола с азотистой кислотой
- •Опыт 12. Цветные реакции фенолов
- •Опыт14. Некоторые способы получения альдегидов
- •Опыт 15. Реакции окисления альдегидов
- •Опыт 16. Альдольная и кротоновая конденсация уксусного альдегида и его осмоление
- •Опыт 17. Получение ацетона пиролизом ацетата кальция
- •Опыт 18. Реакция ацетона с гидросульфитом натрия (реакция нуклеофильного присоединения)
- •Опыт 19. Реакции замещения карбонильного кислорода
- •3.2.Ароматические карбонильные соединения Опыт 20. Окисление бензальдегида аммиачным раствором гидроксида серебра (реакция «серебряного зеркала»)
- •Опыт 21. Реакция с фенилгидразином (получение фенилгидразона бензойного альдегида)
- •Опыт 22. Получение беизальанилина (основание Шиффа)
- •Опыт 24. Некоторые свойства уксусной кислоты и ее солей
- •Опыт 25. Получение высших жирных кислот и их свойства
- •4.2. Ароматические кислоты и их производные Опыт 26. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
- •Опыт 27. Отношение бензойной и коричной кислот к перманганату калия
- •Опыт 28. Реакции бензойной и салициловой кислот с хлоридом железа (III)
- •Опыт 29. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
- •4.3. Непредельные карбоновые кислоты Опыт 30. Свойства олеиновой кислоты
- •4.4. Двухосновные карбоновые кислоты Опыт 31. Получение щавелевой кислоты и ее свойства
- •Опыт 32. Получение ангидрида янтарной кислоты
- •Опыт 33. Образование фталевого ангидрида
- •4.5. Сложные эфиры предельных одноосновных кислот Опыт 34. Получение сложных эфиров предельных кислот (реакция этерификации)
- •Опыт 35. Гидролиз этилацетата
- •Жиры и масла Опыт 36. Определение непредельности растительного масла реакцией с бромной водой (тяга)
- •Опыт 37. Взаимодействие растительного масла с водным раствором перманганата калия (реакция Вагнера)
Опыт 17. Получение ацетона пиролизом ацетата кальция
Реактивы и оборудование: ацетат кальция (безводный); газоотводные трубки, изогнутые под тупым углом, пробирки.
В сухую пробирку насыпают безводный ацетат кальция (высота слоя 3—4 см) и равномерно распределяют его по нижней ее стенке. Пробирку закрывают пробкой с газоотводной трубкой, изогнутой под тупым углом, и закрепляют в лапке штатива с наклоном в сторону пробки. Конец газоотводной трубки опускают в пробирку-приемник, содержащую 1,5—2 мл дистиллированной воды. Сначала равномерно прогревают всю пробирку с ацетатом кальция, а потом прокаливают ее, начиная со дна. Соль плавится, а затем разлагается с образованием ацетона:
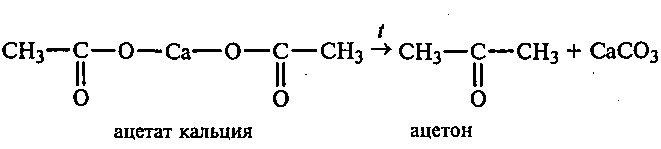
Пары ацетона отгоняются и растворяются в воде, находящейся в пробирке-приемнике. Через 6—8 мин объем жидкости в приемнике увеличивается вдвое. Ощущается характерный запах ацетона.
После прекращения вспенивания в нагреваемой пробирке на ее дне остается карбонат кальция, который можно обнаружить после охлаждения пробирки реакцией с 10%-ной соляной кислотой.
Ацетон в пробирке-приемнике можно обнаружить иодоформной пробой (проба Лебена) или реакцией с нитропруссидом натрия (проба Легаля).
Опыт 18. Реакция ацетона с гидросульфитом натрия (реакция нуклеофильного присоединения)
Реактивы и оборудование: насыщенный раствор гидросульфита натрия NaHS03, ацетон, 10%-ная соляная кислота, 10%-ный раствор карбоната натрия; стаканы на 50—100 мл, лед, пробирки.
В пробирку наливают 3 мл насыщенного раствора гидросульфита натрия и добавляют при энергичном встряхивании 2 мл ацетона. Разогревшуюся реакционную смесь охлаждают в стакане со льдом. Через некоторое время в пробирке выпадает кристаллический осадок гидросульфитного производного ацетона:
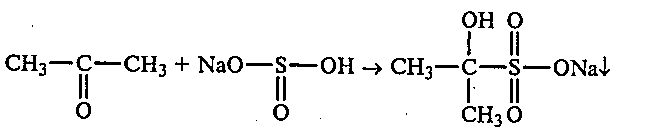
Если осадок не появляется, то кристаллизацию вызывают потиранием стеклянной палочкой о стенку пробирки.
Необходимо отметить, что в эту реакцию вступают альдегиды и только те кетоны, которые имеют метальную группу, непосредственно связанную с карбонильной группой.
Напишите механизм реакции образования гидросульфитного производного ацетона и формальдегида.
Эту реакцию применяют для очистки альдегидов и кетонов и для выделения их из трудно разделяемых смесей. Отфильтрованное от растворимых примесей гидросульфитное производное легко гидролизуется под действием разбавленной соляной кислоты или раствора соды.
Опыт 19. Реакции замещения карбонильного кислорода
Реактивы и оборудование: уксусный альдегид, ацетон, насыщенный раствор солянокислого фенилгидразина, ацетат натрия, солянокислый гидроксиламин, карбонат натрия (безводный); стаканы химические на 100 мл, лед, пробирки.
19.1. Получение фенилгидразона уксусного альдегида. В пробирку приливают 1 мл насыщенного раствора солянокислого фенилгидразина, добавляют небольшое количество кристаллического ацетата натрия и при встряхивании вносят 1 мл уксусного альдегида. Наблюдают выпадение кристаллов фенилгидразона уксусного альдегида:
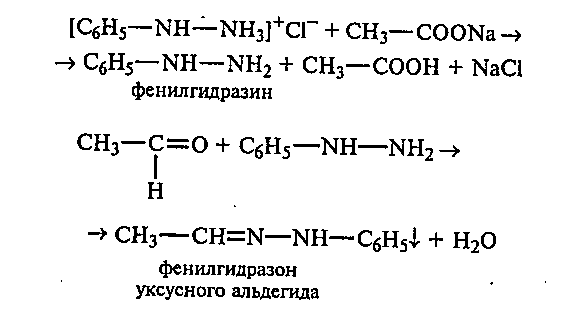
Рассмотрите механизм реакции образования фенилгидразона уксусного альдегида.
19.2 Получение оксима ацетона. В пробирке растворяют 1 г солянокислого гидроксиламина в 3 мл воды. Полученный кислый раствор нейтрализуют ~ 0,7 г безводного карбоната натрия. При встряхивании пробирки наблюдают выделение оксида углерода (IV). Пробирку с полученным раствором охлаждают в стакане с ледяной водой, а затем добавляют к раствору 0,7 мл ацетона при встряхивании. Смесь разогревается, снова выделяется углекислый газ и появляются бесцветные кристаллы оксима ацетона. При дальнейшем охлаждении пробирки количество кристаллов увеличивается.
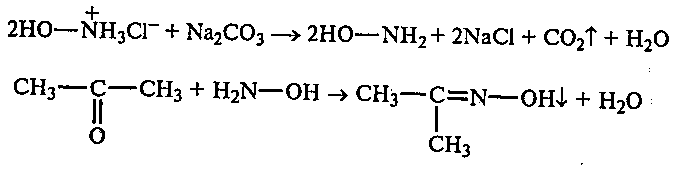
оксим ацетона
Напишите механизм реакции образования оксима ацетона.
