
- •1. Тепловое излучение.
- •Характеристики теплового излучения.
- •Закон Кирхгофа
- •Квант. Гипотеза Планка. Ф-ла Планка.
- •Вольт-амперная характеристика (вах) внешнего фотоэффекта
- •Эффект Комптона.
- •Квантовые объясн. Кемптон-эффекта.
- •Потсулаты Бора
- •Опыты Франка и Греца
- •Теория Бора для атома водорода и водородоподобных систем
- •Соотношения неопред. Гейзенберга
Квантовые объясн. Кемптон-эффекта.
Эф. Комптона является наиболее ярким примером справедл. выполнения квант. теории света. Явление объясн. на основании з-нов сохр. энергии и импульса, выполн. при упругом столкн. со слабосвязанными эл-нами вещ-ва. Внеш. эл-ны, слабосвяз. с ядром атома под действ. жёстких R-лучей могут легко уходить за пределы атома, оставаясь в образце. Слабосвяз. эл-ны, потеряв связь с ядром атома становятся относительно (не полностью) свободны. Применяем з-н сохр. энергии.
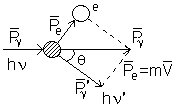
Излучение прежней длины волны присутств. по причинам: не все фотоны R-лучей взаимод. со слабосвяз. эл-нами, а с атомами в целом, поэтому атом поглащ. значит. меньшую энергию от фотона, поэтому часть фотонов проходит.
До столкновения.
|
|
Фотон |
Электрон |
|
Энергия |
h |
m0C2 (энергия покоя) |
|
Импульс |
|
0 |
После столкновения.
|
|
Фотон |
Электрон |
|
Энергия |
h |
mC2 (полная энергия) |
|
Импульс |
|
|
1) З-н сохранения энергии: h+m0C2= =h+m0C2 h=h+(m-m0)C2=h+Te
2) З-н сохр. импульса:
![]() .
.
Перейдём к скалярной
записи (см. рис). Из треугольника, содержащ.
след.:
![]() После
ряда упрощ. получают выражение вида:
После
ряда упрощ. получают выражение вида:![]() .
.
![]() .
.
Явление Комптона с примен. з-нов сохр. энергии и импульса полн. объясняется по квант. представлениям. Комптон-эффект набл. также для -излучения.
8.
У водорода в спектре
4 линии:
Спектры отражают
внутреннюю структуру атома этого
элемента. В спектре любого элемента
присутствуют т.н. спектральные серии.
Спектральной
серией наз.
совокупность линий, расположенных
определённым образом, длины волн которых
подчиняются одной определённой
закономерности. Обобщённая
формула Бальмера (1)...
![]() - обобщённая формула Бальмера, где
n=3,4,5...; R - постоянная Ридберга, R=1,1·107м-1.
Значение n соответствует определённой
линии данной серии Бальмера. (2)...
- обобщённая формула Бальмера, где
n=3,4,5...; R - постоянная Ридберга, R=1,1·107м-1.
Значение n соответствует определённой
линии данной серии Бальмера. (2)...
![]()
![]() Удалось обнаружить
спектры в ультрафиолетовой и инфракрасной
области. УФ - Лайман
Удалось обнаружить
спектры в ультрафиолетовой и инфракрасной
области. УФ - Лайман
![]() ,
n=2,3.. ИК - Пашен
,
n=2,3.. ИК - Пашен![]() ,
n=4,5,6...
,
n=4,5,6...
Брэкет (ni=4)Пфунд
(ni=5)
Хэмтрс (ni=6)
(3)...
![]() ni
- соответствует определённой спектральной
серии;
ni
- соответствует определённой спектральной
серии;
![]() Спектральные
серии Излучение
спектров газами добиваются с помощью
либо эл. поля, либо нагреванием. Физики
установили, что атомарные газы любых
элементов посылают дискретное излучение.
В спектре наблюдаются только определённые
длины волн.
Спектральные
серии Излучение
спектров газами добиваются с помощью
либо эл. поля, либо нагреванием. Физики
установили, что атомарные газы любых
элементов посылают дискретное излучение.
В спектре наблюдаются только определённые
длины волн.
9.
Опытами Резерфорда было показано, что в центне атома располагается заряженное массивное ядро. Размер атома ~2r1~1010м. Размеры ядер~1015м (1 Ферми). В физике долго существовала протонно-электронная модель, которая предполагала что ядро состоит из протонов и электронов. Эту модель отбросили и в 1932 г. была принята протонно-нейтронная модель. Согласно ей, ядро состоит из двух видов ядерных частиц: протонов и нейтронов. Протон - это частица с зарядом электрона, но со знаком “+”. mp=1,6726·10 кг. Нейтрон электрически нейтрален. mn=1,6749·10 кг. Вместе протоны и нейтроны называют нуклонами. Протоны и нейтроны обладают спинами.
![]() и для протона и для
нейтрона.
и для протона и для
нейтрона.
Протоны и нейтроны являются фермионами. имеют место магнитные спиновые моменты.

![]() - ядерный магнетон.
- ядерный магнетон.
Резерфорд предложил ядерную (планетарную) модель атома. Атом представл. собой тело, внутри которого наход. ядро R=101510м с зарядом +Ze. Вокруг него вращаются эл-ны, образуя электронную оболочку атома. Суммарный заряд эл-нов Ze. На основании нейтральности атома он сделал вывод что всего Z эл-нов. Согласно Резерфорду, радиусы орбит эл-нов могут быть произвольными. Ограничения на радиусы нет. Движение эл-на ускоренное эл-н испускает энергию. С позиций классической электродинамики электрон вращается по спирали и падает на ядро, т.к. радиус уменьшается.
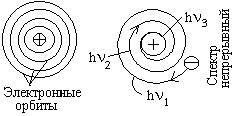
Атом испускает близкие энергии h - равномерный спектр. Атом по Ридбергу представляет электродинамически неустойчивую структуру (за короткое время электрон должен упасть на ядро).
10.
