
- •Методичні рекомендації до виконання лабораторних робіт з дисципліни «Техніка єксперименту в хімії»
- •7.091602- Хімічна технологія неорганічних речовин
- •Дослід 2. Визначення температури плавлення. 19
- •Додаток №1. Основні операції, які виконуються в
- •Додаток №2. Схеми стандартних приладів для роботи в органічному практикумі. 37
- •Дослід 2. Визначення температури плавлення.
- •Дослід 5. Кристалізація.
- •Дослід 7 . Сублімація.
- •Завдання.
- •Додаток № 1. Основні операції, які виконуються в хімічній лабораторії.
- •Фільтрування
Дослід 7 . Сублімація.
Сублімація (від лат. sublimo — підношу, піднімаю) — перехід кристалічної речовини безпосередньо в пару, минаючи рідку фазу. Сублімація належить до фазового переходу першого роду. Сублімація відбувається за температури, нижчої за температуру потрійної крапки. Для здійснення сублімації до речовини потрібно прикласти енергію, що називають енергією сублімації.
Хід роботи. У порцелянову чашку або тигель вмішують 0,5-1,0 г технічного нафталену або технічної кислоти бензойної, накривають скляною лійкою і нагрівають (мал. 5). При нагріванні бажано не досягати температури плавлення.
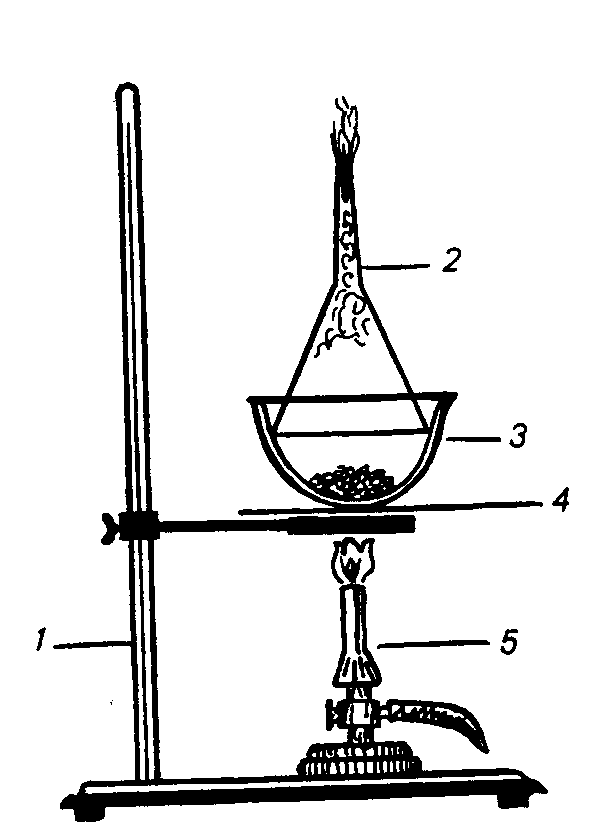
Мал. 5. Установка для сублімації:
/ — штатив ; 2 — лійка; 3 — тигель; 4 — азбестова сітка; 5 — газовий пальник
Охолоджують. На стінках лійки виділяються кристали нафталену або кислоти бензойної. Очищену речовину зскрібають на чисте предметне скло.
Задача.
Замалюйте прилад і запишіть результати досвіду.
Лабораторна робота №5.
Методи очищення рідких речовин.
Дослід 8.
Проста перегонка при атмосферному тиску.
Перегонка є найбільш важливим широко використовуваним методом очищення органічних рідин і поділу рідких сумішей.
Цей метод полягає в кип'ятінні і випарюванні рідини з наступною конденсацією пар у дистиллат. При зниженні тиску температура кипіння знижується,що дозволяє переганяти высококипящие рідини й олії. Такий метод називається вакуумною перегонкою.Найпростіша перегонка є ефективною тільки в тому випадку, якщо компоненти суміші відрізняються по температурах кипіння не менш, ніж на 60о. В усіх других випадках речовини піддають фракційній перегонці з використанням різного типу перегінних колон. Найпростішим стовпчиком ( дефлегматор Вигре), може бути колонка з наповнювачем, так називана “насадочная“. За допомогою високоефективного набивного стовпчика розділяють компоненти з дуже близькими температурами кипіння (розходження в температурах кипіння до 2о).
При атмосферному тиску звичайно переганяють речовини з температурами кипіння от 50ос до 150ос (при більш високій температурі кипіння речовини виникає небезпека його термічного розкладання).
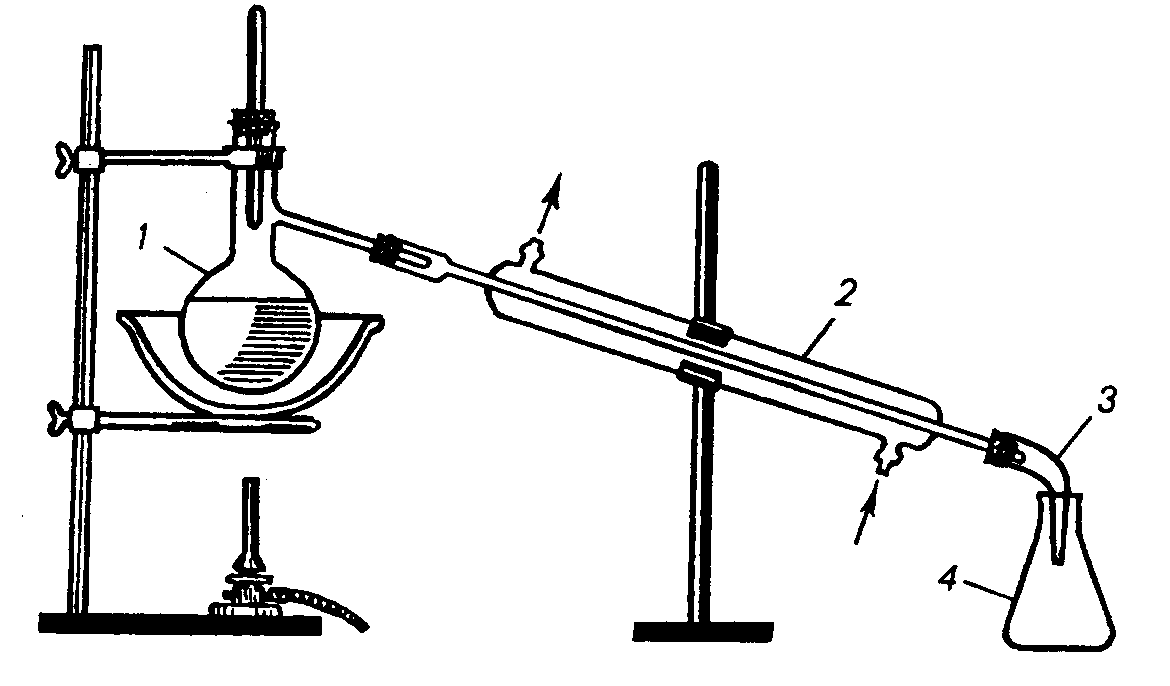
Рис . Прилад для простої перегонки рідин.
1 – колба Вюрца; 2 – холодильник Лібіха; 3 – алонж; 4 - приймальна колба.
Завдання.
Зберіть установку для простої перегонки рідини. Відженіть ефірну фракцію, що утворилася в ході виконання досліду 5. Зробіть висновки і замалюйте схему установки.
Лабораторна робота №6.
Фракційна перегонка рідини. Ознайомлення з методом на прикладі фракційної перегонки нафти.
Дослід 9. Фракційна перегонка нафти.
Фракційну перегонку використовують для розділення складних сумішей на окремі фракції, що киплять за визначених інтервалів температур. Прикладом фракційної перегонки може бути перегонка нафти. За допомогою такої перегонки спочатку добувають три головні фракції: бензинову (інтервал температур — 38— 180 °С), гасову (180 — 270 °С) і мазут (понад 280 °С). У подальшому окремі фракції розділяють на підфракції (повторною перегонкою). Наприклад, з бензинової фракції повторною перегонкою добувають н-пентан, газолін, або петролейний етер, авіаційний бензин, автомобільний бензин і лігроїн.
Задача.
Замалюйте схему прилада. Здійсните фракційну перегонку нафти. Визначите густину кожної отриманої фракції. Зробить висновки.
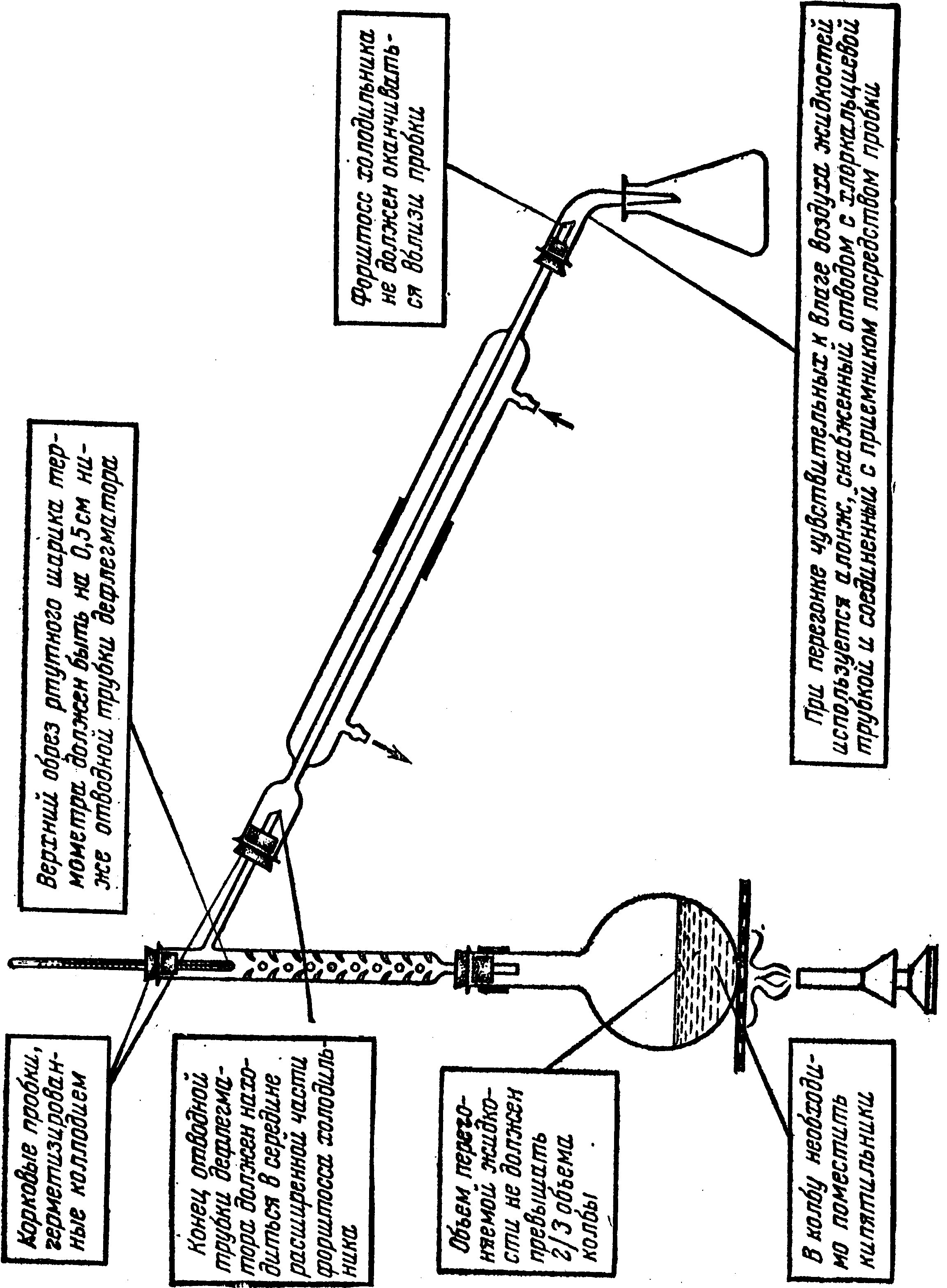
Мал. Прилад для фракційної перегонки рідини.
Лабораторна робота №7.
Хроматографічні методи виділення, ідентифікації й очищення хімічних речовин. Паперова хроматографія і хроматографія в тонкому шарі.
Хроматографія – метод розділення, аналіза, фізико-хімічних досліджень сполук, ідентифікації й випробування на чистоту. Дуже ефективним методом розділення сумішей речовин на компоненти є хроматографія – метод заснований на тому, що під час проходження досліджуваного розчину крізь шар порошкоподрібненого нерозчинного матеріалу (сорбенту) окремі компоненти суміші сорбуються (утримуються) з різною силою. Під час розділу компонентів в суміші окремі сполуки утворюють окремі смуги або зони, звідки потім можуть бути вилученими.
Усі види хроматографії ґрунтуються на різній рухливості розчінених речовин під час їхнього проходження крізь систему, тобто на розподілі компонентів суміші між двома фазами – нерухомої (сорбент) і рухомої (елюент) що проникає крізь нерухому.
Розрізняють тонкошарову і паперову хроматографії.
Дослід 10. Хроматографія на папері.
Хроматографія на папері відноситься до мікрометоду. В якості носія нерухомої фази використовують спеціальний фільтрувальний папір, що володіє рівномірною щільністю і чистотою.
Речовини наносять на лінію старту накресленої олівцем на відстані 2-3 см від центра фільтрувального папера, спеціальним тонким капіляром наносять розчини речовин. Роблять в центрі паперу отвір і вставляють спеціальний джгут, який подає елюент і розміщають папір між двома чашками Петрі. Положення плям по закінченні хроматографування і виявлення характеризується значенням Rf :
Rf
=
![]()
де – Х – відстань, пройдена речовиною від лінії старту до центра плями;
У – відстань, пройдена елюентом від лінії старту до лінії фінішу.
Значення Rf величина постійна для даної речовини і використовується для ідентифікації, залежить від температури, розчинника, якості папера. Тому хроматографування проводять у присутності сполук з відомим значенням Rf (сполуки – свідки).
Хід роботи. На папір для паперової хроматографії, що відповідає розміром чашки Петрі наносять розчини глюкози, фруктози, меду, соків солодких фруктів, у центр вставляють джгут, який подає з нижньої чашки елюент складу: бутанол:оцтова кислота:вода – 4:1:5 і накривають відповідних розмірів чашкою Петрі. Коли елюент досягає країв чашки, папір виймають, висушують і виявляють. Для виявлення плям використовують 1-% розчин резорцинолу, до 10 мл якого додають 90 мл 2н HCl, яким і зрошують хроматограмму. Папір висушують при температурі 70-100ºС. Виявленні плями використовують для розрахунку Rf .
Виявленні плями мають для кожного вуглеводу своє забарвлення: фруктоза – червоне, ксилоза – синє, арабіноза – зелене, галактоза, глюкоза, маноза – сіре.
Завдання. Замалюйте отриману хроматограму і розрахуйте для кожного вуглеводу Rf. .
Дослід 11. Тонкошарова хроматографія.
Крім хроматографії на папері для аналізу й ідентифікації використовують тонкошарову хроматографю. У цьому випадку використовують спеціальні пластинки з різноманітними шарами сорбентів, наприклад, silufol. Техніка виконання тонкошарової хроматографії аналогічна паперової хроматографії. У якості хроматографічних камер використовують ексикатори, кристалізатори, склянки, що мають пришліфовані кришки. На дно камери наливають елюент, щоб висота шару не перевищувала лінію старту на пластинці.
Хід роботи.
1. Виявлення кислоти аскорбінової. На пластинку silufolа, що відповідає розмірам хроматографічної камери, на відстані 1-2 см від нижнього краю нанесіть лінію старту. Потім, за допомогою капіляру на відстані 1-1,5 см один від одного нанесіть краплю 1-% ного розчину кислоти аскорбінової, соків салатного перцю, смородини, малини і поміщають пластинку в хроматографічну камеру. У якості елюенту використовують етанол-гексан (3:1). Для виявлення плям висушену пластинку поміщають в ексикатор з парами йоду. Виявленні плями використовують для розрахунку Rf .
2. Виявлення нітроанілінів. Аналогічно виявленню кислоти аскорбінової 1-%ні розчини орто-, пара- мета-нітроанілінів у бензені тонким капіляром наносять на пластинку, як свідків, і їхню суміш. У якості елюенту використовують бензен-етилацетат (4:1). Плями не виявляють так, як вони забарвлені, розраховують Rf індивідуальних нітроанілінів і в суміші.
Задача.
Замалюйте отриману хроматограму і розрахуйте Rf .
Лабораторна робота №8.
Вступ в органічний синтез.
На практичній частині даного заняття студент вперше приступає до виконання роботи з органічного синтезу. Перед початком роботи студент повинний ознайомитися з вимогами по веденню лабораторного журналу. Схема за якою оформляються синтези в робочому журналі (табл. 1).
Таблиця 1.
№ п-п |
Вихідні речовини |
Кількість речовин необхідних для синтезу |
Надлишок |
|||||||
Реакти-ви і їх форму-ли |
Молекулярна маса |
Данні із здовідника, Тпл, Ткип. |
Концентрація реаген тів |
По рівнян-ню реакції |
За методикою |
в молях |
в % |
|||
в молях |
в грамах |
у мл |
||||||||
в молях |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
Якщо в методиці кількості реагентів приводяться в молях то їхній необхідно перевести в грами, а для рідин – у мілілітри. На основі зроблених записів роблять висновок про те, які речовини беруться в надлишку.
Звіт. У звіті студент повинний детально описати механізм реакції, пояснити роль каталізаторів, прийоми зсуву рівноваги у випадку зворотної реакції. Наприкінці звіту заповнюють таблицю 2 виходи синтезованої речовини.
Таблиця 2.
Синтезована речовина і його формула |
Даності речовини |
Вихід речовини |
|||
Встановленні в роботі |
Даності літератури |
В грамах |
В % |
||
Від теоретичного |
Від методиного |
||||
|
|
|
|
|
|
Завдання.
Запротоколюйте запропоновану викладачем методику органічного синтезу. Замалюйте схему використовуваного лабораторного приладу. Заповните таблицю 1.
Лабораторна робота №9.
Органічний синтез.
Завдання.
Студент збирає необхідний для синтезу лабораторний прилад, та й у відповідності із вказаною вище методикою виконує необхідний синтез, виділяє, очищує та ідентифікує отриману речовину, заповнює таблицю 2.
Лабораторна робота №10.
Залікове заняття.
