
- •Методичні рекомендації до виконання лабораторних робіт з дисципліни «Техніка єксперименту в хімії»
- •7.091602- Хімічна технологія неорганічних речовин
- •Дослід 2. Визначення температури плавлення. 19
- •Додаток №1. Основні операції, які виконуються в
- •Додаток №2. Схеми стандартних приладів для роботи в органічному практикумі. 37
- •Дослід 2. Визначення температури плавлення.
- •Дослід 5. Кристалізація.
- •Дослід 7 . Сублімація.
- •Завдання.
- •Додаток № 1. Основні операції, які виконуються в хімічній лабораторії.
- •Фільтрування
Дослід 2. Визначення температури плавлення.
Температура плавлення — одна з важливих констант твердих речовин. Плавлення — перехід речовини з кристалічного стану в рідкий під час нагрівання. Воно є фазовим перехідом першого роду, що відбувається з поглинанням теплової енергії. Під час плавлення збільшується питомий обсяг речовини (за винятком брому, кальцію і деяких інших речовин). Плавленню передують посилена розупорядкованість кристалів і поява рідких ділянок біля міжкристалічних частин речовини. Температура плавлення чистих речовин і твердих розчинів залежить від тиску, напруженості електричних або магнітних полів. Температура плавлення чистих речовин при стабільних умовах завжди одна й та сама і може бути критерієм їхньої чистоти. Тверда органічна речовина плавиться у вузькому температурному інтервалі в межах 0,5-1 °С. Наявність домішок найчастіше знижує температуру плавлення на 5-10 °С. Кристалічні полімери плавляться в інтервалі температур, що іноді досягає десятків градусів і залежить від хімічної природи макромолекул, їхнього молекулярно-масового розподілу й умов кристалізації. Для аморфних твердих речовин температура плавлення збігається з температурою розм'якшення, за якої під час нагрівання різко зростає деформованість зразка.
Температуру плавлення найзручніше визначати на прикладі плавлення нафталену, бензойної кислоти. Нафтален — ароматичний вуглеводень, молекулярна формула — С10Н8 . Це біла кристалічна речовина, має різкий специфічний запах, важко розчиняється у воді, добре — у багатьох органічних розчинниках. Виділяють кристалізацією з кам'яновугільної смоли (карболової і креозотової олій, що киплять відповідно при 160—130 і 230 — 270 °С). Використовується як, вихідна речовина для синтезу фенолфталеїну (пургену), багатьох барвників, медикаментів, пестицидів і т.п..
Хід роботи. На предметне скельце насипають невелику кількість бензойної кислоти, розтирають скляною паличкою і відкритим кінцем капіляра набивають речовину. Щоб перемістити речовину з відкритого кінця в заплавленний, його кидають у скляну трубку поставлену вертикально на лабораторному столі. Капіляр закріплюють у лапці термометра і поміщають у прилад для визначення температури плавлення. Нагрівання ведуть з розрахунком, щоб температура за хвилину підвищувалася в середньому на 2-3 °С. У момент утворення меніска на поверхні стовпчика речовини, вміщеної в капіляр, записують температуру плавлення речовини або їхньої суміші.(мал. 2).
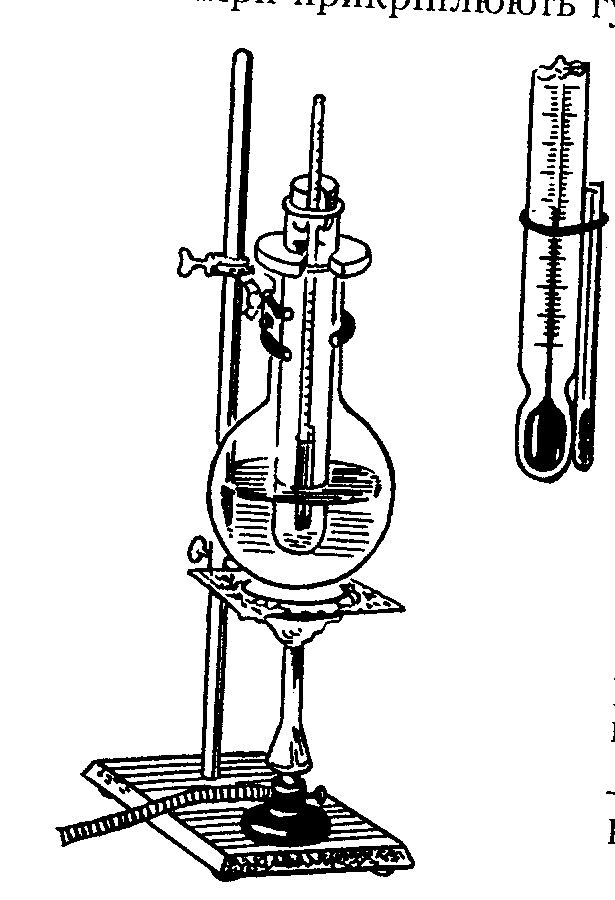
Мал 2. Прилад для визначення температури плавлення
Задача. Замалюйте прилад. Запишіть результати дослідів. Поясніть різницю в температурах плавлення чистих речовин і суміші.
Дослід 3. Визначення температури кипіння спирту етилового.
Температура кипіння — важлива константа органічної речовини. За температурою кипіння ідентифікують органічна речовину і визначають її чистоту. Температурою кипіння вважається така температура, за якої тиск пари рідини над її поверхнею дорівнює атмосферному тискові. Речовина вважається тім чистішою, чим менший інтервал температур початку і кінця кипіння. Такий інтервал під час звичайних перегонок знаходиться у вузьких температурних межах — 0,5-1 °С. Домішки сторонніх речовин значно змінюють показники температури кипіння.
Хід роботи. У широку пробірку наливають 2-3 мл спирту етилового, опускають кип'ятильний камінчик, вставляють термометр на пробці з прорізом на висоті 2-5 см від рівня спирту етилового, нагрівають. Пари спирту після конденсації на термометрі рівномірно скапують назад у пробірку. На термометрі фіксують температуру кипіння.
Задача. Зберіть прилад і визначите температуру кипіння дистильованої води, спирту етилового і порівняєте з даними довідникової літератури.
Дослід 4. Визначення показника заломлення nД20.
Показником заломлення називають відношення швидкості розповсюдження світла у вакуумі до швидкості розповсюдження світла в досліджуваній речовині - це абсолютний показник заломлення і є важливої фізичною сталою для ідентифікації і визначення чистоти рідких речовин. На практиці визначають відносний показник заломлення – це відношення швидкості поширення світла в повітрі до швидкості поширення в досліджувальній речовині. Для визначення показника заломлення використовують прилади – рефрактометри (мал. 6).
Вимірювання проводять при температурі 200.3С і довжині хвилі 589.3 нм (лінія жовтого натрієвого полум'я). Прилади налаштовують за еталонними рідинами які додаються до приладу, або по дистильованій воді для якої пД20 =1.333.
Хід роботи. На площину вимірювальної призми (мал. 7) за допомогою піпетки, не торкаючись поверхні призми наносять декілька крапель спирту етилового й обережно закривають верхню вимірювальну голівку 4.
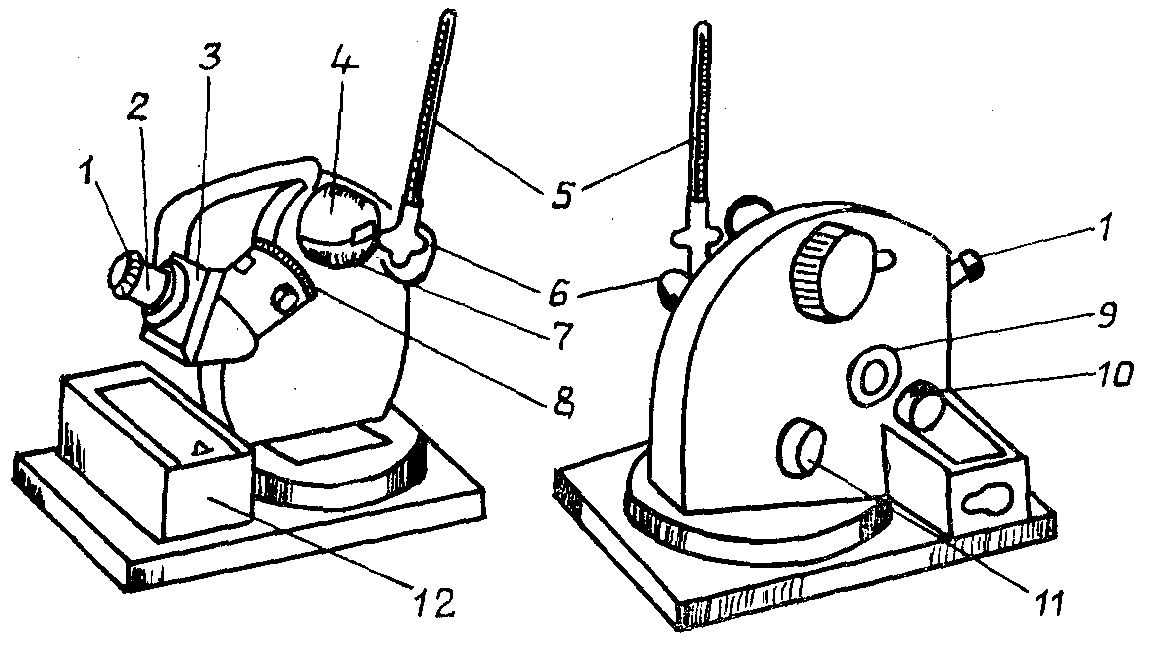
Рис. 6. Рефрактометр ИРФ-22:
1-окуляр; 2-зорова трубка; 3-гніздо для ключа; 4-верхня вимірювальна голівка; 5- термометр; 6-освітлювальне дзеркало; 7-нижня вимірювальна голівка; 8,11-маховички; 9-віконце; 10-дзеркало для висвітлення шкали; 12-пенал.
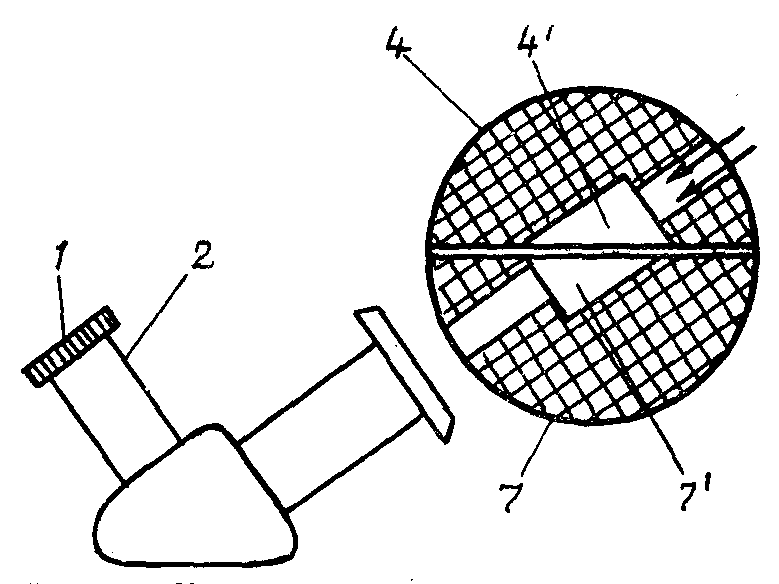
Рис. 7. Вимірювальна голівка рефрактометра ИРФ-22 у розрізі:
4,7- вимірювальні голівки; 4 -освітлювальна призма; 7-вимірювальна призма.
Освітлювальне дзеркало 6 встановлюють так щоб світло від джерела попадало до освітлювальної призми і рівномірно освітлювало поле зору. За допомогою маховика встановлюють чітку фазу розділу в центрі поля зору на перехресті волосків (мал. 8).
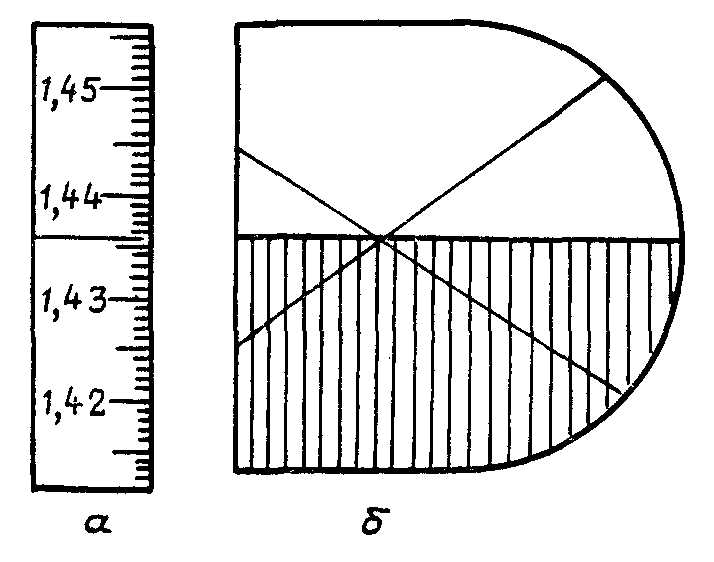
Мал.8. Зняття показників рефрактометра.
а-шкала; б-вид поля зору під час зняття показників.
Задача.
Визначте показник заломлення дистильованої води і спирту етилового. Порівняйте отримані данні з літературними значеннями. Зробить висновки.
Лабораторна робота №4.
Методи очищення кристалічних речовин.
