
- •1.Топливо. Классификация по агрегатному состоянию и способу получения.
- •2.Элементарный состав твердого и жидкого топлива
- •3.Рабочая масса. Элементарный состав. Внутренний и внешний балласт
- •4.Сухая масса. Элементарный состав. Формулы пересчета с рабочей массы на сухую.
- •5.Горючая масса. Элементарный состав. Пересчет с сухой и раб массы на горючую.
- •6.Органическая масса. Элементарный состав. Пересчет с горючей на органическую.
- •7.Влажность топлива. Внешняя и внутренняя. Способы определения.
- •8.Зола топлива. Способы определения. Сланцевая зола.
- •10. Летучие вещества, кокс, полукокс. Классификация кокса.
- •12) Жидкое топливо. Способы получения. Марки мазута
- •13) Газообразное топливо. Горючая и негорючая части.
- •14)Состав газообразного топлива
- •15)Углеродное число. Сущность метода. Формула.
- •16)Теплота сгорания. Размерность. Связь между низшей и высшей теплотой сгорания
- •17)Лабораторные работы определения теплоты сгорания твердого и тяжелого жидкого топлива
- •18)Лабораторные способы определения теплоты сгорания твердого и тяжелого жидкого топлива
- •19) Методика определения теплоты сгорания.
- •20)Расчетные методы определения теплоты сгорания твердого, жидкого и газообразного топлива
- •21) Условное топливо. Топливный коэффициент
- •22)Формулы вычисления теплоты сгорания смесей твердых, жидких, газообразных видов топлива.
- •23) Теоретический массовый расход кислорода на горение топлива
- •24) Теоретический массовый и объемный расходы воздуха на горение твердого и жидкого топлива(Выводы формул).
- •25) Состав продуктов полного сгорания твердого и жидкого топлива.
- •26)Количество трехатомных продуктов полного сгорания (масса и объем)твердого и жидкого топлива
- •27)Теоретический объем водяных паров образующихся при сгорании 1 кг твердого и жидкого топлива
- •28. Теоретический объем двухатомных и сухих газов в продуктах сгорания твердого и жидкого топлива. Суммарный теоретический объем продуктов сгорания.
- •31. Действительная масса газообразных продуктов сгорания (кроме сланцев).
- •32. Реакции горения компонентов газообразного топлива.
- •33.Теоретическое количество воздуха, необходимого для сжигания 1м3 газа (вывод формулы)
- •34 ) Теоретические объемы двухатомных, 3хатомных и сухих продуктов сгорания газообразного топлива
- •36) Действительные объемы двухатомных, трехатомных и сухих продуктов горения газообразного топлива
- •37)Действительный суммарный объем продуктов сгорания газообразного топлива
- •38)Топливная характеристика
- •39)Уравнение полного горения твердого и жидкого топлива
- •40)Определение количества сухих продуктов сгорания при неполном горении твердого и жидкого топлива
- •41)Определение горючих со,сн4,н2 составляющих продуктов неполного сгорания газообразного топлива
- •42)Определение коэффициента расхода воздуха при полном сгорании топлива
33.Теоретическое количество воздуха, необходимого для сжигания 1м3 газа (вывод формулы)
V0-min кол-во воздуха, необходимого для обеспечения полного сгорания 1м3 топлива при условии, что весь кислород воздуха и весь кислород топлива будут использованы при горении. Теоретически необходимого для полного сгорания 1м3 газа надо в 1/0,21=4,76 раз больше, чем кислорода. Теоретическое кол-во воздуха необходимого для сжигания газа:
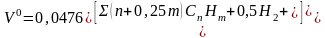 ,
м3/м3
,
м3/м3
CnHm-% содерж-е i-го углеводорода в 1 м3 топлива; H2,CO,H2S,O2-% содерж-е соот-го газа в 1 м3 топлива; n,m – число атомов соотв-но углерода и водорода в химич ф-ле i-го углеводорода.
34 ) Теоретические объемы двухатомных, 3хатомных и сухих продуктов сгорания газообразного топлива
Теоретический обьем сгорания газообразного топлива рассчитываются на основании
Стехиометрических реакций СО,H2.H2S.CnHm образуется двухатомный углерод СО2 ,SO2 и водяные пары
Для газообразного топлива теоретические объемы продуктов сгорания (м3/м3) определяются по формулам: а). объем двухатомных газов
VoN2 = 0,79 Vo + N2 / 100
б). объем трехатомных газов
VRO2 = 0,01[СO2 + СО + Н2S + ∑mCmHn] ;
CO2- углекислого газа по обьему в исходном газообразном топливе.
Оббьем водяного пара
VoH20 = 0,01(H2+HnS+ ∑m/2CmHn )+d/0.805*1000+v0d/0.805*1000
d- влагосодержание газа
d=13 г/м3
VoH20 = 0,01(H2+H2S+ 0,124 d+∑m/2CmHn )+0.016v0
в). объем сухих газов :
Voс.г. = VRO2 + VoN2
Vro=VN2=0.79V0+N2/100
Vгo=Vсг+VN20
VH20=VoH20+(α-1)Vo d/0.805*1000
VH20=V oH20+0.0161(ā-1) Vo
VN2=0.79V0+N2/100+0.79(α-1) V0
V02=0.21(α-1) V0
Если состав непред. Углеводородов СnH2n входящих в газ неизвестен,а общее их содержание не превышает 3 % то учитывается как С2H4
35) Теоретический обьем вод пара в продуктах горения газообразного топлива (при d≠13 г/м3 и d=13 г/м3)
При горении водорода
VгH20==(36/4)(Hp/100)/0.805=0.111Hp
2)при испарении влажного топлива
VтH20=Wp/100/0.805=0.0124Wp
3)Обьем форсуночного пара
VH2O=WФ/0,805=1,24Wф
Wф=0,3-0,35 кг/кг
4) Обьем водяного пара
VH20=Vod/1000/0.805
0.805- плотность водяного пара при d=13 кг/м3
VoH2O=0.111Hp+0.0124Wp+1.24Wф+0.0161V0
36) Действительные объемы двухатомных, трехатомных и сухих продуктов горения газообразного топлива
При полном сгорании топлива, продукты сгорания содержат газы: СО2, S2O, N2, О2 и пары воды Н2О, т. е. СО2+ S2O + N2 + О2 + Н2О = 100 %. Полный объем продуктов сгорания Vг (м3/кг) представляет собой сумму объемов сухих газов Vс.г. и водяных паров VН2О :
Vг = Vс.г. + VН2О
при этом Vс.г. = VRO2 + VN2 + VO2 , где VR2O =VCO2 +VSO2 -объем трехатомных газов,м3/кг VN2 +VO2 -объем двухатомных газов, м3/кг. A.При aт =1
Для газообразного топлива теоретические объемы продуктов сгорания (м3/м3) определяются по формулам: а). объем двухатомных газов
VoN2 = 0,79 Vo + N2 / 100
б). объем трехатомных газов
VRO2 = 0,01[СO2 + СО + Н2S + SmCmHn]
в). объем сухих газов :
Voс.г. = VRO2 + VoN2
г). объем водяных паров
VoH2O = 0,01[Н2S + Н2 + ∑(m/2)CmHn + 0,124dг ]+0,0161Vo
где dг -влагосодержание газообразноготоплива, отнесенное к 1 м3 сухого газа, г/м3;
д). полный объем продуктов сгорания
Voг = Voс.г. + VoН2О
Б. При aт >1 VR2=VN2+V02=V0N2+(α-1)V0
VH20=V0H20+ ((α-1)V0d)/0,805*1000 при d=13г/м3
VH20=V0H20+0,0161(α-1)V0 при d≠13 г/м3
VN2=0.79V0+(N2/100)+0.79(α-1)V0
V02=0.21(α-1)V0
Если состав непредельных углеводородов CnH2n, входящих в газ, неизвестен, а их общее содержание не превышает 3%, то в расчетах уч-ся как этилен С2Н4
