
- •Модуль 1. Основные положения мкт.
- •Модуль 2. Количества вещества.
- •Модуль 3. Броуновское движение.
- •Модуль 4. Силы взаимодействия молекул.
- •Модуль 5. Газы, жидкости, твёрдые тела.
- •Модуль 6. Основное уравнение мкт.
- •Модуль 7. Тепловое равновесие. Температура.
- •Модуль 8. Газы в состоянии теплового равновесия.
- •Модуль 9. Скорости и молекул газов.
Модуль 7. Тепловое равновесие. Температура.
Что такое термодинамическая система?
Термодинамическая система — это некая физическая система, состоящая из большого количества частиц, способная обмениваться с окружающей средой энергией и веществом. Также обычно полагается, что такая система подчиняется статистическим закономерностям.
Величины, характеризующие состояние макроскопических тех без учёта молекулярного строения тел-макроскопические параметры: объём давление температуры.
Тепловым равновесием называют такое состояние, при котором все макроскопические параметры столь угодно долго остаются не именными.
При измерение температуры тела термометр приходит в тепловое равновесие с телом человека.
Температурой
Температура - характеризует состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии имеют одну и ту же температуры. Температура – мера средней кинетической энергии и молекул: чем выше температура, тем быстрее движутся молекулы и тем больше их кинетическая энергия.
При увеличении температуры объём жидкостей и газов увеличиваются
Жидкостный термометр-прибор для измерения температуры (См. Температура), принцип действия которого основан на тепловом расширении (См. Тепловое расширение) жидкости. Т. ж. относится к Термометрам непосредственного отсчёта.
Широко применяется в технике и лабораторной практике для измерения температур в диапазоне от –200 до 750 °С. Т. ж. представляет собой прозрачный стеклянный (редко кварцевый) резервуар с припаянным к нему капилляром (из того же материала). Шкала в °С наносится непосредственно на толстостенный капилляр (так называемый палочный Т. ж.) или на пластинку, жестко соединённую с ним (Т. ж. с наружной шкалой, рис., а). Т. ж. с вложенной шкалой (рис., б) имеет внешний стеклянный (кварцевый) чехол. Термометрическая жидкость заполняет весь резервуар и часть капилляра. В зависимости от диапазона измерений Т. ж. заполняют пентаном (от -200 до 20 °С), этиловым спиртом (от -80 до 70 °С), керосином (от -20 до 300 °С), ртутью (от -35 до 750 °С) и др.
Газовый термометр- прибор для измерения температуры, действие которого основано на зависимости давления или объёма идеального газа от температуры. Чаще всего применяют Г. т. постоянного объёма (рис.), который представляет собой заполненный газом баллон 1 неизменного объёма, соединённый тонкой трубкой 2 с устройством 3 для измерения давления. В таком Г. т. изменение температуры газа в баллоне пропорционально изменению давления. Г. т. измеряют температуры в интервале от 2К до 1300 К.
Модуль 8. Газы в состоянии теплового равновесия.
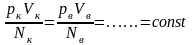
 ,
k-постоянная
Больцмана связывает температуру
,
k-постоянная
Больцмана связывает температуру
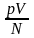 в Дж, с температурой T
в Кельвинах.
в Дж, с температурой T
в Кельвинах.
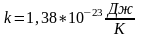
Предельную температуру, при которой давление идеального газа превращается в нуль при фиксированном объёме или объём идеального газа стремиться нулю, при неизменном давлении называют абсолютным нулём температуры. Это самое низкая температура, её еще никто не наблюдал и не получал.
Давление равно 0.
Шкала Цельсия: за нуль температуры он принял температуру плавления льда (температуры отвердевания воды) при нормальном атмосферном давлении. 100 градусов – температур кипении воды, при нормальном атмосферном давлении.
По школе Цельсия существует, как положительные, так и отрицательны температуры.
Абсолютная шкала температур, шкала Кельвина: нулевая температура соответствует абсолютному нулю. По этой шкале существуют только положительные температуры. Один градус Цельсия равен одному Кельвину.
Связь
школы Кельвина со шкалой Цельсии.
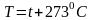

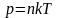 ,
из этой формулы вытекает, что при
одинаковых давлениях и температурах
концентрация молекул у всех газов одна
и та же.
,
из этой формулы вытекает, что при
одинаковых давлениях и температурах
концентрация молекул у всех газов одна
и та же.
Нормальные условия: T= 273 K ( t=0 C ), p=100000Па
