
- •Модуль 1. Основные положения мкт.
- •Модуль 2. Количества вещества.
- •Модуль 3. Броуновское движение.
- •Модуль 4. Силы взаимодействия молекул.
- •Модуль 5. Газы, жидкости, твёрдые тела.
- •Модуль 6. Основное уравнение мкт.
- •Модуль 7. Тепловое равновесие. Температура.
- •Модуль 8. Газы в состоянии теплового равновесия.
- •Модуль 9. Скорости и молекул газов.
Модуль 5. Газы, жидкости, твёрдые тела.
Перечислите агрегатные состояния вещества. Попытайтесь написать соотношение между кинетической и потенциальной энергии для газообразного, жидкого и твердого состояния вещества.
Твёрдое, жидкое, газообразные.
Опишите характер движения молекул в газах, жидкостях и твердых телах.
Газы: частица движутся свободно между столкновениями друг с другом.
Жидкости: частицы колеблются около положения равновесия, сталкиваюсь с соседними молекулами. Время от времени она совершает прыжок на другое место.
Твёрдые тела: частицы колеблются около определенных положений равновесия. Иногда частицы меняют положения равновесия, но это происходит крайне редко.
Каков характер упаковки частиц у газов, жидкостей и твердых тел?
Твёрдые тела и жидкости упаковка плотная: расстояния между центрами соседних частиц приблизительно равно диаметру самих частиц. В газах: расстояние между соседними частицами во много раз больше диаметров частиц.
Каково среднее расстояние между молекулами у газов, жидкостей и твердых тел?
Среднее расстояние между молекулами а) газов: намного больше размеров самих молекул; б) жидкостей: равно диаметру молекул; в) твердых тел: равно диаметру молекул.
Перечислите основные свойства газов, жидкостей и твердых тел.
а) Газы: занимают весь предоставленный объём, не имеют форму; б) жидкостей: текучи, сохраняют объём, принимают форму сосуда; в) твёрдые тела: сохраняют объём и форму.
Что называют идеальным газом в МКТ?
Идеальный газ-это модель сильно разряжённых реальных газов, это газ частицы которого только движутся и не взаимодействуют электромагнитными силами друг с другом. Частицы этого газа представляются в виде упругих шариков.
Назовите условия, при которых газ можно считать идеальным?
Плотность газа очень мала, то есть он сильно разряжён: промежутки между молекулами настолько велики, что они не притягиваются и не отталкиваются электромагнитными силами.
Модуль 6. Основное уравнение мкт.
Каков механизм возникновения давления газа с точки зрения МКТ?
Газы давят на поверхности тел и стенки сосудов за счёт столкновений молекул этими поверхностями.
Какую скорость движения молекул называют средней квадратичной?
Средняя квадратичная скорость молекул — среднее квадратическое значение модулей скоростей всех молекул рассматриваемого количества газа.
Что называют концентрацией молекул? Какая формула выражает смысл этого понятия?
Концентрация
показывает, какое количество молекул
содержится в
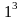 метр.
метр.
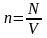
Запишите и объясните физический смысл основного уравнения МКТ?
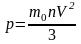 ,
Эта формула связывает макроскопическую
величину-давление, которая может быть
измерена манометром, - с микроскопическими
величинами, характеризующими молекулы,
и является ка бы мостом между двумя
мирами: макроскопическим и микроскопическим.
,
Эта формула связывает макроскопическую
величину-давление, которая может быть
измерена манометром, - с микроскопическими
величинами, характеризующими молекулы,
и является ка бы мостом между двумя
мирами: макроскопическим и микроскопическим.
Получите формулу, связывающую давление идеального газа и среднюю кинетическую энергию движения молекулы?

Как записываются основное уравнение МКТ через средний квадрат скорости молекул газа и его плотность?
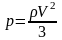
Какими приборами измеряется давление газа?
Манометр.
