- •2. Які основні характеристики і параметри хімічних сенсорів?
- •3. Дайте означення понять "адсорбція", "адсорбат", "адсорбент", “ступінь покриття поверхні”. Яка різниця між фізичною та хімічною адсорбцією? Як їх розрізнити експерименально?
- •4. Моделі адсорбції. Рівняння Гібса та ізотерми адсорбції Ленгмюра. Порівняйте висновки з теорії адсорбції Брунауера-Еммета-Теллера та Ленгмюра.
- •5. Опишіть можливі процеси адсорбції молекул води на поверхню твердого тіла. За яких умов виникає капілярна конденсація?
- •6. Що таке каталізатори і як вони працюють? Поясніть енергетичну діаграму для каталітичних реакцій на прикладі адсорбції н2 в системі Pd–SiO2.
- •7. Мультисенсори. Дайте приклад алгоритму математичної обробки матриці хімічних сенсорів за "методикою розпізнавання образів" та «головних компонент».
- •8. Поясніть зонну модель поверхні SnO2. Як відбувається обмін зарядами між твердим тілом і донорними/акцепторними молекулами на прикладі молекул со, н2, о2?
- •9. Виведіть формулу для розрахунку концентрації адсорбованих молекул кисню на поверхні метал-оксиду.
- •10. Виведіть формулу для розрахунку концентрації ко-адсорбованих на поверхні метал-оксиду молекул кисню та редокс-газу
- •12. Сенсори вологості на метал-оксидах. Наведіть еквівалентну електричну схему для контакту гранула–гранула–електрод для адсорбції води. Сенсорний метод контролю процесів горіння.
- •13. Поясніть принцип дії λ-сенсорів резитивного та потенціометричного типів.
- •14. Принцип дії польового транзистора з інверсним шаром. Основні характеристики приладу.
- •15. Принцип дії сенсору GasFet сенсора на водень. Модель чутливості до водню для Pd затворів. Як розрахувати парціальний тиск водню? Як впливає на чутливість до водню атмосферний кисень?
- •16. Параметри GasFet сенсорів на водень. Сенсори інших газів на основі польового транзистора. Модель чутливості до аміаку мон-структури. Польовий транзистор з підвішеною мембраною.
- •17. РН метр на isfet структурі. Як визначити значення рН розчину?
- •18. Сенсори водню на основі бар’єрів Шоткі. Зміною яких параметрів бар’єру визначається чутливість структури до адсорбції?
- •19.Потенціометричний сенсор зі світловою адресацією ((laPs). Навести принцип роботи та приклад характеристики фотоструму від прикладеної напруги в газовій атмосфері.
- •Принцип роботи сенсору електроліт-ізолятор-напівпровідник (еіs). Як підняти чутливість цього сенсору?
- •Газові сенсори на основі методу вібруючого електроду (метод зонду Кельвіна).
- •22. Назвіть та поясніть методи отримання квантових структур кремнію за високими технологіями, хімічного та електрохімічного травлення.
- •26. Поясніть, які механізми описують транспорт носіїв заряду в макропоруватому та нанопоруватого кремнії. Вплив адсорбції на електричні властивості поруватого Si.
- •28. Сенсор на польовому транзисторі із використанням пористого кремнію. Поясніть принцип дії. Який принцип дії газового сенсора з пористим кремнієм на основі кмон процесу?
- •29. Основні властивості полімерів. Π-спряжені зв’язки. Використання полімерів для сенсорів провідності.
- •31 Калориметричні сенсори на кремнієвих термопарах та транзисторах
- •32. Калориметричний сенсор з плаваючою мембраною: еквівалентна електрична схема та параметри. Термічний сенсор вологості.
- •33. Ефект зникаючого поля в оптичному волокні. Сенсори на оптичному волокні. Оптод.
- •Як використовується ефект поверхнево-підсиленого комбінаційного розсіяння світла для газових сенсорів.
- •35 Дайте означення біосенсору. Сенсори на основі біоспорідненості та метаболізму. Перші біосенсори на глюкозу та сечовину.
- •Cхема біосенсора
- •38.Еванесцентні хвилі. Хвилі, що локалізовані на межі розподілу «зовнішнє середовище-метал», «зовнішнє середовище-напівпровідник».
- •40.Закон дисперсії поверхневого плазмон-поляритону.
- •4 1.Параметри, що впливають на збудження та розповсюдження ппп.
- •42. Ефект поверхневого плазмон поляритонного резонансу пппр.
- •43. Схема вимірювання поверхневого плазмон поляритонного резонансу пппр.
- •44. Принципи побудови датчиків на основі поверхневого плазмон поляритонного резонансу пппр.
- •45. Методи, що використовуються для покращення умов збудження та розповсюдження ппп.
- •46. Методи, що використовуються для підвищення чутливості пппр датчика біомолекул.
- •47. Методи, що використовуються для підвищення селективності пппр датчика біомолекул.
- •48. Коефіцієнт відбиття від багатошарової системи. Методи обробки даних пппр вимірювань.
15. Принцип дії сенсору GasFet сенсора на водень. Модель чутливості до водню для Pd затворів. Як розрахувати парціальний тиск водню? Як впливає на чутливість до водню атмосферний кисень?
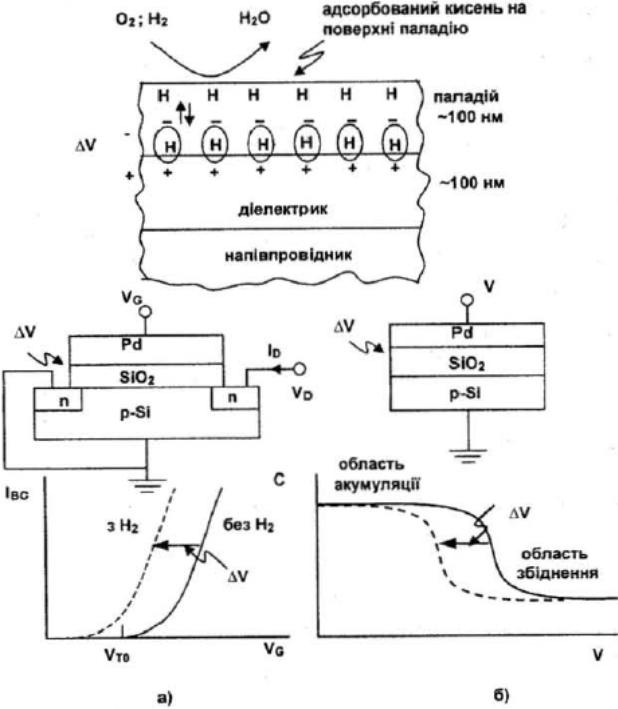
Принцип дії сенсору GasFET сенсора на водень. У структурі, яка має назву GasFET (газовий польовий транзистор), як затворний метал використовують плівку Pd або інших перехідних металів, які є каталізаторами до водню. Молекули водню з атмосфери адсорбуються на поверхні каталізатора й дисоціюють на атоми водню, частина атомів водню дифундує крізь шар Pd і адсорбується в інтерфейсі Pd-оксид (або інший діелектрик). Кількість
адсорбованих атомів водню в інтерфейсі визначається концентрацією молекул водню в атмосфері та хімічними реакціями на поверхні. В інтерфейсі адсорбовані атоми водню поляризуються і створюють дипольний шар, який змінює потенціал затвора на величину ΔV, що зменшує роботу виходу металу в інтерфейсі.
|
Рис. 3.2. МОН-структура Pd–SiO2–p-Si за присутності молекул водню та кисню (нагорі): а) схема вимірювань і крива струму витік – стік залежно від напруги на затворі транзистора; б) МОН-ємність і відповідні ВФХ. Стрілка показує напрямок зсуву характеристик при адсорбції водню на поверхні паладію |
VT=VTO-ΔV (3.7) де VTO – порогова напруга виникнення інверсного шару без присутності водню. Аналогічно, ємність МОН-структури також зсувається вздовж осі напруг на величину ΔV , оскільки напруга плоских зон VFB залежить від роботи виходу металу й входить до величини VT (вирази (3.5), (3.6)).
(3.5) де ψp – потенціал у р-області, Vps – напруга зворотного зміщення на підкладці, а величина напруги плоских зон VFB дорівнює:
(3.6)
Величина ΔV дорівнює:
 (3.8)
(3.8)
де ni – кількість атомів водню в області інтерфейсу (на одиниці поверхні, см–2), μ – дипольний момент адсорбованих атомів водню в інтерфейсі, ε0 – діелектрична проникність вакууму. Зростання ΔV відповідає зменшенню роботи виходу металу.
Для того, щоб описати фізико-хімічні причини виникнення зміни електричних характеристик МОН-структури необхідно розглянути три різних процеси: 1) поверхневі реакції, які ведуть до адсорбції атомів водню на зовнішній поверхні металу; 2) транспорт атомів водню крізь плівку каталітичного металу; 3) утворення диполів в інтерфейсі метал–діелектрик чи метал–напівпровідник (у випадку контакту типу Шотткі).
Модель чутливості до водню для Pd затворів.
Основні припущення моделі такі (рис. 3.3):
1) молекули водню адсорбуються та дисоціюють на поверхні каталізатора. Концентрація адсорбованих атомів на поверхні пропорційна парціальному тиску водню та кількості вільних вузлів адсорбції;
|
Рис. 3.3. Хімічні реакції при адсорбції водню та кисню на МОН-структурі з паладієм |
2) водень десорбується з поверхні металу за рахунок рекомбінації та утворення молекул Н2 чи за рахунок хімічної реакції з киснем і утворенням молекул води. Тобто механізми 1 та 2 описуються такими реакціями:
дисоціація молекул водню H22Ha (зі швидкістю c1);
рекомбінація адсорбованих атомів водню 2НаН2 (зі швидкістю d1);
дисоціація молекул кисню О22Оа;
рекомбінація адсорбованих атомів кисню 2ОаО2;
утворення та десорбція молекул води 4На+О22Н2О.
Залежно від температури реакції утворення води та гідроксилів можуть відбуватися також за іншими каналами (рис. 3.3), а саме:
з утворенням адсорбованих OH -груп 2На+О22ОНа, (зі швидкістю c2 ) На+ОаОНа;
дисоціації ОН-груп ОНаОа+На;
утворенням молекул води ОНа+НаН2О.
При балансі вказаних реакцій встановлюється рівноважній стан, який залежить від співвідношень парціальних тисків водню та кисню.
3) атоми водню дифундують крізь метал і адсорбуються в інтерфейсі метал–діелектрик. Завдяки дуже високій швидкості дифузії (час дифузії крізь 200нм шар паладію дорівнює 10мкс при 150 0С та 0,15мс при кімнатній температурі) завжди існує рівновага між кількістю водневих атомів на двох поверхнях: На«Нi;
4) атоми водню, які адсорбуються в інтерфейсі метал–діелектрик, стають поляризованими, що веде до зсуву напруги ΔV, який пропорційний кількості адсорбованих водневих атомів в інтерфейсі (3.8).
Як розрахувати парціальний тиск водню? Як впливає на чутливість до водню атмосферний кисень? Ці реакції можуть бути виражені простими кінетичними рівняннями для коефіцієнта покриття поверхні металу адсорбованими атомами водню θa (відношення кількості адсорбованого водню на загальну кількість вузлів адсорбції на поверхні каталізатора) з урахуванням лише найбільш вірогідних реакцій. Тоді з припущень 1 та 2 випливає, що адсорбція атомів кисню блокує хімічні реакції на поверхні. Якщо формування молекул ОНа іде за рахунок адсорбованих атомів водню і молекулярного кисню, то емпірично можна встановити, що:
 (3.9)
(3.9)
де θOH – покриття ОН-групами поверхні каталізатора, PH2 та PO2 – парціальний тиск Н2 і О2, відповідно, θa пропорційне квадратному кореню з парціального тиску водню за умови θa << 1 - θOH і PO2 = const.
Якщо ОНа створюються за рахунок адсорбованих кисню та водню і процес дисоціації ОНа швидкий, то адсорбовані кисневі атоми блокуватимуть дисоціацію молекул водню і співвідношення (3.9) буде іншим:
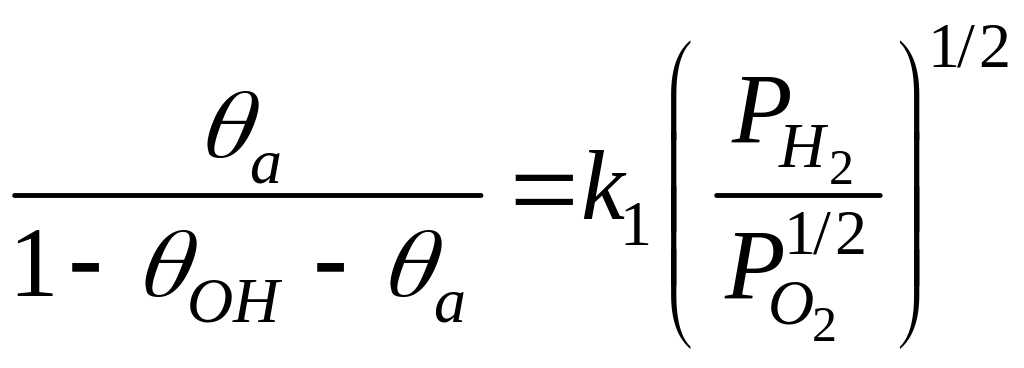 (3.10)
(3.10)
де нехтуємо рекомбінацією двох атомів водню в молекулу водню, оскільки швидкість утворення молекул води значно вища за швидкість рекомбінації при концентрації кисню порядку відсотків. Якщо атмосфера інертна, то спонтанна рекомбінація атомів водню вже істотна й тоді:
 (3.11)
(3.11)
Ці результати можуть бути зрозумілими на підставі аналізу простих кінетичних рівнянь для θa. Рівняння (3.9) можна отримати з кінетичного рівняння:
d( a)011H(2O1H)2a2O222aaiiacPcPFF
![]() (3.12)
(3.12)
де θ0 – це покриття атомами кисню, яке блокує дисоціацію водню на поверхні, Fai та Fia – це потоки атомів водню з поверхні в діелектричний шар, і навпаки (рис. 3.3), які однакові за рівноважних умов. Введемо величину ступеня покриття воднем інтерфейсу метал–діелектрик θi. Тоді для цих потоків можна записати:
![]() (3.13)
(3.13)
де c, d – відповідно, швидкості дифузії HaHi та HiHa. За рівноважних умов Fai=Fia. Звідси
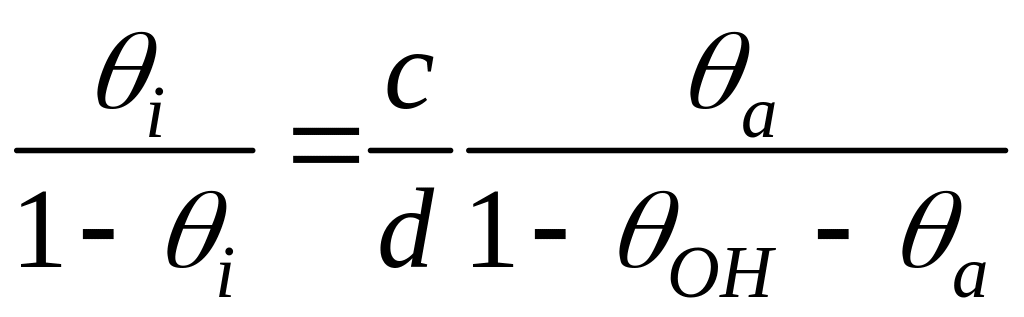 (3.14)
(3.14)
Якщо вузли адсорбції на поверхні та в інтерфейсі мають одну природу й однакову теплоту адсорбції, то c/d=1. Ця умова виконується для паладієвої МОН-структури при роботі за атмосферних умов. Таким чином, концентрація атомів водню в інтерфейсі визначається концентрацією молекул водню у вимірюваній атмосфері та хімічними реакціями на поверхні каталізатора. В інтерфейсі при адсорбції атомів водню виникає дипольний шар і додаткове падіння напруги, яке змінює роботу виходу металу в інтерфейсі. Якщо припустити, що
ΔV=ΔVmaxθi (3.15)
то можна отримати рівняння для залежності зсуву I-V та C-V характеристик від парціального тиску водню й кисню:
 (3.16)
(3.16)
або від парціального тиску водню в інертній атмосфері:
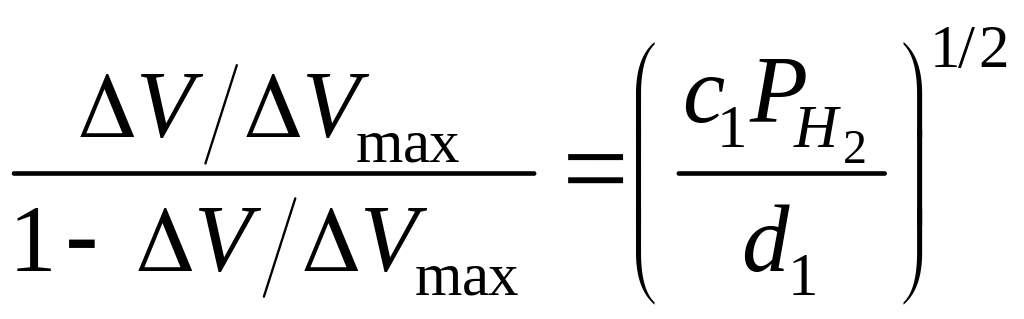 (3.17)
(3.17)
де K – постійна, а функція f (PO2), згідно з рівняннями (3.9) та (3.10) дорівнює PO2 або PO21/2. Тобто напруга зсуву залежить як корінь квадратний від парціального тиску водню