
- •Г. М. Давидан, а. Г. Нелин, л. Н. Олейник, е. Д. Скутин общая химическая технология
- •Предисловие
- •Глава 1 общие понятия о химическом производстве
- •1.1. Химическая технология как наука
- •М акрокинетика
- •1.2. Связь химической технологии с другими науками
- •Химическая технология
- •1.3. История отечественной химической технологии
- •Контрольные вопросы
- •Глава 2 компоненты химического производства
- •2.1. Сырье в химическом производстве
- •Классификация химического сырья
- •2.2. Энергия в химической технологии
- •2.4. Воздух в химической технологии
- •Контрольные вопросы
- •Глава 3 критерии оценки эффективности химического производства
- •3.1. Технико-экономические показатели (тэп)
- •3.2. Структура экономики химического производства
- •Материальный и энергетический баланс химического производства
- •Контрольные вопросы
- •Глава 4 системный подход в изучении химико-технологического процесса
- •4.1. Общие понятия и определения
- •4.2. Химико-технологическая система как объект моделирования
- •4.3. Операторы
- •4.4. Матричное представление моделей
- •4.5. Подсистемы хтс
- •4.6. Связи
- •4.7. Классификация технологических схем
- •4.8. Системный подход к разработке технологии производства
- •4.9. Оптимизация производства
- •Контрольные вопросы
- •Глава 5 общие закономерности химических процессов
- •5.1. Понятие о химическом процессе
- •5.2. Классификация химических реакций
- •5.3. Интенсификация гомогенных процессов
- •5.4. Интенсификация гетерогенных процессов
- •5.5. Интенсификация процессов, основанных на необратимых реакциях
- •5.6. Интенсификация процессов, основанных на обратимых реакциях
- •Контрольные вопросы
- •Глава 6 гетерогенный катализ
- •6.1. Общие положения катализа
- •6.2. Процессы адсорбции и хемосорбции в гетерогенном катализе
- •6.3. Механизм гетерогенных каталитических процессов
- •6.4. Основные требования к гетерогенным катализаторам
- •6.5. Основные структурные параметры гетерогенных катализаторов
- •6.6. Технологические свойства гетерогенных катализаторов
- •6.7. Классификация гетерогенных катализаторов
- •6.8. Состав катализаторов
- •6.9. Приготовление катализаторов
- •Контрольные вопросы
- •Глава 7 гомогенный катализ
- •7.1. Кислотный (основной) катализ
- •7.2. Металлокомплексный катализ
- •7.3. Ферментативный катализ
- •Контрольные вопросы
- •Глава 8 химические реакторы
- •8.1. Принципы классификации химических реакторов
- •8.2. Принципы проектирования химических реакторов
- •8.3. Химические реакторы с идеальной структурой потока в изотермическом режиме
- •8.3.3. Примеры аналитического решения математической модели (8.22) и (8.23) для частных случаев
- •8.4. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения
- •8.5. Конструкции реакторов
- •Контрольные вопросы
- •Глава 9 производство серной кислоты
- •9.1. Способы производства серной кислоты
- •9.2. Сырье процесса
- •9.3. Промышленные процессы получения серной кислоты
- •9.4. Пути совершенствования сернокислотного производства
- •Контрольные вопросы
- •Глава 10 производство аммиака
- •10.1. Проблема связанного азота
- •10.2. Получение азота и водорода для синтеза аммиака
- •10.3. Синтез аммиака
- •Контрольные вопросы
- •Глава 11 переработка нефти
- •11.1. Общие сведения о нефти
- •11.2. Классификация нефтей
- •11.3. Состав нефти
- •11.4. Нефтепродукты
- •11.5. Подготовка нефти на нефтепромыслах
- •11.6. Первичная переработка нефти
- •11.7. Пиролиз
- •11.8. Коксование
- •11.9. Каталитический крекинг
- •11.10. Каталитический риформинг
- •11.11. Гидроочистка
- •11.12. Производство нефтяных масел
- •Контрольные вопросы
- •Глава 12 переработка каменного угля
- •12.1. Показатели качества каменных углей
- •12.2. Классификация углей
- •12.3. Коксование каменных углей
- •Коксование
- •Тушение
- •Разгонка
- •12.4. Состав прямого коксового газа и его разделение
- •12.5. Переработка сырого бензола
- •12.6. Переработка каменноугольной смолы
- •12.7. Газификация твердого топлива. Процесс Фишера – Тропша
- •Контрольные вопросы
- •Глава 13 производство стирола
- •13.1. Получение этилбензола
- •13.2. Производство стирола дегидрированием этилбензола
- •13.3. Технологическая схема производства стирола дегидрированием этилбензола
- •Контрольные вопросы
- •Глава 14 производство этанола
- •Контрольные вопросы
- •Библиографический список
- •Содержание
- •Глава 12. Переработка каменного угля 231
- •Глава 13. Производство стирола 246
- •Глава 14. Производство этанола 252
12.7. Газификация твердого топлива. Процесс Фишера – Тропша
Рассматриваемые здесь процессы связаны с получением искусственного жидкого топлива.
Гидрирование твердого топлива представляет собой деструктивный каталитический процесс, проводимый при 400–500 оС под давлением водорода 20–70 МПа. В этих условиях в органической массе топлива протекают следующие реакции:
– деструкции и деполимеризации высокомолекулярных структур угля
( С)п + пН2 СпН2п; (12.7)
– гидрирования образовавшихся алкенов
СпН2п + Н2 СпН2п +2; (12.8)
– деструкции высших алканов с последующим гидрированием образовавшихся алкенов и образованием алканов с меньшей молекулярной массой
СпН2п +2 СтН2т +2 + СрН2р; (12.9)
С рН2р + Н2 СрН2р + 2 ; (12.10)
– гидрирования конденсированных углеводородных систем с последующим разрывом цикла и деалкилированием
 С2Н5
С2Н5
2Н2 Н2 + 2С2Н4. (12.11)
С2Н5
– раскрытия пятичленных
циклов с образованием изоалканов
раскрытия пятичленных
циклов с образованием изоалканов
R + Н2 СН3 – СН – СН2 – СН2 – СН3 (12.12)
R
и другие реакции.
Процесс гидрирования твердого топлива является каталитическим. В качестве катализаторов используют контактные массы на основе соединений молибдена, никеля или железа, активированные, например, оксидами кальция и бария. В качестве носителя применяют оксид алюминия. Пример такой композиции имеет состав МоО3 + NiS + CaO + Al2O3.
Впервые гидрогенизацией угля получил жидкое топливо (бензин) в 1911 г. немецкий химик Ф. Бергиус.
Однако промышленная реализация получения моторных топлив из угля базировалась на другом способе газификации угля – его взаимодействием с водяным паром и получением синтез-газа:
С + Н2О СО + Н2 (12.13)
Это эндотермическая реакция, которая существенно сдвинута вправо при температуре 900–1000 оС. Необходимую температуру можно получить частичным сжиганием части угля по реакции
С + 0,5О2 СО. (12.14)
По реакции (12.13) также получают оксид углерода (II).
История использования синтез-газа для производства моторного топлива восходит к 1926 г., когда немецкие ученые Ф. Фишер и Г. Тропш опубликовали работу «О прямом синтезе нефтяных углеводородов при обыкновенном давлении», в которой сообщалось, что при восстановлении водородом монооксида углерода при атмосферном давлении в присутствии различных катализаторов (железо – оксид цинка или кобальт – оксид хрома) при 270 °С получаются жидкие и даже твердые гомологи метана.
Так возник знаменитый синтез углеводородов из монооксида углерода и водорода, называемый с тех пор синтезом Фишера–Тропша (ФТ). Смесь CO и H2 в различных соотношениях, называемая синтез-газом, легко может быть получена как из угля, так и из любого другого углеродсодержащего сырья.
Процесс Фишера – Тропша описывается следующими уравнениями:
пСО + (2п + 1) Н2 СпН2п +2 + пН2О; (12.15)
2пСО + (п + 1) Н2 СпН2п +2 + пСО2. (12.16)
В направлении (12.15) синтез идет на никельсодержащих (например, Ni-Mn-Al2O3 на кизельгуре или сплав Ni-Si-Mn) либо кобальтовых катализаторах (например, Co-ThO2 или Co-ThO2-MgO на кизельгуре) при 175–215 оC, 0,1–1,5 МПа, объемном соотношении CO/H2 1/1–1/2. Выход углеводородов в этом случае составляет 100–180 мл на 1 м3 исходной газовой смеси. Пример фракционного состава для Со-катализатора: фракция с Ткип <150 оC (бензин) – 20–24 %; 150 – 200 оС – 12–15 %; 250–300 оC – 25 %; парафины 34–42 %. В основном все фракции содержат алканы с нормальной цепью. При этом бензиновая фракция содержит от 8 до 40 % олефинов.
На катализаторах на основе железа (например, Fe-ZnO либо Fe-Cu-Mn на доломите или кизельгуре) при 220–250 оC, 0,5–1 МПа и объемном соотношении CO/H2 2/1 – 1/1 преобладает процесс (12.16). Выход углеводородов до 160 мл на 1 м3 газовой смеси (в т.ч. бензина и масел около 110 мл). В числе жидких продуктов содержатся значительные количества (до 60 %) олефинов.
Парафины преимущественно (60–70 %) образуются на рутениевых катализаторах при 180–200 оC и 10–30 МПа; на оксидах Cr, Mo, Th с добавками K2CO3 при 475–500 оC, 3 МПа и соотношении CO/H2 1/1 – значительные количества аренов. На оксидах Zn, Al или Th при 420–450 оC, 30 МПа и соотношении CO/H2 1,2/1 основными продуктами являются изоалканы (главным образом изобутан и изопентан).
В качестве побочных продуктов образуются незначительные количества карбоновых кислот, спиртов, альдегидов.
Механизм синтеза Фишера–Тропша до конца не выяснен. Наиболее вероятно, что первой стадией является образование комплекса металла и СО, затем начинается синтез углеводородной цепи, например:
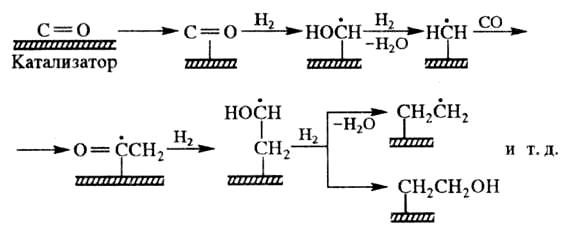
В росте цепи могут участвовать структурные единицы с одним, двумя и большим числом атомов С (образуются, например, в результате деструкции углеводородов с длинной цепью).
В присутствии Ce, Cr, Mn, Mo и некоторых других металлов и их оксидов при высоких давлениях и температурах (около 15 МПа, 400–450 оC) из СО и H2 образуются в основном кислородсодержащие соединения (около 10 % кислот, остальное – спирты, альдегиды, кетоны).
Первый промышленный реактор был пущен в Германии в 1935 г., использовался Co-Th осажденный катализатор. В 1930–40-е гг. на основе технологии Фишера–Тропша было налажено производство синтетического бензина (когазин-I, или синтин) с октановым числом 40–55, синтетической высококачественной дизельной фракции (когазин-II) с цетановым числом 75–100 и твёрдого парафина. Сырьем для процесса служил уголь, из которого газификацией получали синтез-газ, а из него – углеводороды. К 1945 г в мире имелось 15 заводов синтеза Фишера – Тропша (в Германии, США, Китае и Японии) общей мощностью около 1 млн.т углеводородов в год. Они выпускали в основном синтетические моторные топлива и смазочные масла.
В годы после Второй мировой войны синтезу ФТ уделяли большое внимание во всём мире, поскольку считалось, что запасы нефти подходят к концу, и надо искать ей замену. В 1950 г. был пущен завод в г. Браунсвилле (шт. Техас, США) на 360 тыс. т/г. В 1955 г. южноафриканская компания Sasol построила собственное производство, существующее и развивающееся до сих пор.
В г. Новочеркасске с 1952 г. работала установка мощностью около 50 тыс. т/г на вывезенном из Германии оборудовании. Сырьем служил сначала уголь донецкого бассейна, а затем природный газ. Немецкий Co-Th катализатор был со временем заменён на оригинальный: Co-Zr. На заводе была установлена колонна точной ректификации, так что в ассортимент продукции завода входили индивидуальные углеводороды высокой чистоты, в том числе α-олефины с нечетным углеродным номером. Установка работала на Новочеркасском заводе синтетических продуктов вплоть до 1990-х г. и была остановлена по экономическим причинам.
Все эти предприятия в значительной степени заимствовали опыт немецких химиков и инженеров, накопленный в 30–40-е годы.
Открытие обширных месторождений нефти в Аравии, Северном море, Нигерии, Аляске резко снизило интерес к синтезу Фишера – Тропша. Почти все существующие заводы были закрыты, единственное крупное производство сохранилось в ЮАР с годовой мощностью около 5 млн. т жидких продуктов.
Активность в этой области возобновилась к 1990 г. В 1990 г. компания Exxon запустила опытную установку на 8 тыс. т/г с Co-катализатором. В 1992 г. южноафриканская компания Mossgas построила завод мощностью 900 тыс. т/г. В отличие от технологии Sasol, в качестве сырья здесь использовался природный газ с шельфового месторождения. В 1993 г. компания Shell запустила завод в Бинтулу (Малайзия) мощностью 500 тыс. т/г, используя Co-Zr катализатор и оригинальную технологию «средних дистиллятов». Сырьем служит синтез-газ, получаемый парциальным окислением местного природного газа. В настоящее время Shell строит завод в Катаре по той же технологии, но на порядок большей мощности. Свои проекты в области синтеза Фишера–Тропша разной степени проработки имеют также компании Chevron, Conoco, BP, ENI, Statoil, Rentech, Syntroleum и др.
