
- •Г. М. Давидан, а. Г. Нелин, л. Н. Олейник, е. Д. Скутин общая химическая технология
- •Предисловие
- •Глава 1 общие понятия о химическом производстве
- •1.1. Химическая технология как наука
- •М акрокинетика
- •1.2. Связь химической технологии с другими науками
- •Химическая технология
- •1.3. История отечественной химической технологии
- •Контрольные вопросы
- •Глава 2 компоненты химического производства
- •2.1. Сырье в химическом производстве
- •Классификация химического сырья
- •2.2. Энергия в химической технологии
- •2.4. Воздух в химической технологии
- •Контрольные вопросы
- •Глава 3 критерии оценки эффективности химического производства
- •3.1. Технико-экономические показатели (тэп)
- •3.2. Структура экономики химического производства
- •Материальный и энергетический баланс химического производства
- •Контрольные вопросы
- •Глава 4 системный подход в изучении химико-технологического процесса
- •4.1. Общие понятия и определения
- •4.2. Химико-технологическая система как объект моделирования
- •4.3. Операторы
- •4.4. Матричное представление моделей
- •4.5. Подсистемы хтс
- •4.6. Связи
- •4.7. Классификация технологических схем
- •4.8. Системный подход к разработке технологии производства
- •4.9. Оптимизация производства
- •Контрольные вопросы
- •Глава 5 общие закономерности химических процессов
- •5.1. Понятие о химическом процессе
- •5.2. Классификация химических реакций
- •5.3. Интенсификация гомогенных процессов
- •5.4. Интенсификация гетерогенных процессов
- •5.5. Интенсификация процессов, основанных на необратимых реакциях
- •5.6. Интенсификация процессов, основанных на обратимых реакциях
- •Контрольные вопросы
- •Глава 6 гетерогенный катализ
- •6.1. Общие положения катализа
- •6.2. Процессы адсорбции и хемосорбции в гетерогенном катализе
- •6.3. Механизм гетерогенных каталитических процессов
- •6.4. Основные требования к гетерогенным катализаторам
- •6.5. Основные структурные параметры гетерогенных катализаторов
- •6.6. Технологические свойства гетерогенных катализаторов
- •6.7. Классификация гетерогенных катализаторов
- •6.8. Состав катализаторов
- •6.9. Приготовление катализаторов
- •Контрольные вопросы
- •Глава 7 гомогенный катализ
- •7.1. Кислотный (основной) катализ
- •7.2. Металлокомплексный катализ
- •7.3. Ферментативный катализ
- •Контрольные вопросы
- •Глава 8 химические реакторы
- •8.1. Принципы классификации химических реакторов
- •8.2. Принципы проектирования химических реакторов
- •8.3. Химические реакторы с идеальной структурой потока в изотермическом режиме
- •8.3.3. Примеры аналитического решения математической модели (8.22) и (8.23) для частных случаев
- •8.4. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения
- •8.5. Конструкции реакторов
- •Контрольные вопросы
- •Глава 9 производство серной кислоты
- •9.1. Способы производства серной кислоты
- •9.2. Сырье процесса
- •9.3. Промышленные процессы получения серной кислоты
- •9.4. Пути совершенствования сернокислотного производства
- •Контрольные вопросы
- •Глава 10 производство аммиака
- •10.1. Проблема связанного азота
- •10.2. Получение азота и водорода для синтеза аммиака
- •10.3. Синтез аммиака
- •Контрольные вопросы
- •Глава 11 переработка нефти
- •11.1. Общие сведения о нефти
- •11.2. Классификация нефтей
- •11.3. Состав нефти
- •11.4. Нефтепродукты
- •11.5. Подготовка нефти на нефтепромыслах
- •11.6. Первичная переработка нефти
- •11.7. Пиролиз
- •11.8. Коксование
- •11.9. Каталитический крекинг
- •11.10. Каталитический риформинг
- •11.11. Гидроочистка
- •11.12. Производство нефтяных масел
- •Контрольные вопросы
- •Глава 12 переработка каменного угля
- •12.1. Показатели качества каменных углей
- •12.2. Классификация углей
- •12.3. Коксование каменных углей
- •Коксование
- •Тушение
- •Разгонка
- •12.4. Состав прямого коксового газа и его разделение
- •12.5. Переработка сырого бензола
- •12.6. Переработка каменноугольной смолы
- •12.7. Газификация твердого топлива. Процесс Фишера – Тропша
- •Контрольные вопросы
- •Глава 13 производство стирола
- •13.1. Получение этилбензола
- •13.2. Производство стирола дегидрированием этилбензола
- •13.3. Технологическая схема производства стирола дегидрированием этилбензола
- •Контрольные вопросы
- •Глава 14 производство этанола
- •Контрольные вопросы
- •Библиографический список
- •Содержание
- •Глава 12. Переработка каменного угля 231
- •Глава 13. Производство стирола 246
- •Глава 14. Производство этанола 252
Контрольные вопросы
1. Объясните понятие «химико-технологический процесс».
2. Дайте определение понятию «технологический режим». Какие параметры его определяют?
3. Представьте классификацию реакций, определяющих основу ХТП.
4. Напишите уравнение закона действующих масс. Объясните с позиции этого закона влияние концентрации на приемы интенсификации гомогенных процессов.
5. Напишите уравнение Аррениуса. Объясните на основе этого уравнения влияние температуры и энергии активации на скорость химических процессов.
6. Объясните влияние давления на скорость гомогенных процессов. Какие давления по абсолютной величине применяют в химической технологии? Приведите примеры.
7. Приведите классификацию гетерогенных систем. Дайте примеры.
9. Назовите элементарные стадии гетерогенных процессов.
10. Дайте определение лимитирующей стадии процесса. В каких областях может протекать гетерогенная реакция?
11. От каких факторов зависит скорость гетерогенной реакции, протекающей в диффузионной области? Дайте соответствующее уравнение этой зависимости.
12. Что такое движущая сила процесса массопередачи? Как она влияет на скорость гетерогенных процессов? Как можно повысить градиент концентраций?
13. Дайте определение понятию «химическое равновесие». Как его можно нарушить? Принцип Ле-Шателье.
14. Напишите уравнение Гиббса. На его основе объясните принципиальную возможность протекания химической реакции и величину движущей силы процесса.
Глава 6 гетерогенный катализ
6.1. Общие положения катализа
Современные процессы основного неорганического синтеза, нефтепереработки, нефтехимии и органического синтеза в настоящее время без при-менения катализаторов невозможно представить. Около 90 % промышленных химико-технологических процессов ведут с применением катализаторов в качестве активаторов. Примерами неорганического синтеза являются тех-нологические процессы производства аммиака, азотной и серной кислот; нефтехимии и органического синтеза – процессы производства метанола, стирола, бутадиена, фенола и ацетона, ацетальдегида и др. В нефтепереработке – это процессы каталитическиого крекинга и риформинга, гидроочистки и гидрокрекинга, алкилирования изобутана и изомеризации парафино-вых углеводородов, производства оксигенатов и т.д.
Каталитические процессы имеют ряд важных преимуществ по сравнению с некаталитическими процессами. Кроме того, что применение катализаторов резко ускоряет скорости химических реакций, процессы с их использованием могут быть организованы как непрерывные, безотходные и менее энергоемкие, отличающиеся высокими технико-экономическими показателями и обеспечивающие более высокий выход целевых продуктов.
Применение катализаторов позволяет интенсифицировать химико-тех-нологические процессы, а в ряде случаев осуществлять процессы, которые на практике без катализаторов не могут быть реализованы. Особо значимо использование катализаторов при обратимых экзотермических процессах, что позволяет существенно снижать температуру процесса и добиваться приемлемой степени превращения сырья.
Определение понятию катализа можно сформулировать следующим образом. Катализ – это явление, состоящее в том, что присутствие в системе какого-либо вещества вызывает или ускоряет (реже замедляет) протекание некоторой химической реакции, либо открывает новый путь для химического процесса. Само это вещество в конце реакции оказывается неизменным (в химическом смысле, так как физическое состояние катализатора может достаточно сильно отличаться от исходного). С точки зрения формальной химической кинетики это означает, что у всех каталитических реакций имеется циклический каталитический маршрут. Отметим, что катализатор не сдвигает химическое равновесие, а только изменяет скорость протекания химического процесса. Это означает, что катализатор одинаково влияет на протекание и прямой и обратной реакций. Каждый катализатор способен катализировать только вполне определенные реакции или классы реакций.
Специфичность действия катализатора может различаться весьма сильно: от уникальности в случае некоторых ферментов до катализа многих классов реакций. Общий принцип действия катализатора состоит в снижении энергии активации. Схематическая зависимость энергии реагирующей системы от координаты реакции (для реакции без катализатора – сплошная линия и реакции с участием катализатора – пунктирная) приведена на рисунке 6.1.
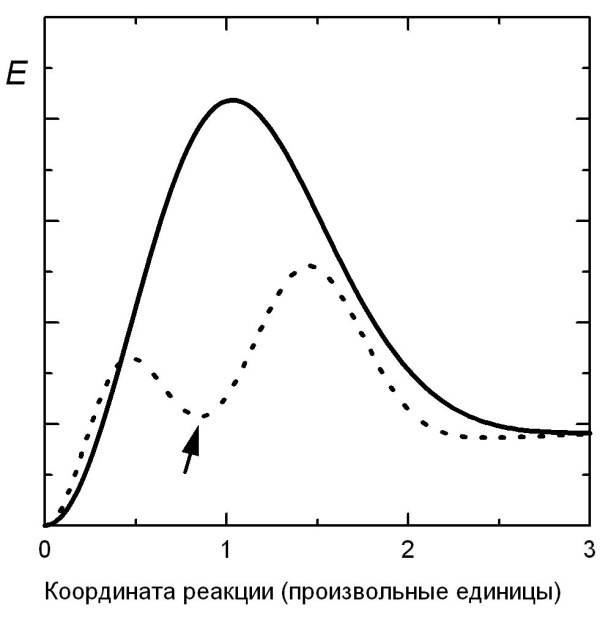
Рис. 6.1. Зависимость энергии реагирующей системы от координаты реакции
Из рисунка 6.1 видна главная особенность действия катализатора – образование промежуточного продукта (комплекса субстрат-катализатор, показанно стрелкой), что приводит к разбиению исходной элементарной реакции, по крайней мере, на две стадии, каждая из которых имеет энергию активации, меньшую энергии активации исходной реакции.
В зависимости от места протекания реакции катализ разбивают на гомогенный и гетерогенный. Если реагенты и катализатор находятся в одной жидкой или газовой фазе, то это гомогенный катализ, если в разных фазах (газ – твердое тело или жидкость – твердое тело), то это гетерогенный катализ. Существует и гомогенно-гетерогенный катализ, когда начавшаяся на гетерогенном катализаторе реакция продолжается затем в объеме другой фазы.
Гетерогенный катализ наиболее распространен в химической технологии. Он отличается рядом достоинств, например, простотой разделения катализатора и продуктов процесса, высокой термостойкостью и сравнительной легкостью регенерации собственно катализатора.
Каталитические гетерогенные реакции сопровождаются рядом явлений, связанных со свойствами твердых тел, неоднородных по химическому и фазовому составу. Важнейшую роль играют нарушения структуры (дефекты) кристаллической решетки катализаторов. Эти нарушения обусловливают энергетическую неоднородность поверхностных атомов и обеспечивают опре-деленную сорбционную способность поверхности катализатора. В целом эффективность применения катализаторов определяется комплексом их химических и физических свойств.
