
- •1. Какое положение занимают коллоидные системы в общей системе дисперсных систем?
- •2. Что такое степень дисперсности? Как классифицируются дисперсные системы по размеру частиц дисперсной фазы?
- •3. Как классифицируются дисперсные системы по агрегатному состоянию дисперсной фазы и дисперсной среды? Приведите примеры медико-биологического профиля.
- •4. Объясните. Почему коллоидно-дисперсные и грубодисперсные системы являются термодинамически неустойчивыми
- •5. Какие условия необходимо соблюдать для получения устойчивых эмульсий? Каково биологическое значение эмульсий?
- •6. Охарактеризуйте молекулярно-кинетические свойства золей и сравните их с истинными растворами
- •7. Объясните причину возникновения конуса Тиндаля при падении луча света на золь
- •8. Объясните, почему золи рассеивают преимущественно коротковолновое излучение
- •9. Какими способами можно отличить золь от грубодисперсной системы? На каких свойствах основаны эти способы?
- •10. Приведите примеры практического использования электрофореза. Какое значение имеет для характеристики коллоидно-дисперсных систем дзета-потенциал? Каким образом его можно определить
- •11. Что называют коагуляцией? Каковы внешние признаки коагуляции? Укажите возможные продукты коагуляции золей
- •12. Что такое электрофорез и электроосмос? Как объясняются эти явления?
- •13. Почему при электродиализе используется только постоянный электрический ток?
- •14. Каково строение мицелл лиофобных золей? Покажите это на примере мицеллы золя сульфида сурьмы (го)?
- •15. Какой коллоидный агрегат называется мицеллой? Что такое гранула?
- •16. Напишите формулу мицеллы сульфата бария, полученного сливанием одинакового объема сильно разбавленного раствора хлорида бария и менее разбавленного раствора серной кислоты
- •17. Напишите формулу мицеллы золя бромида серебра, полученного при взаимодействии разбавленного раствора нитрата серебра с избытком бромида натрия. Какой заряд будет иметь гранула?
- •18. Как можно получить гидрозоли сульфата кальция с различным знаком заряда коллоидных частиц? Напишите схемы строения мицеллы золя для каждого случая
- •19. Потенциалолределяющими ионами золя бромида серебра оказались ионы серебра. Напишите схему строения мицеллы этого золя
- •20. Дайте общую характеристику явления адсорбции. Почему адсорбция является наиболее эффективным регулятором поверхностных свойств дисперсных систем?
- •21. Объясните принцип классификации веществ на поверхностно-активные и поверхностно-инактивные
- •23. Укажите наиболее существенные особенности адсорбции пав на границе раздела двух жидкостей
- •24. Укажите наиболее существенные особенности адсорбции пав на поверхности твердых тел
- •25. По какому признаку вещества относят к высокомолекулярным соединениям?
- •27. Что такое набухание? Какие стадии в нем различают?
- •28. По каким признакам растворы высокомолекулярных соединений сходны с коллоидным растворами?
- •29. Чем отличается денатурация от коацервации?
- •31. Что называется суспензией? Какой вид устойчивости для нее характерен?
- •32. Что представляют собой эмульсии? Как их классифицируют?
- •33. Какие дисперсные системы называют пенами?
- •34. Что такое аэрозоли. Какими основными свойствами они обладают?
Размещено на http://www.allbest.ru/
1. Какое положение занимают коллоидные системы в общей системе дисперсных систем?
дисперсный эмульсия золь раствор коагуляция
Коллоидные системы относятся к дисперсным системам – системам, где одно вещество в виде частиц различной величины распределено в другом. Дисперсные системы чрезвычайно многообразны; практически всякая реальная система является дисперсной. Дисперсные системы классифицируют прежде всего по размеру частиц дисперсной фазы (или степени дисперсности); кроме того, их разделяют на группы, различающиеся по природе и агрегатному состоянию дисперсной фазы и дисперсионной среды.
Если дисперсионной средой является жидкость, а дисперсной фазой – твердые частицы, система называется взвесью или суспензией; если дисперсная фаза представляет собой капельки жидкости, то систему называют эмульсией. Эмульсии, в свою очередь, подразделяют на два типа: прямые, или "масло в воде" (когда дисперсная фаза – неполярная жидкость, а дисперсионная среда – полярная жидкость) и обратные, или "вода в масле" (когда полярная жидкость диспергирована в неполярной). Среди дисперсных систем выделяют также пены (газ диспергирован в жидкости) и пористые тела (твердая фаза, в которой диспергированы газ либо жидкость).
Коллоидные системы, в свою очередь, подразделяются на две группы, резко отличные по характеру взаимодействий между частицами дисперсной фазы и дисперсионной среды – лиофобные коллоидные растворы (золи) и растворы высокомолекулярных соединений (ВМС), которые ранее называли лиофильными коллоидами. К лиофобным коллоидам относятся системы, в которых частицы дисперсной фазы слабо взаимодействуют с дисперсионной средой; эти системы могут быть получены только с затратой энергии и устойчивы лишь в присутствии стабилизаторов.
Растворы ВМС образуются самопроизвольно благодаря сильному взаимодействию частиц дисперсной фазы с дисперсионной средой и способны сохранять устойчивость без стабилизаторов. Лиофобные коллоиды и растворы ВМС различаются также и структурой частиц, составляющих дисперсную фазу. Для лиофобных коллоидов единицей структуры является сложный многокомпонентный агрегат переменного состава – мицелла, для растворов ВМС – макромолекула.
2. Что такое степень дисперсности? Как классифицируются дисперсные системы по размеру частиц дисперсной фазы?
Cтепень дисперсности:
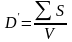 ,
[см-1;
м-1],
,
[см-1;
м-1],
где S - суммарная межфазная поверхность или поверхность всех частиц дисперсной фазы; V - объем частиц дисперсной фазы.
По степени дисперсности выделяют обычно следующие классы дисперсных систем:
Грубодисперсные системы – системы, размер частиц дисперсной фазы в которых превышает 10-7 м.
Коллоидные системы – системы, размер частиц дисперсной фазы в которых составляет 10-7 – 10-9 м. Коллоидные системы характеризуются гетерогенностью, т.е. наличием поверхностей раздела фаз и очень большим значением удельной поверхности дисперсной фазы. Это обусловливает значительный вклад поверхностной фазы в состояние системы и приводит к появлению у коллоидных систем особых, присущих только им, свойств.
Иногда выделяют молекулярно(ионно)-дисперсные системы, которые, строго говоря, являются истинными растворами, т.е. гомогенными системами, поскольку в них нет поверхностей раздела фаз.
Основные типы дисперсных систем
Дисперсная фаза |
Дисперсионная среда |
Условное обозначение |
Примеры дисперсных систем |
Жидкость |
Газ |
ж/г |
Туман, облака, жидкие аэрозоли |
Твердое тело |
Газ |
т/г |
Дым, пыль, твердые аэрозоли |
Газ |
Жидкость |
г/ж |
Пены, газовые эмульсии |
Жидкость |
Жидкость |
ж/ж |
Эмульсии (молоко, латекс) |
Твердое тело |
Жидкость |
т/ж |
Суспензии, коллоидные растворы, гели, пасты |
Газ |
Твердое тело |
г/т |
Твердые пены, пористые тела (пенопласты, силикагель, пемза) |
Жидкость |
Твердое тело |
ж/т |
Жемчуг, опал |
Твердое тело |
Твердое тело |
т/т |
Цветные стекла, сплавы |
По дисперсности различают:
а) грубодисперсные системы, для них D < 103 [1/см] (рис. 1.1.1.3);
б) микрогетерогенные системы, для них D = 103 - 105 [1/см];
в) ультрамикрогетерогенные системы, для них D = 105 - 107 [1/см].
