
- •1.Техническая термодинамика. Определение. Общие сведения.
- •2.Термодинамическая система. Определение.
- •3.Термодинамический процесс. Работа процесса. I – закон термодинамики.
- •4.Диаграммы термодинамических процессов в pv, ts и hS координатах.
- •5.Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона).
- •6.Термодинамические процессы изменения состояния газа.
- •Изохорные процессы в p - t координатах:
- •Изобарные процессы в V - t координатах
- •Изотермические процессы в p-V координатах
- •7. Смеси идеальных газов.
- •8.Теплоемкость газов.
- •9.Истечение газов.
- •10.Теплообмен. Виды теплообмена.
- •Виды теплообмена:
- •11. Теплопроводность. Основы теории.
- •12. Конвективный теплообмен.
- •13.Факторы влияющие на интенсивность теплообмена.
- •14.Лучистый теплообмен.
- •15.Круговой процесс. Цикл Карно.
- •Цикл Карно и максимальный кпд тепловой машины
- •16.Параметры состояния термодинамической системы (давление, температура, удельный объем).
- •17.Энтальпия. Энтропия. Определение. Физический смысл. Размерность.
- •18.Политропный процесс. Частные случаи политропного процесса.
- •В зависимости от процесса можно определить значение n:
- •20. Уравнение состояния реальных газов.
- •21.Параметры и функции состояния воды и водяного пара.
- •22. Процесс парообразования в pv-координатах.
- •23.Второй закон термодинамики
- •24. Принцип работы турбины.
- •25. Паротурбинные установки. Циклы пту.
- •Циклы паротурбинных установок (пту)
- •26. Газотурбинные установки. Циклы газотурбинных установок (гту)
- •27.Методе повышения экономичности работы паротурбинных и газотурбинных установок.
- •28.Промышленные холодильные установки. Циклы холодильных установок.
- •Циклы холодильных установок
- •29. Теплопередача. Общий вид уравнения.
- •Основное уравнение теплоотдачи
- •30.Цикл Ренкина.
- •Кпд цикла
- •Обратный цикл Ренкина
- •31.Цикл двигателей внутреннего сгорания.
- •Типы двс
- •Газотурбинный двс
- •Двс классифицируют:
- •Циклы работы поршневых двс
- •32.Паросиловые установки. Перегрев пара. Термический кпд. Удельный расход пара.
- •Перегретый пар
- •33.Котельные установки. Типы котлов и конструктивные особенности.
- •34.Котельно-вспомогательное оборудование. Назначение и основные характеристики.
- •35.Тепловой баланс котлоагрегата.
- •36.Конструктивные особенности паровых и водонагревательных котлов.
- •37.Водоподготовка и водный режим паровых водогрейных котлов. Водоподготовка
- •Новыми высокотехнологичными элементами систем водоподготовки являются:
- •38.Топливо. Виды топлив. Общая характеристика.
- •Основные современные виды топлива
- •Жидкие топлива
- •Газообразные топлива
- •Дисперсные системы, растворы
- •Нетипичные топлива
- •39.Процессы горения. Расчет процесса горения.
- •Статическая сирена для процессов горения
- •40.Топки котлов и печей. Классификация и характеристика топочных устройств.
- •Классификация и конструктивные особенности топочных устройств
- •41.Особенности сжигания твердых и газообразных топлив. Особенности горения твердого топлива
- •Особенности сжигания газообразного топлива
- •42.Тепловые электрические станции. Общин сведения.
- •43.Тепловые сети.
- •44.Основные элементы тепловых сетей.
- •45. Расчет тепловых сетей
- •46.Системы теплоснабжения (водяные теплосети).
- •47.Системы пароснабжения. Сбор и возврат конденсата.
- •Сбор и возврат конденсата.
- •Возможные проблемы:
- •48.Режимы работы систем теплоснабжения.
- •49.Температурные графики систем отопления и горячего водоснабжения. Температурный график отопления
- •50.Наладка и регулирования систем теплоснабжения. Наладка систем теплоснабжения
- •Регулирование системы отопления
- •51.Теплообменные аппараты. Основные типы. Конструкция.
- •Основные типы
- •Конструкции теплообменников
- •52.Расчет теплообменных аппаратов.
- •Уравнение теплопередачи:
- •Величину произведения
- •Для аппаратов с прямотоком
- •Для аппаратов с противотоком
- •53.Сушильные установки.
- •54.Промышленные печи.
20. Уравнение состояния реальных газов.
Наиболее простым и качественно верно отображающим поведение реального газа, является уравнение Ван-дер-Ваальса:
(P + a/n2)·(n – b) = R·T . (6.3)
а, b – постоянные величины, первая учитывает силы взаимодействия, вторая учитывает размер молекул.
a/n2 – характеризует добавочное давление, под которым находится реальный газ вследствие сил сцепления между молекулами и называется внутренним давлением. Для жидких тел это давление имеет большие значения (например, для воды при 200С составляет 1050 Мпа), а для газов из-за малых сил сцепления молекул оно очень мало. Поэтому внешнее давление, под которым находится жидкость, оказывает ничтожное влияние на её объем, и жидкость считают несжимаемой. В газах в виду малости значения a/n2 внешнее давление легко изменяет их объем.
21.Параметры и функции состояния воды и водяного пара.
Известно, что любое вещество в зависимости от внешних условий (давления и температуры) может находиться в газообразном, жидком и твердом агрегатных состояниях, или фазах, а также одновременно находиться в двух или трех состояниях.
Переход вещества из одного агрегатного состояния в другое называется фазовым переходом, или фазовым превращением. Вещество в разных агрегатных состояниях имеет различные свойства, в частности плотность. Это различие объясняется характером межмолекулярного взаимодействия.
Переход вещества из твердого состояния в жидкое называется плавлением, из жидкого в газообразное — испарением, из твердого в газообразное — сублимацией. Обратные процессы соответственно называются затвердеванием, или кристаллизацией, конденсацией и де-сублимацией.
Процесс получения пара из жидкости может осуществляться испарением и кипением.
Испарением называется парообразование, происходящее только со свободной поверхности жидкости и при любой температуре.
Кипением называется бурное парообразование по всей массе жидкости, которое происходит при сообщении жидкости через стенку сосуда определенного количества теплоты. При этом образовавшиеся у стенок сосуда и внутри жидкости пузырьки пара, увеличиваясь в объеме, поднимаются на поверхность жидкости.
Процесс парообразования начинается при достижении жидкостью температуры кипения, которая называется температурой насыщения tн и на протяжении всего процесса остается неизменной. Температура кипения, или температура насыщения, tн зависит от природы вещества и давления, причем с повышением давления tн увеличивается. Давление, соответствующее tн называется давлением насыщения рн.
Насыщенным паром называют пар, который образовался в процессе кипения и находится в динамическом равновесии с жидкостью. Насыщенный пар по своему состоянию бывает сухим насыщенным и влажным насыщенным.
Сухой насыщенный пар представляет собой пар, не содержащий капель жидкости и имеющий температуру насыщения (t=tн) при данном давлении.
Влажный насыщенный пар – это равновесная смесь, состоящая из капель жидкости, находящейся при температуре кипения, и сухого нсыщенного пара.
Отношение массы сухого насыщенного пара mс.п. к массе влажного насыщенного пара mв.п. называется степенью сухости х влажного пара, то есть
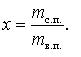
Очевидно, что для жидкости х=0, для сухого насыщенного пара х=1.
Если к сухому насыщенному пару продолжать подводить теплоту, то его температура увеличится. Пар, температура которого при данном давлении больше, чем температура насыщения (t>tн), называется перегретым. Другими словами говоря перегретый пар – это пар, находящийся при температуре, превышающей температуру кипения жидкости при давлении, равном давлению перегретого пара. Величина превышения температурой пара температуры кипения жидкости называется степенью перегрева пара.
Водяной пар является реальным рабочим телом и может находиться в трёх состояниях: влажного насыщения, сухого насыщения и в перегретом состоянии. Для технических нужд водяной пар получают в паровых котлах (парогенераторах), где специально поддерживается постоянное давление.
